用天然气合成氨的工艺流程示意如下: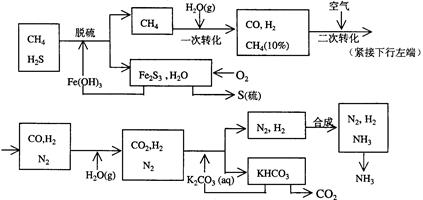
依据上述流程,完成下列填空:
(1)天然气脱硫时的化学方程式是
(2)n mol CH4经一次转化后产生CO 0.9n mol、产生H2 mol(用含n的代数式表示)
(3)K2CO3(aq)和 CO2反应在加压下进行,加压的理论依据是 (多选扣分)
(a)相似相溶原理 (b)勒沙特列原理 (c)酸碱中和原理
(4)由KHCO3分解得到的CO2可以用于
(写出CO2的一种重要用途)。
(5)整个流程有三处循环,一是Fe(OH)3循环,二是K2CO3(aq)循环,请在上述流程图中标出第三处循环(循环方向、循环物质)。
A—F 六种有机物,在一定条件下,按下图发生转化。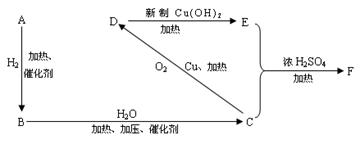
又知烃A的密度(在标准状况下)是1.16 g/L,试回答下列问题:
(1)有机物的结构简式:A.,F.。
(2)写出化学方程式:反应B→C ___,
反应C→D
反应D→E_ ___。
苹果醋(ACV)是一种由苹果发酵而成的酸性饮品,具有解毒。降脂等药效,主要酸性物质为苹果酸。苹果酸在分离提纯后的化学分析如下:①相对分子质量不超过150,完全燃烧后只生成CO2和H2O,分子中C、H质量分数分别为w(C)=35 .82%。
.82%。 w(H)=4.48%;②1 mol该酸与足量的NaHCO3反应放出44.8
w(H)=4.48%;②1 mol该酸与足量的NaHCO3反应放出44.8
 L CO2,与足量的Na反应放出33.6 L H2(气体体积均已折算为标准状况);③该
L CO2,与足量的Na反应放出33.6 L H2(气体体积均已折算为标准状况);③该 分子中存在四种化学环境不同的碳原子,氢原子处于五种不同的化学环境。回答下列问题:
分子中存在四种化学环境不同的碳原子,氢原子处于五种不同的化学环境。回答下列问题:
(1)苹果酸的分子式为,分子中有个羧基。
(2)写出苹果酸的结构简式。
(3)苹果酸的同分异构体 中,符合上述①、②两个条件的有(写出结构简式):
中,符合上述①、②两个条件的有(写出结构简式): 、
、 。
。
肼(N2H4)又称联氨,是一种可燃性的液体,可用作火箭燃料。已知在25℃,101kPa时,32.0gN2H4在氧气中完全燃烧生成氮气,放出热量624kJ
(1)写出该状态下N2H4完全燃烧反应的热化学方程式
。
(2)肼—空气燃料电池是一种碱性燃料电池,电解质溶液是20%~30%的KOH溶液。肼—空气燃料电池放电时:正极的电极反应式是
。
( 3)下图是一个电化学过程示意图。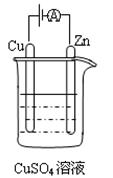
①锌片上发生的电极反应式是。
②假设使用肼—空气燃料电池作为本过程中的电源,铜片的质量变化128g,则肼一空气燃料电池理论上需要标准状况下的空气
L(假设空气中氧气体积含量为20%)
亚硫酸钠是食品加工中广泛使用的漂白剂、防腐剂和抗氧化剂,其在食品中的残留量通常以二氧化硫含量计算。
(1)亚硫酸盐具有一定的毒性,长期摄入过量的亚硫酸盐,红细胞和血红蛋白会减少,钙的吸收也会减少,原因是。
检验某黑木耳中是否含有亚硫酸盐的简单方法是:将黑木耳样品剪成碎末放入烧杯,加入20mL水和10mL盐酸,加热一会儿,滴入试剂A,观察现象既可。
(2)加热的作用是,加热时间不能太长的原因是。
(3)试剂A是。
在足量的亚硫酸钠溶液中加入1~2滴液溴,振荡后溶液变为无色。
(4)写出以上反应的离子方程式 。
(5)以上反应后的溶液中含有SO32-、HSO3-、SO42-、Br-、OH-等阴离子。设计实验检验SO42- 和Br-,写出实验方法。试剂不限。
| 实验操作 |
预期现象与结论 |
| 步骤1: |
|
| 步骤2: |
工业上生产高氯酸(沸点:90oC)时还同时生产了亚氯酸钠,其工艺流程如下: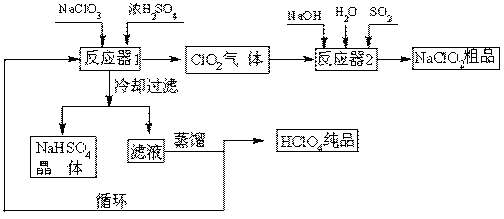
(1)冷却过滤的目的。
(2)通入反应器2的SO2作用是;反应器2中发生反应的离子方程式为。
(3)循环使用的物质是。
(4)可以通过蒸馏滤液的方法得到高氯酸的原因可能是。
(5)通过电解NaClO3水溶液的方法也可以制备NaClO4,进而可以制备HClO4,写出阳极的电极反应式。