(10分)实验室常用二氧化锰和浓盐酸反应制取氯气:MnO2+4HCl(浓) MnCl2 + Cl2↑+ 2H2O。某学习小组利用此原理设计如图所示装置制取氯气并探究其性质。
MnCl2 + Cl2↑+ 2H2O。某学习小组利用此原理设计如图所示装置制取氯气并探究其性质。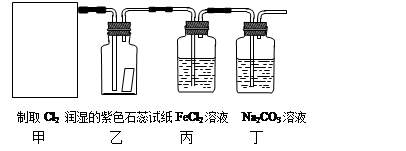
⑴在该实验中,甲部分的装置是 (填写字母)。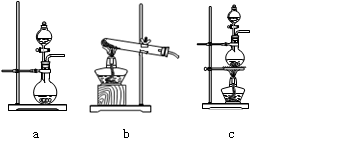
⑵乙装置中可观察到的颜色变化为: 。
⑶丙装置中FeCl2溶液与Cl2反应的离子方程式是 。
⑷丁装置中通入少量Cl2,可制得某种生活中常用的漂白、消毒的物质。已知碳酸的酸性强于次氯酸,则丙中发生反应的化学方程式是 。
⑸该实验存在明显的缺陷,改进的方法是 。
为了探究HClO的漂白性,某同学设计了如下的实验。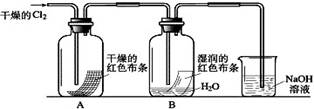
(1)通入Cl2后,从集气瓶A中干燥的红色布条的现象可得出的结论是;从集气瓶B中湿润的红色布条的现象可得出的结论是,其中发生的反应的化学方程式为。
(2)为了确证是HClO使湿润的红色布条褪色,你认为还应增加的实验是。
(3)烧杯中溶液所起的作用是,烧杯中所发生反应的化学方程式为。
(4)为保证实验安全,当氯气以每分钟1.12L(标准状况)的流速匀速通入时,若实验需耗时4分钟,小烧杯中盛2 mol·L—1的NaOH溶液的体积至少应为__________mL。
实验室欲配制250mL 0.2 mol·L-1的碳酸钠溶液,回答下列问题:
可供选择的仪器:①量筒②胶头滴管③托盘天平④药匙⑤烧瓶⑥烧杯
(1)通过计算可知,应用托盘天平称取g碳酸钠晶体(Na2CO3•10H2O)。
(2)配制过程需要的仪器______________(填序号),还缺少的仪器有。
(3)配制时,正确的操作顺序是(用字母表示,每个字母只能用一次)_____________;
| A.用30mL水洗涤烧杯2~3次,洗涤液均注入容量瓶 |
| B.用托盘天平准确称取所需的Na2CO3固体的质量,放入烧杯中,再加入少量水(约30mL),用玻璃棒慢慢搅动,使其充分溶解 |
| C.将已冷却的溶液沿玻璃棒注入250mL的容量瓶中 |
| D.将容量瓶盖紧,振荡,摇匀 |
E.改用胶头滴管加水,使溶液凹面恰好与刻度相切
F.继续往容量瓶内小心加水,直到液面接近刻度1~2cm处
(4)若出现如下情况,对所配溶液浓度将有何影响(填“偏高”、“偏低”或“无影响”)。若没有进行A操作______________;若定容时俯视刻度线_______________。
某校学生用中和滴定法测定某NaOH溶液的物质的量浓度,选甲基橙作指示剂。
⑴盛装0.2000 mol/L盐酸标准液应该用式滴定管。
⑵滴定时,左手控制滴定管,右手摇动锥形瓶,眼睛注视__,直到因加入一滴盐酸后,溶液由黄色变为橙色,并为止。
⑶滴定操作可分解为如下几步:
①检查滴定管是否漏水
②取一定体积的待测液于锥形瓶中
③用标准溶液润洗盛标准溶液的滴定管,用待测液润洗盛待测液的滴定管
④装标准溶液和待测液并调整液面(记录初读数)
⑤用蒸馏水洗涤玻璃仪器
⑥滴定操作
正确的操作顺序为:。
⑷有关数据记录如下:
| 实验序号 |
待测液体积(mL) |
所消耗盐酸标准液的体积(mL) |
|
| 滴定前 |
滴定后 |
||
| 1 |
20.00 |
0.50 |
20.70 |
| 2 |
20.00 |
6.00 |
26.00 |
| 3 |
20.00 |
1.40 |
21.20 |
则NaOH溶液的物质的量浓度为______________mol/L。
⑸若只用蒸馏水冲洗锥形瓶,则测定结果_________________,若滴定前平视读数,滴定终点时俯视读数,则会使所测酸的浓度值。(填“无影响”、“偏高”或“偏低”)。
如何防止铁的腐蚀是工业上研究的重点内容。为研究铁锈蚀的影响因素,某同学做了如下探究实验:
| 序号 |
内容 |
实验现象 |
| 1 |
常温下将铁丝放在干燥空气中一个月 |
干燥的铁丝表面依然光亮 |
| 2 |
常温下将铁丝放在潮湿空气中一小时 |
铁丝表面依然光亮 |
| 3 |
常温下将铁丝放在潮湿空气中一个月 |
铁丝表面已变得灰暗 |
| 4 |
将潮湿的铁丝放在常温的氧气流中一小时 |
铁丝表面略显灰暗 |
| 5 |
将潮湿的铁丝放在高于常温的氧气流中一小时 |
铁丝表面已变得灰暗 |
| 6 |
将浸过氯化钠溶液的铁丝放在高于常温的氧气流中一小时 |
铁丝表面灰暗程度比实验5严重 |
回答以下问题:
⑴上述实验中发生了电化学腐蚀的是(填实验序号),在电化学腐蚀中,负极反应是_______________,正极反应是_______________。
⑵由该实验可知,可以影响铁锈蚀速率的因素是。
⑶下列对金属制品采取的防护方法不正确的是(填序号)。
A.在电线的外面包上一层塑料层
B.在自行车钢圈上镀上一层金属铬
C.在海轮的铁制外壳上焊上铜块
某校课外活动小组为了探究铜与稀硝酸反应产生的气体主要是NO而设计了下列实验,装置如图所示(加热装置和固定装置均已略去)。图中K为止水夹(处于关闭状态),F是一半空的注射器。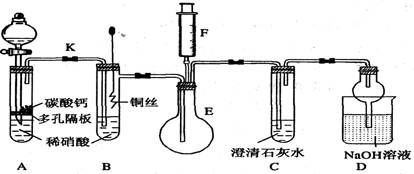
请回答有关问题:
(1) 设计装置A的目的是;
为达到此目的,应进行的操作是打开K,且打开分液漏斗活塞,当装置C中产生
时,关闭K。
(2) 在完成(1)中的“操作”后,将装置B中铜丝插入稀硝酸,并微热之,观察到装置B中的
现象是;
B中反应的离子方程式为:。
(3) 装置E和F的作用是;为实现此作用,其操作方法是。
(4) 装置D的作用是吸收多余的氮氧化物,防止污染空气,兼有的功能。