对照试验是化学研究中常用的一种方法。某研究小组对铁生锈进行如下研究。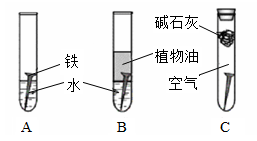
(1)经过较长时间后发现:上述图中的铁钉最容易生锈的是 。
(2)在铁钉的锈蚀过程中,Fe发生了 (填“氧化”或“还原”)反应。
(3)铁生锈的外部条件是 。
(4)钢铁工业史国家工业的基础。下列措施能起到防腐作用的是 。
A.刷油漆 B.包上一层塑料层 C.连接一定数量镁块
氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用。请回答下列问题:
(1)用CH4 催化还原NOx 可以消除氮氧化物的污染。例如:
CH4(g) + 4NO2(g) = 4NO(g)+CO2(g) + 2H2O(g)ΔH1=-574 kJ·mol-1
CH4(g) + 4NO(g) =" 2" N2(g)+CO2(g) + 2H2O(g)ΔH2
若1 mol CH4 还原NO2 至N2,整个过程中放出的热量为867 kJ,则ΔH2=;
(2)工业合成氨气需要的反应条件非常高且产量低,而一些科学家采用高质子导电性的SCY陶瓷(能传递H+)实现氨的电化学合成,从而大大提高了氮气和氢气的转化率。电化学合成氨过程的总反应式为: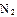 +3
+3
 2
2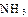 ,则在电化学合成氨的过程中,阴极反应式为_________;
,则在电化学合成氨的过程中,阴极反应式为_________;
(3)在一定条件下,将l mol N2 与3 mol H2 混合于一个10 L密闭容器中,反应达到平衡时,A点混合气体中氨占25%,试回答:
①N2的转化率为;
②右图中在状态A时,平衡常数 KA(填写代入数值
的表达式,不要求算出具体数值);当温度由T1变化到T2时,
KA KB(填“>”、“<”或“=”)。
③在容积固定的密闭容器中发生上述反应,各物质的浓度如下表:
反应从0 min到3 min之间,H2的反应速率为;反应在3 min时,条件发生了改变,改变的条件可能是(填序号)。
a.使用催化剂 b.降低温度 c.增加H2的浓度
现有A、B、C、D、E五种短周期元素,已知他们的原子序数依次增大,元素A的原子只有一个电子层;又知元素A能分别与元素B、C、D形成电子总数相等的化合物分
子X、Y、Z,Y有刺激性气味,Z常温下为液态,元素E的单质的水溶液有漂白性。
请回答下列问题:
(1)元素E的单质的饱和溶液与石灰石反应后所得溶液的漂白性增强的原因是 ;
(2) 在锅炉水中加入C2A4,可以把锅炉表面的氧化铁还原为结构紧密的四氧化三铁保护层,C2A4被氧化,且反应中无污染物生成,写出反应的化学方程式(不必配平),1 mol C2A4参加反应转移电子的数目为,氧化产物的化学式为;
(3)化合物Y与元素C的最高正价氧化物的水化物按物质的量比为2:1完全反应后的水溶液呈性(填“酸”“碱”或“中”),溶液中离子浓度由大到小的顺序为;
(4)用X、D2 和能传导O2-的的固体电解质组成的原电池中,负极的电极反应式为。
(5)A、B、D三种元素可以形成最简式为B2A4D且有香味的有机物,该有机物在酸性条件下可以水解,生成含碳原子数相同的两种常见有机物,这两种有机物均可用作食品调味剂。则这种有香味的有机物在一定条件下水解的化学方程式是。
某化学研究性学习小组为探究某品牌花生油中不饱和脂肪酸的含量,进行了如下实验:
步骤Ⅰ:称取0.4g花生油样品,置于两个干燥的碘瓶(如图)内,加入10mL四氯化碳,轻轻摇动使油全部溶解。向碘瓶中加入25.00mL含0.01mol IBr的无水乙酸溶液,盖好瓶塞,在玻璃塞与瓶口之间滴加数滴10%碘化钾溶液封闭缝隙,以免IBr的挥发损失。
步骤Ⅱ:在暗处放置30min,并不时轻轻摇动。30min后,小心地打开玻璃塞,用新配制的10%碘化钾10mL和蒸馏水50mL把玻璃塞和瓶颈上的液体冲洗入瓶内。
步骤Ⅲ:加入指示剂,用0.1mol·L-1硫代硫酸钠溶液滴定,用力振荡碘瓶,直至终点。
测定过程中发生的相关反应如下:
① +IBr →
+IBr →
②IBr+KI=I2+KBr
③I2+2S2O32-=2I-+S4O62-
请回答下列问题:
⑴已知卤素互化物IBr的性质与卤素单质类似,实验中准确量取IBr溶液应用▲,用方程式表示碘瓶必须干燥的原因▲。
⑵步骤Ⅱ中碘瓶在暗处放置30min,并不时轻轻摇动的原因是▲。
⑶步骤Ⅲ中所加指示剂为▲,滴定终点的现象▲。
⑷反应结束后从液体混合物中回收四氯化碳,则所需操作有▲。
已知:A、B、C、D、E为周期表1~36号中的元素,它们的原子序数逐渐增大。A的基态原子有3个不同的能级,各能级中电子数相等;C的基态原子2p能级上的未成对电子数与A原子相同;C2—离子D2+离子具有相同的、稳定的电子层结构;E的基态原子的外围电子排布式为3d84s2。
 请回答下列问题:
请回答下列问题:
⑴A、B、C、D四种元素中,电负性最大的是▲(填元素符号)。
⑵B的氢化物的沸点远高于A的氢化物的主要原因是▲。
⑶由A、B、C形成的离子CAB-与AC2互为等电子体,则CAB-中A原子的杂化方式为▲。
⑷E2+离子能与AC分子形成[E(AC)4]2+,其原因是AC分子中含有▲。
⑸最近发现,只含A、D、E三种元素的一种晶体(晶胞如右图所示)具有超导性。A原子的配位数为▲;该晶体的化学式为▲。
目前,聚氯乙烯塑料(PVC)占塑料消费量的30%以上,BICM法用乙烯、氯气等为原料合成PVC,其工艺流程如下。
⑴一定条件下,HCl与O2反应制取Cl2的方法称为地康法,其热化学反应方程式为:
4HCl(g)+O2(g)  2Cl2(g)+2H2O(g)ΔH=-114.4kJ·mol-1。
2Cl2(g)+2H2O(g)ΔH=-114.4kJ·mol-1。
升高温度,该反应的化学平衡常数K会▲。
A.增大 B.减小 C.不变 D.无法确定
⑵一定温度下某体积可变的容器中充入4LHCl气体和6L空气(氧气占20%),充分反应后气体体积为9.2L。该反应中HCl气体的转化率为▲。
⑶假设BICM法中各步反应的转化率均为100%,计算生产1000吨PVC需要购得的氯气质量。