铁和铝是两种重要的金属,它们的单质及化合物有着各自的性质。
(1)在一定温度下,氧化铁可以与一氧化碳发生下列反应:Fe2O3(s)+3CO(g) 2Fe(s)+3CO2(g)
2Fe(s)+3CO2(g)
①该反应的平衡常数表达式为:K= 。
②该温度下,在2L盛有Fe2O3粉末的密闭容器中通入CO气体,10min后,生成了单质铁11.2g。则10min内CO的平均反应速率为 。
(2)请用上述反应中某种气体的有关物理量来说明该反应已达到平衡状态:
① ② 。
(3)某些金属氧化物粉末和Al粉在镁条的引燃下可以发生铝热反应。下列反应速率(v)
和温度(T)的关系示意图中与铝热反应最接近的是 。
(4)写出氢氧化铝在水中发生酸式电离的电离方程式: ,欲使上述体系中Al3+浓度增加,可加入的物质是 。
在HF、H2O、NH3、CH4、CO2-3、CO2、HI分子中
(1)CO2-3的价层电子对的空间构型为,离子的空间构型为。
(2)以极性键相结合,具有正四面体结构的非极性分子是。
(3)以极性键相结合,具有三角锥型结构的极性分子是。
(4)以极性键相结合,具有折线型结构的极性分子是。
(5)以极性键相结合,而且分子极性最大的是。
(6)NH3的价层电子对的空间构型为,分子的空间构型为
1994年度诺贝尔化学奖授予为研究臭氧做出贡献的化学家。O3能吸收有害紫外线,保护人类赖以生存的空间。O3的分子结构如图,呈V型,两个O----O键的夹角为116.5o。三个原子以一个O原子为中心,另外两个O原子分别构成一个共价键;中间O原子提供2个电子,旁边两个O原子各提供一个电子,构成一个特殊的化学键——三个O原子均等地享有这个电子。请回答: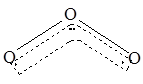
(1)臭氧与氧气的关系是_____________
(2)写出下列分子与O3分子的结构最相似的是_______________
| A.H2O | B.CO2 | C.SO2 | D.BeCl2 |
(3)分子中某原子有一对或几对没有跟其他原子共用的价电子叫孤对电子,那么O3分子有对孤对电子。
(4)O3分子是否为极性分子(填是或否)。
(5)O3具有强氧化性,它能氧化PbS为PbSO4而O2不能,试配平:
PbS +O3 ====PbSO4 +O2
生成1mol O2的转移电子物质的量为mol。
20世纪30年代,Eyring和Pelzer在碰撞理论的基础上提出化学反应的过渡态理论:化学反应并不是通过简单的碰撞就能完成的,而是在反应物到生成物的过程中经过一个高能量过渡态。分析图中信息,回答下列问题:
(1)图一是NO2和CO反应生成CO2和NO过程中能量变化示意图,请写出NO2和CO反应的热化学方程式:。在反应体系中加入催化剂,E1和E2的变化是:E1_________,E2________(填“增大”、“减小”或“不变”),对反应热是否有影响?_______________,原因是_________。
(2)图二是红磷P(s)和Cl2(g)发生反应生成PCl3(g)和PCl5(g)的反应过程与能量关系图(图中的△H表示生成1mol产物的数据)。根据图二回答下列问题:
① P(s)和Cl2(g)反应生成PCl3(g)的热化学方程式。
② P(s)和Cl2(g)分两步反应生成1molPCl5(g)的△H1与P(s)和Cl2(g)一步反应生成1molPCl5(g)的△H2关系是:△H2______△H1(填“大于”、“小于”或“等于”),原因是。
写出下列反应的化学反应方程式,并判断其反应类型。
①乙烯与氯化氢反应:,属于反应;
②由苯制取溴苯:,属于反应;
0.1 mol某液态烷烃完全燃烧需要消耗0.8 mol 氧气,写出符合该物质化学式的烷烃的结构简式并写出每种物质系统命名的名称