化学上常用燃烧法确定有机物的组成。下图装置是用燃烧法确定烃或烃的含氧衍生物分子式的常用装置,这种方法是在电炉加热时用纯氧氧化管内样品,根据产物的质量确定有机物的组成。(已知A中发生的反应为:2H2O2=2H2O+O2↑)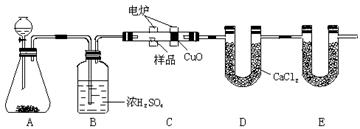
回答下列问题:
(1)C装置(燃烧管)中CuO的作用是 。
(2)写出E装置中所盛放物质的名称 ,
它的作用是 。
(3)若将B装置去掉会对实验结果造成什么影响? 。
(4)若准确称取1.20 g样品(烃或烃的含氧衍生物)。经充分燃烧后,E管质量增加1.76 g,D管质量增加0.72 g,则该有机物的实验式为 。
(5)从定量测定准确角度去考虑,该装置应怎样进一步改进
。
中学实验常用如图所示装置制取少量溴苯。在烧瓶a中装的试剂是苯、溴和铁粉。请填写下列空白。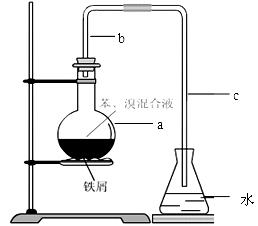
⑴导管b的作用有两个:一是导气,二是兼起的作用;
⑵a中反应的化学方程式为;
⑶该实验得到的是粗苯,为了除去其中的溴,要用到的一种常用除杂操作方法是,提纯溴苯的具体步骤有:
①蒸馏;②水洗;③用干燥剂干燥;④10%NaOH溶液洗;⑤水洗。
正确的操作顺序为()
| A.①②③④⑤ | B.②④⑤③① | C.④②③①⑤ | D.②④①⑤③ |
⑷为证明苯和溴发生的是取代反应而不是加成反应,可向水中加入;但该实验不够严密,为此必须在导管a、b之间加上一盛有的洗气瓶,目的是。
MgSO4·7H2O医药上用作泻剂。工业上用氯碱工业中的一次盐泥为原料生产。已知一次盐泥中含有镁、钙、铁、铝、锰的硅酸盐和碳酸盐等成分。主要工艺如下: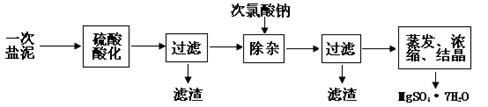
(1)用硫酸调整溶液pH到1~2,硫酸的作用是。 (2)加次氯酸钠溶液至pH=5~6并加热煮沸约5~10分钟,滤渣中主要含MnO2和另两种沉淀,另两种沉淀是(写化学式)。其中次氯酸钠溶液将MnSO4转化为MnO2的离子方程式为:。
(2)加次氯酸钠溶液至pH=5~6并加热煮沸约5~10分钟,滤渣中主要含MnO2和另两种沉淀,另两种沉淀是(写化学式)。其中次氯酸钠溶液将MnSO4转化为MnO2的离子方程式为:。
(3)若除杂后过滤,发现滤液发黄,需采取的措施是。
(4)过滤后晶体常用丙酮代替蒸馏水洗涤的目的是。
(5)晶体中结晶水含量的测定:准确称取0.20g MgSO4·7H2O样品,放入已干燥至恒重的瓷坩埚,置于马弗炉中,在200℃脱水1小时。为准确确定脱水后的质量,还需要经过的操作有:冷却(干燥器中)至室温→。
(6)硫酸根离子质量分数的测定:准确称取自制的样品0.50g,用200mL水溶液,加入2mol·L-1HCl溶液5mL,将溶液加热至沸,在不断搅拌下逐滴加入5~6mL0.5mol·L-1BaCl2溶液,充分沉淀后,得沉淀0.466g,则样品中w(SO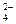 )=。
)=。
为了预防碘缺乏病,有关部门规定食盐中的碘含量(以I计)应在20~50 mg/Kg。制备KIO3的方法如下:
方法1:6I2+11KClO3+3H2O=6KH(IO3)2+5KCl+3Cl2↑;KH(IO3)2+KOH=2KIO3+H2O
方法2:碱性条件下,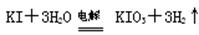
方法3: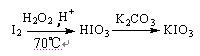
⑴与方法3相比方法1的不足是,方法2的不足是 。
⑵方法2选用的电极是惰性电极,则其阳极反应式是。
⑶方法3反应温度控制在70℃左右,不采用更高温度的主要原因是。
⑷制备纯净KIO3的实验步骤中,最后需将所得晶体最好使用洗涤2~3次,干燥后得产品。
⑸已知:KIO3+5KI+3H2SO4=3K2SO4+3I2+3H2O; I2+2S2O32-=2I-+S4O62-。为测定加碘食盐中碘的含量,设计的方案如下。请完善实验步骤并计算测定结果:
I2+2S2O32-=2I-+S4O62-。为测定加碘食盐中碘的含量,设计的方案如下。请完善实验步骤并计算测定结果:
a.准确称取w g食盐于锥形瓶中,再加适量蒸馏水使其完全溶解。
b.。
c.向锥形瓶中滴加2.0×10-3 mol/L Na2S2O3标准溶液至终点。
d.重复上述实验两次。
三次实验的数据记录如下表。则所测加碘食盐样品中的碘元素含量是mg/kg(以含w的代数式表示)。
| 滴定次数 |
盛标准Na2S2O3溶液的读数 |
|
| 滴定前刻度(/mL) |
滴定后刻度(/mL) |
|
| 1 |
1.02 |
11.03 |
| 2 |
2.00 |
11.99 |
| 3 |
0.20 |
10.20 |
实验室制乙烯时, 常因温度过高而发生副反应。部分乙醇跟浓硫酸反应生成二氧化硫.二氧化碳.水蒸气和炭黑。请用下列编号为①~⑥的实验装置设计一个实验, 以验证上述反应后的混合气中含有二氧化碳.二氧化硫和水蒸气。
(1)用装置的编号表示其连接顺序(按气体产物从左到右的流向)
(2)装置⑤中的固体药品为现象是
(3)装置①中的现象是,验证; 装置②中溴水的作用是,此时盛有澄清石灰水的装置④中出现,
某研究性学习小组查阅资料得知:漂白粉与硫酸溶液反应可制取氯气,化学方程式为:Ca(C1O)2+CaCl2+H2SO4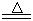 2CaSO4+2Cl2↑+2H2O,该组学生针对上述反应设计如下装置来制取氯气并验证其性质。
2CaSO4+2Cl2↑+2H2O,该组学生针对上述反应设计如下装置来制取氯气并验证其性质。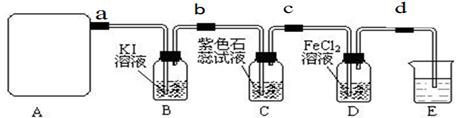
试回答下列问题:
(1)每生成1 mol Cl2,上述化学反应中转移的电子个数为______ (NA表示阿伏加德罗常数)。
(2)该实验中A处可选用装置__________ _____(填写甲.乙.丙或丁)。
(3)检查A装置的气密性的方法是用弹簧夹夹住处(填a.b.c或d)橡皮管,向分液漏斗中加水并打开活塞,当加到一定量时,停止加水,静止观察,当观察到分液漏斗中时,表明该装置不漏气 .
(4) 装置B中发生反应的离子方程式为_____________________。
(5)装置C中的现象为____________________________________
(6)装置E中的试剂是______________(任填一种合适试剂的名称),
其作用是______________________________
(7)请帮助该学习小组同学设计一个实验,证明装置D中有FeCl3生成(请简述实验 步骤)
步骤)
___________________________________________________________