资料显示:“氨气可在纯氧中安静燃烧,并生成无污染的产物……”。某校化学小组学生设计如图装置(图中铁夹等夹持装置已略去)进行氨气与氧气在不同条件下反应的实验。
(1)用装置A制取纯净、干燥的氨气,大试管内碳酸盐的化学式是________;碱石灰的作用是__________________。
(2)将产生的氨气与过量的氧气通到装置B(催化剂为铂石棉)中,用酒精喷灯加热:氨催化氧化的化学方程式是____________________________________;试管内气体变为红棕色,该反应的化学方程式是_________________________。
(3)将过量的氧气与A产生的氨气分别从a、b两管进气口通入到装置C中,并在b管上端点燃氨气:氨气安静燃烧的化学方程式是___________________。
实验室需要配制0.50 mol/L NaCl溶液480 mL,现使用NaCl固体配制,按下列操作步骤填上适当的文字,以使整个操作完整。
Ⅰ.(1)选择仪器。完成本实验所必需的仪器有:托盘天平(精确到0.1 g)、药匙、烧杯、玻璃棒、__________、_________________以及等质量的两片滤纸。
(2)计算。配制该溶液需取NaCl晶体________ g。
(3)称量。
①天平调平。 ②称量。 ③称量完毕,将药品倒入烧杯中。
(4)溶解、冷却,该步实验中需要使用玻璃棒,目的是___________________。
(5)转移、洗涤。在转移时应使用________引流,需要洗涤烧杯2~3次是为了_______________________。
(6)定容、摇匀。
(7)将配好的溶液静置一段时间后,倒入指定的试剂瓶中,并贴好标签,注明配制的时间、溶液名称及浓度。
(8)在配制过程中,某学生观察定容时液面情况如图所示,所配溶液的浓度会______(填“偏高”、“偏低”或“无影响”)。

Ⅱ.实验室利用如图装置进行中和热的测定,请回答下列问题:
(1)该图中有两处未画出,它们是________________,________________。
(2)在操作正确的前提下,提高中和热测定准确性的关键是_________________。
(3)如用0.5 mol/L的盐酸与NaOH固体进行实验,则实验中测得的“中和热”数值将________(填“偏大”、“偏小”、“不变”);原因是_______________。
下图是我校实验室化学试剂浓硫酸标签上的部分内容。
现需要480 mL 1 mol·L-1的稀硫酸。用该浓硫酸和蒸馏水配制,可供选用的仪器有:① 胶头滴管;②玻璃棒;③烧杯;④量筒。
请回答下列问题:
(1)配制稀硫酸时,还缺少的仪器有__________(写仪器名称)。
(2)该浓硫酸的物质的量浓度为 mol/L;所需浓硫酸的体积约为_______mL;
(3)定容时,若加入的水超过刻度线,必须采取的措施是
(4)下列操作对H2SO4的物质的量浓度有什么影响(偏高、偏低或无影响)?
①转移溶液后,未洗涤烧杯: ;
②容量瓶用水洗净后未烘干: ;
③定容时俯视容量瓶的刻度线: ;
④未将烧杯中的溶液冷却即注入容量瓶:________________。
(5)在配置过程中,下列操作不正确的是(填序号) 。
| A.使用容量瓶前检查它是否漏水 |
| B.容量瓶用蒸馏水洗净后,再用待配液润洗 |
| C.将准确量取的浓硫酸,注入已盛有100mL水的500mL的容量瓶中,加水至刻度线. |
| D.将硫酸溶于水后需冷却至室温再转移到容量瓶中 |
E.定容后塞好瓶塞,用食指顶住瓶塞,用另一只手的手指托住瓶底,把容量瓶倒转摇匀
(一)下列各组物质的分离或提纯,应选用下述方法的哪一种?(填序号)
A分液 B过滤 C萃取 D蒸馏 E结晶
从碘水中提取碘 ;分离植物油和水 ;
(二)实验室里需要纯净的氯化钠溶液,但手边只有混有硫酸钠、碳酸氢铵的氯化钠。某学生设计了如下方案: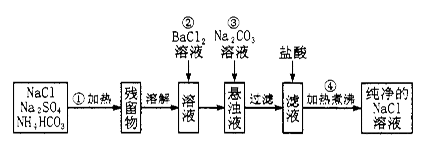
如果此方案正确,那么:
(1)操作②是否可改为加硝酸钡溶液?为什么? 。
(2)操作③的目的是_____________,为什么不先过滤后加碳酸钠溶液?理由是_________________
(三)某水样中要检验出H+ 、SO42-、Cl- 离子,三位学生进行了如下不同的实验:
甲同学:取少量溶液先滴加石蕊溶液,再加入稍过量BaCl2溶液,充分振荡后静置,取上层清液加入AgNO3溶液。
乙同学:取少量溶液先加入稍过量Ba(NO3)2溶液,充分振荡后静置,取上层清液加入AgNO3溶液,再加入少量NaHCO3粉末。
(1)评价二位同学实验的合理性。甲_________ 乙___________(填“合理”或“不合理”)。如不合理,请说明原因____________________(如合理,此空不填)
(2)甲同学所加的BaCl2溶液应该是稍过量的, 判断该试剂过量的方法是: 。
已知某“84消毒液”瓶体部分标签如图所示,该“84消毒液”通常稀释100倍(体积之比)后使用。请回答下列问题:
(1)该“84消毒液”的物质的量浓度约为 (保留两位有效数字)
(2)该同学参阅该“84消毒液”的配方,欲用NaClO固体配制480mL含NaClO质量分数为25%的消毒液(必须用到容量瓶)。下列说法正确的是 (填序号)。
A.如图所示的仪器中,有三种是不需要的,还需要一种玻璃仪器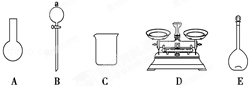
B.容量瓶用蒸馏水洗净后,应烘干后才能用于溶液配制
C.配制过程中,未用蒸馏水洗涤烧杯和玻璃棒可能导致结果偏低
D.需要称量NaClO固体的质量为143.0g
(3)若实验遇下列情况,则所配溶液的物质的量浓度是:A、偏高B、偏低C、不变(用符号回答)
Ⅰ.定容时俯视刻度线 ;
Ⅱ.定容时水多用胶头滴管吸出 。
(4) “84消毒液”与稀硫酸混合使用可增强消毒能力,某消毒小组人员用98%(密度为1.84g•cm﹣3)的浓硫酸配制2 000mL 2.3mol•L﹣1的稀硫酸用于增强“84消毒液”的消毒能力。
①所配制的稀硫酸中,H+的物质的量浓度为 mol•L﹣1;
②需用浓硫酸的体积为 mL。
有一固体粉末,其中可能含有Na2CO3、NaCl、Na2SO4、CuCl2、Ba(NO3)2、K2CO3、K2SO4中的一种或几种,现按下列步骤进行实验。
(1)将该粉末溶于水得无色溶液和白色沉淀。
(2)在滤出的沉淀中加入过量稀硝酸,有部分沉淀溶解,同时产生无色气体。
(3)取滤液做焰色反应,火焰呈黄色,透过蓝色钴玻璃观察没有明显现象。
由上述现象推断:
该混合物中一定含有 ;一定不含有 ;可能含有 ,如要检验其是否存在,应如何操作(写明操作步骤及实验结论) 。