写出下列反应的化学方程式,并注明反应类型:
(1)乙烷和氯气反应产生一氯乙烷:
(2)乙烯和溴水的反应:
(3)丙烷燃烧:
某同学想探究硫和碳原子的得电子能力的强弱,通过比较它们最高价氧化物对应水化物的酸性强弱来验证,设计了如图实验,请回答: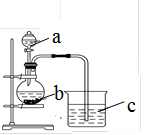
(1)仪器a的名称是,
应盛放下列药品中的(填序号)。
A.稀硫酸 B. 亚硫酸 C. 氢硫酸 D. 盐酸
(2)仪器b应盛放下列药品中的(填序号)。
A.碳酸钙 B. 硫酸钠 C. 氯化钠 D. 碳酸钠
(3)b中反应的离子方程式为。
若看到仪器C中的现象是,即可证明 比酸性强(填化学式),得电子的能力比强。
(1)下列五种物质中①Ar、②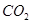 、③
、③ 、④NaOH、⑤
、④NaOH、⑤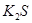 ,只存在共价键的是(填序号,下同),只存在离子键的是,既存在离子键又存在共价键的是,不存在化学键的是。
,只存在共价键的是(填序号,下同),只存在离子键的是,既存在离子键又存在共价键的是,不存在化学键的是。
(2)在以下过程中:①碘的升华、②烧碱熔化、③氯化铵受热分解、④石英熔化、⑤氯化钠溶于水、⑥氯化氢溶于水、⑦氧化钠溶于水、⑧碘溶于四氯化碳,未发生化学键破坏的是
(填序号,下同),仅发生离子键破坏的是,仅发生共价键破坏的是,既发生离子键破坏、又发生共价键破坏的是。
A、B、C、C、E是含有一种相同元素的五种物质,可发生如下转化关系:其中A是一种淡黄色粉末固体单质;B是气态氢化物;C、D是氧化物;E是该元素最高价氧化物对应的水化物。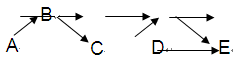
(1)元素A在元素周期表中的位置为。
(2)B的名称是。
(3)写出C的一种用途;
C的水溶液在空气中放置一段时间后溶液的pH减少,试说明其原因
。
(4)D溶于水发生反应的离子方程式。
(5)E的浓溶液与碳单质反应的化学方程式。
下表为元素周期表的一部分,请参照元素①-⑧在表中的位置,用化学用语回答下列问题:
(1)④的最简单氢化物的电子式为,结构式。
(2)③、⑦、⑧的最高价含氧对应的水化物的酸性最强的是(填化学式)。
(3)④、⑥、⑦的原子半径由小到大的顺序为。
(4)由①、②、③、④四种元素可形成多种既含有离子键又含有共价键的化合物,写出其中一种化合物的化学式。
(5)元素③和元素⑧的氢化物极易溶于水,用两根玻璃棒分别蘸取它们的浓溶液,互相靠近时,可看到大量的白烟,写出产生该现象的化学方程式是。
(6)用电子式表示②的最高价氧化物的形成过程:。(7)研究表明:②的最高价氧化物在一定条件下可被还原为晶莹透明的晶体X,其结构中原子的排列为正四面体,请写出X及其同素异形体的名称、。