磷是地壳中含量较为丰富的非金属元素,主要以难溶于水的磷酸盐如等形式存在。它的单质和化合物在工农业生产中有着重要的应用。
(1)白磷()可由、焦炭和在一定条件下反应获得。相关热化学方程式如下:
则 =。
(2)白磷中毒后可用溶液解毒,解毒原理可用下列化学方程式表示:
60能氧化白磷的物质的量是。
(3)磷的重要化合物、和可通过与溶液反应获得,含磷各物种的分布分数(平衡时某物种的浓度占各物种浓度之和的分数)与的关系如图所示。

①为获得尽可能纯的,应控制在;=8时,溶液中主要含磷物种浓度大小关系为。
②溶液显碱性,若向溶液中加入足量的溶液,溶液则显酸性,其原因是(用离子方程式表示)。
(4)磷的化合物三氯氧磷( )与季戊四醇(
)与季戊四醇( )以物质的量之比2:1 反应时,可获得一种新型阻燃剂中间体,并释放出一种酸性气体。季戊四醇与 的核磁共振氢谱如下图所示。
)以物质的量之比2:1 反应时,可获得一种新型阻燃剂中间体,并释放出一种酸性气体。季戊四醇与 的核磁共振氢谱如下图所示。

①酸性气体是(填化学式)。
②的结构简式为
已知A是来自石油的重要有机化工原料,E是具果香味的有机物,F是一种高聚物,可制成多种包装材料。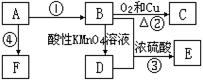
(1)A的最简式为:____________,C的名称:_____________,F的结构简式:____________________________________。
(2)D分子中的官能团名称是_________________,请设计一种实验来验证D物质存在该官能团的方法是_________________________________________。
(3)写出下列反应的化学方程式并指出反应类型:③____________________________,反应类型_____________。
新合成的一种烃,其碳架呈正三棱柱(如图所示)
(1)写出该烃的分子式_____________________________。
(2)该烃的一氯代物是否有同分异构体?_______。(填“是”或“否”)
(3)该烃的二氯取代物有_________________种。
(4)该烃的同分异构体有多种,其中一种不能使酸性高锰酸钾溶液或Br2的CCl4溶液褪色,但在一定条件下能跟溴发生取代反应,和H2能发生加成反应,这种同分异构体的结构简式是_______________________________。
短周期元素的单质X、Y、Z在通常状况下均为气态,并有右图转化关系(反应条件略去),已知: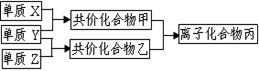
a.常见双原子单质分子中,X分子含共价键最多。
b.甲分子中含10个电子,乙分子含有18个电子。
(1)X的电子式是_______________________。
(2)实验室可用下图所示装置(缺少收集装置,夹持固定装置略去)制备并收集甲。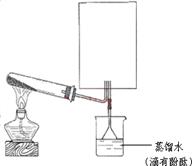
①在图中方框内绘出收集甲的仪器装置简图。
②试管中的试剂是____________________。(填写化学式)
③烧杯中溶液由无色变为红色,其原因是(用电离方程式表示)_________________________。 (3)磷在Z中燃烧可生成两种产物,其中一种产物丁分子中各原子最外层不全是8电子结构,丁的化学式是__________。
(3)磷在Z中燃烧可生成两种产物,其中一种产物丁分子中各原子最外层不全是8电子结构,丁的化学式是__________。
某高分子材料的结构如右图,则其对应的单体的结构简式为:______________________,______________________。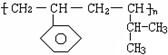
组成一种原电池如图所示。试回答下列问题(灯泡功率合适):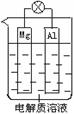
(1)电解质溶液为稀H2SO4时,灯泡______(填“亮”做①题,填“不亮”做②题) 。
。
①若灯泡亮,则Mg电极上发生的反应为:____________________;
Al电极上发生的反应为:___________________________________。
②若灯泡不亮,其理由为:__________________________________。
(2)电解质溶液为NaOH溶液时,灯泡_____(填“亮”做①题,填“不亮”做②题)。
①若灯泡亮,则Al电极上发生的反应为:_____________________________。
②若灯泡不亮,其理由为:__________________________________________。