现用质量分数为98%、密度为1.84g•cm-3的浓H2SO4来配制500mL、0.2mol•L-1的稀H2S04。可供选择的仪器有:①玻璃棒②烧瓶③烧杯④胶头滴管⑤量筒⑥容量瓶⑦托盘天平⑧药匙。请回答下列问题:
(1)上述仪器中,在配制稀H2S04时用不到的有_________ (填代号)。
(2)经计算,需浓H2S04的体积为______。现有①10mL②50mL③100mL三种 规格的量筒,你选用的量筒是______ (填代号)。
(3)将浓H2S04加适量蒸馏水稀释后,冷却片刻,随后全部转移到_______mL的容量瓶中,转移时应用玻璃棒_________ 。转移完毕,用少量蒸馏水洗涤____________ 2—3次,并将洗涤液全部转移到容量瓶中,再加适量蒸馏水,振荡容量瓶,使溶液混合均匀。然后缓缓地把蒸馏水直接注入容量瓶直到液面接近刻度________ 处。改用______________ 加蒸馏水到瓶颈刻度的地方,使溶液的________________________________________ 。 振荡、摇匀后,装瓶、贴签。
(4)在配制过程中,其他操作都准确,下列操作中错误的是______ (填代号,下同) ,能引起误差偏高的有_________。
①洗涤量取浓H2S04后的量筒,并将洗涤液转移到容量瓶中
②未等稀释后的H2S04溶液冷却至室温就转移到容量瓶中
③将浓H2S04直接倒人烧杯,再向烧杯中注入蒸馏水来稀释浓H2S04
④定容时,加蒸馏水超过标线,又用胶头滴管吸出
⑤转移前,容量瓶中含有少量蒸馏水
⑥定容摇匀后,发现液面低于标线,又用胶头滴管加蒸馏水至标线
⑦定容时,俯视标线
为了证明铜与稀硝酸反应产生NO,某校学生实验小组设计了一个实验,其装置如图所示(加热装置和固定装置均已略去),B为一个用金属丝固定的干燥管,内装块状碳酸钙固体;E为一个空的蒸馏烧瓶;F是用于鼓入空气的双连打气球。
(1) 实验时,先将B装置下移,使碳酸钙与稀硝酸接触产生气体,当C处产生白色沉淀时,立刻将B装置上提,使之与稀硝酸分离。该组学生设计此步操作的目的为。
(2)将A中铜丝放入稀硝酸中,给装置A微微加热,在装置A中产生无色气体,其反应的化学方程式为。
(3)装置E中开始时出现浅红棕色气体,用F向E中鼓入空气后,可观察到烧瓶E内气体颜色加深,产生上述现象的原因是。
(4)一段时间后,C中白色沉淀溶解,其原因是__________________________。
(5)装置D的作用是____________________________________________。
利用甲烷与氯气发生取代反应制取副产品盐酸的设想在工业上已成为现实。某化学兴趣小组通过在实验室中模拟上述过程,其设计的模拟装置如下: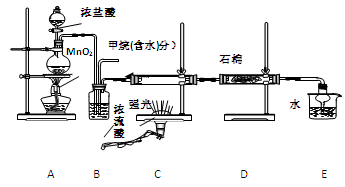
(1) B装置有三种功能:①控制气流速度;②均匀混合气体;③
|
(2) 设V(Cl2)/V(CH4)=x,若理论上欲取代反应获得最多的氯化氢则x≥
(3) D装置的石棉中均匀混有KI粉末其作用是 。实验室用下图所示装置来制取乙酸乙酯,回答下列问题: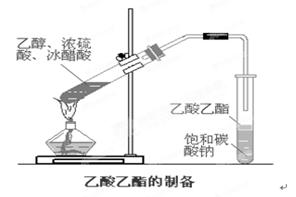
(1)请写出本实验中发生的主要反应方程式。
(2)配置混合溶液时,加入试剂的正确顺序是(填“A”或“B”)。
A.先加乙醇,再慢慢注入浓硫酸和乙酸 B.先加浓硫酸,再慢慢注入乙醇和乙酸
(3)浓硫酸的作用是。
(4)饱和Na2CO3溶液的作用是。
(5)实验完成后,右边试管液面上有透明的不溶于水的油状液体生成。若要分离10mL该液体混合物需要用到的主要玻璃仪器是,这种分离方法叫做。
对于H2O2分解反应,Cu2+也有一定的催化作用。为比较Fe3+和Cu2+对H2O2分解的催化效果,某化学研究小组的同学分别设计了如图甲、乙所示的实验。请回答相关问题: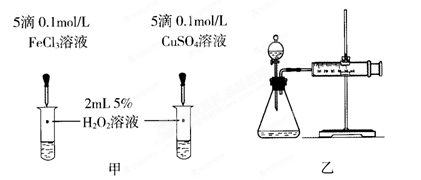
①定性分析:如图甲可通过观察_________________________,定性比较得出结论。有同学提出将FeCl3改为Fe2(SO4)3更为合理,其理由是_________________________。
②定量分析:用图乙所示装置做对照实验,实验时均以生成40 mL气体为准,其他可能影响实验的因素均已忽略。实验中需要测量的数据是________________________。
为了研究外界条件对过氧化氢分解速率的影响,某同学做了以下实验,请回答下列问题。
| 编号 |
操作 |
实验现象 |
| ① |
分别在试管A、B中加入5 mL 5% H2O2溶液,各滴入2滴1mol/L FeCl3溶液。待试管中均有适量气泡出现时,将试管A放入盛有5℃左右冷水的烧杯中浸泡;将试管B放入盛有40℃左右热水的烧杯中浸泡。 |
试管A中不再产生气泡; 试管B中产生的气泡量增大。 |
| ② |
另取两支试管分别加入5 mL 5% H2O2溶液和5 mL 10% H2O2溶液 |
试管A、B中均未明显见到有气泡产生。 |
(1)过氧化氢分解的化学方程式为_____________________________________。
(2)实验①的目的是_________________________________________________。
实验中滴加FeCl3溶液的目的是_______________________________________。
(3)实验②未观察到预期的实验现象,为了帮助该同学达到实验目的,你提出的对上述操作的改进意见是_______________________(用实验中所提供的几种试剂)。
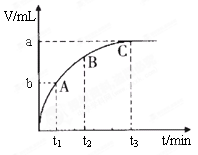
(4)某同学在50 mL一定浓度的H2O2溶液中加入一定量的二氧化锰,放出气体的体积(标准状况下)与反应时间的关系如下图所示,则A、B、C三点所表示的瞬时反应速率最慢的是______。