由短周期元素组成的单质A、B、C和甲、乙、丙、丁四种化合物有下图所示的转化关系,已知C为密度最小的气体。
根据图示转化关系回答:
(1)写出下列物质的化学式:B 、丙 、丁 。
(2)组成单质A的元素在周期表中的位置是 。
(3)乙与过量CO2反应的离子反应方程式____________________________
(4)A与NaOH溶液反应的化学反应方程式____________________________
(10分)短周期元素A、B、C、D中,0.5mol A元素的离子得到6.02×1023个电子被还原为中性原子,0.4g A的氧化物恰好与100ml 0.2mol/L的盐酸完全反应,A原子核内质子数目与中子数目相等,B元素原子核外第三层电子数目比第一层多1个,C—比A元素的离子多1个电子层,D元素的原子核外第二层比第一层多2个电子。回答下列问题:
(1)C―的结构示意图为;
与C同族的上一周期元素的气态氢化物的稳定性比HC的________(填“强”或“弱”);
与C同族的上一周期元素的气态氢化物的沸点比HC的________(填“高”或“低”);
(2)元素D的最高价氧化物的电子式为_______,D的气态氢化物的二氯代物有_____种结构。
(3)工业上冶炼单质A的化学方程式为_____________________________________;
(4)若将单质A、B用导线连接插入到氢氧化钠溶液中可以组成原电池,则正极材料是_______(用化学式填写),负极电极反应是___________________________________。
已知:
I.冠心平F是降血脂、降胆固醇的药物,它的一条合成路线如下:
(1)A为饱和一元羧酸,8.8g A与足量NaHCO3溶液反应生成2.24L CO2(标准状况),A的分子式为___________________。
(2)写出符合A分子式的所有甲酸酯的结构简式: ______________________________。
(3)B是氯代羧酸,其核磁共振氢谱有两个峰,写出B→C的反应方程式:
__________________________________________________________。
(4)C+E→F的反应类型为________________________。
(5)写出A和F的结构简式:A______________________; F__________________________。
(6)D的苯环上有两种氢,它所含官能团的名称为___________________;写出a、b所代表的试剂:a ______________; b___________。
Ⅱ. 按如下路线,由C可合成高聚物H:
(7)C G的反应类型为_____________________.
G的反应类型为_____________________.
(8)写出G H的反应方程式:_______________________。
H的反应方程式:_______________________。
实验室用加热l-丁醇、溴化钠和浓H2SO4的混合物的方法来制备1-溴丁烷时,还会有烯、醚等副产物生成。反应结束后将反应混合物蒸馏,分离得到1—溴丁烷,已知相关有机物的性质如下: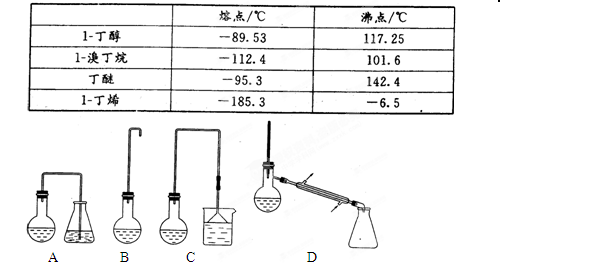 ⑴反应中由于发生副反应而生成副产物的有机反应类型有_________________。
⑴反应中由于发生副反应而生成副产物的有机反应类型有_________________。
⑵制备1-溴丁烷的装置应选用上图中的_______(填序号)。反应加热时的温度不宜超过100℃,理由是__________________________;较好的加热方法是_____________。
⑶当给烧瓶中的混合物加热时,溶液会出现橘红色,其原因是_____________。
⑷反应结束后,将反应混合物中1-溴丁烷分离出来,应选用上图的装置是______。该操作应控制的温度(t)范围是_______________。
(14分) CO2、SO2、NOx是对环境影响较大的气体,控制和治理CO2、SO2、NOx是解决温室效应、减少酸雨和光化学烟雾的有效途径。
(1)下列措施中,有利于降低大气中的CO2、SO2、NOx浓度的是(填序号)
| A.减少化石燃料的使用,开发新能源 |
| B.使用无氟冰箱,减少氟利昂排放 |
| C.多步行或乘公交车,少用私家车 |
| D.将工业废气用碱液吸收后再排放 |
(2)有学者设想以右图所示装置用电化学原理将CO2、SO2转化为重要化工原料。
①若A为CO2,B为H2,C为CH3OH,则正极的电极反应式为;
②若A为SO2,B为O2,C为H2SO4,则负极的电极反应式为;
当电路中有1 mol e-流过,正极区溶液中的H+的物质的量的变化量 n(H+)=mol。
n(H+)=mol。
(3)在研究氮的氧化物的转化时,某小组查阅到以下数据:l7℃、l.01×l05Pa时,2NO2(g) N2O4(g)△H<0的平衡常数K=13.3。
N2O4(g)△H<0的平衡常数K=13.3。
①若该条件下密闭容器中N2O4和NO2的混合气体达到平衡时,c(NO2)=0.0300mol.L-1,
则c(N2O4)=。(保留两位有效数字)
②若改变上述体系的某一个条件,达到新的平衡后,测得混合气体中c(NO2)="0.04" mol.L-1,c(N2O4)="0.007" mol.L-1,则改变的条件为 。
(4)为了降低汽车尾气对大气的污染,有关部门拟用甲醇替代作为公交车的燃料。由CO和H2合成甲醇的方法是CO(g)+2H2(g) CH3OH(g),己知该反应在300OC时的化学平衡常数为0.27,该温度下将2moI CO、3mol H2利2molCH3OH(g)充入容积为2 L的密闭容器中,此时反应将。(填“向正反应方向进行”、“向逆反应方向进行”或“处于平衡状态”)。
CH3OH(g),己知该反应在300OC时的化学平衡常数为0.27,该温度下将2moI CO、3mol H2利2molCH3OH(g)充入容积为2 L的密闭容器中,此时反应将。(填“向正反应方向进行”、“向逆反应方向进行”或“处于平衡状态”)。
已知A的产量通常用来衡量一个国家的石油化工水平,现以A为主要
原料合成一种具有果香味的物质E,其合成路线如下图所示。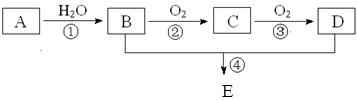
已知:醛可氧化生成羧酸。回答下列问题:
(1)写出下列物质的结构简式:ADE
(2)写出下列反应的化学方程式,并注明反应类型:
①、
②、