X、Y、Z、W是元素周期表中原子序数依次增大的四种短周期元素,其相关信息如下表:
| 元素 |
相关信息 |
| X |
X的最高价氧化物对应的水化物化学式为H2XO3 |
| Y |
Y是地壳中含量最高的元素 |
| Z |
Z的基态原子最外层电子排布式为3s23p1 |
| W |
W的一种核素的质量数为28,中子数为14 |
(1)W位于元素周期表第 周期第 族;W的原子半径比X的
(填“大”或“小”)。
(2)Z的第一电离能比W的 (填“大”或“小”); XY2由固态变为气态所需克服的微粒间作用力是 ;氢元素、X、Y的原子可共同形成多种分子,写出其中一种能形成同种分子间氢键的物质名称 。
(3)振荡下,向Z单质与盐酸反应后的无色溶液中滴加NaOH溶液直至过量,能观察到的现象是 ;W的单质与氢氟酸反应生成两种无色气体,该反应的化学方程式是 。
(4)在25°、101kpa下,已知13.5g的Z固体单质在Y2气体中完全燃烧后恢复至原状态,放热419kJ,该反应的热化学方程式是 。
(5)工业上冶炼Z时用到的催化剂是冰晶石,制取冰晶石(Na3AlF6)的化学方程式如下: 2Al(OH)3+ 12HF+ 3 A = 2Na3AlF6+ 3CO2↑+ 9H2O
根据题意完成下列填空:
①反应物A的化学式为 ,属于 晶体
②冰晶石(Na3AlF6)是离子化合物,由两种微粒构成,冰晶石晶胞结构如下图所示, 位于大立方体顶点和面心,
位于大立方体顶点和面心,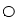 位于大立方体的12条棱的中点和8个小立方体的体心,那么大立方体的体心处▽所代表的微粒是 (填具体的微粒符号)
位于大立方体的12条棱的中点和8个小立方体的体心,那么大立方体的体心处▽所代表的微粒是 (填具体的微粒符号)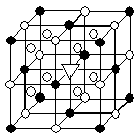
(1)已知: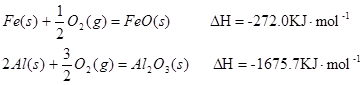
Al和FeO发生铝热反应的热化学方程式是。
(2)某可逆反应在不同条件下的反应历程分别为A、B,如图所示。
①据图判断该反应是(填“吸”或“放”)热反应,当反应达到平衡后,其他条件不变,升高温度,反应物的转化率(填“增大”、“减小”或“不变”);
②其中B历程表明此反应采用的条件为(选填序号)。
A.升高温度 B.增大反应物的浓度
C.降低温度 D.使用催化剂
(3)1000℃时,硫酸钠与氢气发生下列反应: 该反应的平衡常数表达式为。
该反应的平衡常数表达式为。
(4)常温下,如果取0.1mol·L-1HA溶液与0.1mol·L-1NaOH溶液等体积混合(混合后溶液体积的变化忽略不计),测得混合液的pH=8。
①混合液中由水电离出的OH-浓度与0.1mol·L-1NaOH溶液中由水电离出的OH-浓度之比为;
②已知NH4A溶液为中性,又知将HA溶液加到Na2CO3溶液中有气体放出,试推断(NH4)2CO3溶液的pH7(填“<”、“>”或“=”)。
如图所示3套实验装置,分别回答下列问题。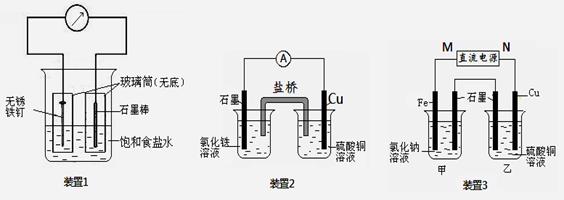
(1)装置1为铁的吸氧腐蚀实验。一段时间后, 向插入碳棒的玻璃筒内滴入酚酞溶液,可观察到碳棒附近的溶液变红,该电极反应为 。
(2)装置2中的石墨是 极(填“正”或“负” ),该装置发生的总反应的离子方程式为 。
(3)装置3中甲烧杯盛放200 mL 0.2 mol/L的NaCl溶液,乙烧杯盛放200 mL 1.0 mol/L的CuSO4溶液。反应一段时间后,停止通电。向甲烧杯中滴入几滴酚酞溶液,观察到石墨电极附近首先变红。
|
① 电源的M端为 极,甲烧杯中铁电极的电极反应为 ②停止电解,取出Cu电极,洗涤、干燥、称量、电极增重 1.28 g,甲烧杯中产生的气体标准状况下体积为 mL 。
一定条件下,在体积为3L的密闭容器中,一氧化碳与氢气反应生成甲醇(催化剂为Cu2O/ZnO):CO(g)+ 2H2(g) CH3OH(g)
CH3OH(g)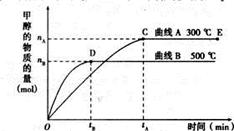
根据题意完成下列各题:
(1)5000C,从反应开始到平衡,甲醇的平均反应速率v(CH3OH)=(用nB、 tB 表示)
(2)在其他条件不变的情况下,将处于E点的体系的体积压缩到原来的1/2,下列有关该体系的说法正确的是
a .氢气的浓度减少 b.正反应速率加快,逆反应速率也加快
c.甲醇的物质的量增加 d.重新平衡时n(H2)/n(CH3OH)增大
(3)可逆反应:CO(g)+ 2H2(g) CH3OH(g) 在恒容密闭容器中反应,达到平衡状态的标志是:
CH3OH(g) 在恒容密闭容器中反应,达到平衡状态的标志是:
①单位时间内生成2n molH2的同时生成n mol CH3OH
②单位时间内生成2n molH2的同时,生成n mol CO
③用CO、H2、CH3OH 的物质的量浓度变化表示的反应速率的比为1 : 2 : 1的状态
④混 合气体的密度不再改变的状态
⑤ 混合气体的平均相对分子质量不再改变的状态
(4)改变下列哪些条件能增大甲醇的产量()
| A.增大容器体积 | B.增大压强 | C.升高温度 | D.加催化剂 |
(5)反应达到平衡后再升高温度,K值(填“增大”“减小”或“不变”)。
(6)据研究,反应过程中起催化作用的为Cu2O,反应体系中含少量CO2有利于维持催化剂Cu2O的量不变,原因是:(用化学方程式表示)。
工业上常利用反应 3Cl2+8NH3 =6NH4Cl+N2 检查氯气管道是否漏气。回答下列问题:
(1)该反应中,氧化剂是,发生氧化反应的物质是。
(2)该反应中氧化剂与还原剂的物质的量之比为。
(3)若标准状况下有6.72L N2生成,则转移电子的物质的量为mol。
亚铁盐不稳定,在空气中易被氧化,因此在存放FeSO4溶液时,常加入 ,其理由是(用离子方程式表示)。