已知某无色溶液中可能含有Na+、Ba2+、Fe3+、MnO4—、SO32—、Cl—、HCO3— 中的几种,依次进行以下实验,观察到的现象如下:①用PH试纸检验,溶液的PH>7;
②向溶液中滴加氯水,没有气体产生,得到无色溶液;
③向②的溶液中滴加硝酸酸化硝酸银溶液,产生白色沉淀;
④向②的溶液中滴加BaCl2溶液,产生不溶于盐酸的白色沉淀。
则(1)原溶液中一定含有的阴离子是 ;肯定没有的阳离子是 。
(2)步骤②的离子反应方程式为 。
(3)能否确定含有阳离子 ,(若有,写出离子符号,没有则写没有),其理由是 。
A、B、C均为短周期元素,可形成A2C和BC2两种化合物。A、B、C的原子序数依次递增,A原子的K层的电子数目只有一个,B位于A的下一周期,它的最外能层电子数比K层多2个,而C原子核外的最外能层电子数比次外层电子数少2个。
(1)它们的元素符号分别为:A;B;C;
(2)BC2是由键组成的(填“极性”或“非极性”)分子。
(3)画出C原子的核外电子排布图。
(4)A2C和BC2的空间构形分别是和。
二氧化硅晶体是立体的网状结构。其晶体模型如图所示。认真观察晶体模型并回答下列问题: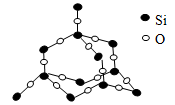

(1)二氧化硅晶体中最小的环为元环。
(2)每个硅原子为个最小环共有。
(3)每个最小环平均拥有个氧原子。
FeBr2是一种黄绿色鳞片状的固体,某研究性学习小组为了探究它的还原性,进行了如下实验:
1.实验需要90mL 0.1mol/L FeBr2溶液
(1)配制FeBr2溶液除烧杯、量筒、胶头滴管外还需的玻璃仪器是、
(2)下列有关配制过程中说法错误的是(填序号)。
A用电子天平称量质量为1.944g的FeBr2.
B将称量的FeBr2放入容量瓶中,加90mL蒸馏水溶解
C洗涤溶解FeBr2的烧杯,并将洗涤液转移至容量瓶中
D.容量瓶贴签存放配好的FeBr2溶液
E.定容时,仰视容量瓶刻度线会使配制的FeBr2溶液浓度偏高
II. 探究FeBr2的还原性
取10mL上述FeBr2溶液,向其中滴加少量新制的氯水,振荡后溶液呈黄色。某同学对产生黄色的原因提出了假设:
假设1:Br-被Cl2氧化成Br2溶解在溶液中;假设2:Fe2+被Cl2氧化成Fe3+。
(1)请你完成下表,验证假设:
| 实验步骤、预期现象 |
结论 |
| ①溶液中加入适量四氯化碳, |
假设1正确 |
| ②向溶液中加入 |
假设2正确 |
若假设1正确,从实验①中分离出Br2的实验操作名称是 ____________;
(2)实验证明:还原性Fe2+> Br-,请用一个离子方程式来证明: _________________;
(3)若在50mL上述FeBr2溶液中通入5×10-3molCl2,反应的离子方程式为。
某实验小组同学为了探究铜与浓硫酸的反应,进行了如下系列实验。
[实验1]铜与浓硫酸反应,实验装置如图所示。
实验步骤:
①先连接好装置,检验气密性,加入试剂;
②加热A试管直到B中品红褪色,熄灭酒精灯;
③将Cu丝上提离开液面。
(1)装置A中发生反应的化学方程式为。
(2)熄灭酒精灯后,因为有导管D的存在,B中的液体不会倒吸,其原因是。
(3)拆除装置前,不需打开胶塞,就可使装置中残留气体完全被吸收,应当采取的操作是。
[实验2]实验中发现试管内除了产生白色固体外,在铜丝表面还产生黑色固体甲,其中可能含有氧化铜、硫化铜、硫化亚铜,以及被掩蔽的氧化亚铜。
查阅资料:①氧化亚铜在酸性环境下会发生自身氧化还原反应生成Cu2+和铜单质,在氧气流中煅烧,可以转化为氧化铜。②硫化铜和硫化亚铜常温下都不溶于稀盐酸,在氧气流中煅烧,硫化铜和硫化亚铜都转化为氧化铜和二氧化硫。
为了研究甲的成分,该小组同学在收集到足够量的固体甲后,进行了如图的实验: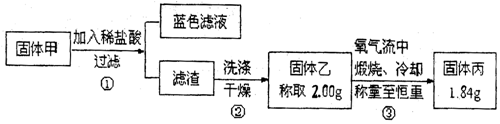
(4)②中检验滤渣是否洗涤干净的实验方法是
(5)③中在煅烧过程中一定发生的反应的化学方程式为。
某待测溶液(阳离子为Na+)中可能含有SO42-、SO32-、NO3-、Cl-、Br-、CO32+、HCO3-中的一种或多种,进行如图所示的实验,每次实验所加试剂均过量,回答以下问题:
(1)待测液中是否含有SO42-、SO32-:。
(2)沉淀B的化学式为;生成沉淀B的离子方程式为。
(3)根据以上实验,待测液中肯定没有的离子是;
肯定存在的离子还有。