多昔芬主要用于防治骨质疏松等病症,其合成路线如下:
说明:D+G→H的转化中分别发生了加成反应和水解反应。
(1)D中含氧官能团的名称是 。
(2)C→D的反应类型是 ,H→多昔芬的反应类型是 。
(3)E→F转化中另一产物是HBr,则试剂X的结构简式是 。
(4)H分子中有 个手性碳原子。
(5)写出同时满足下列条件的A物质同分异构体的结构简式 。
①能发生银镜反应;②与FeCl3发生显色反应;③苯环上的一溴代物只有2种。
(6)苯甲酰氯(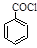 )是合成药品的重要中间体。请写出以苯、乙醚、甲醛为原料制备苯甲酰氯的合成路线流程图(无机试剂任用)。合成路线流程图示例如下:
)是合成药品的重要中间体。请写出以苯、乙醚、甲醛为原料制备苯甲酰氯的合成路线流程图(无机试剂任用)。合成路线流程图示例如下: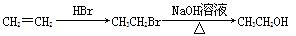
向硫酸亚铁溶液中滴加氢氧化钠溶液,实验的现象是:有色沉淀产生,迅速变为色,最后变为色。有关的化学方程式为:
1)2)
1、已知X、Y、Z、W为四种短周期主族元素,它们的原子序数依次增大,其中X、Y、W位于不同周期,Y是形成化合物种类最多的元素,Z可形成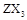 型化合物,常温下W的单质为气态。
型化合物,常温下W的单质为气态。
(1)由X、Y组成的最简单化合物可作为某燃料电池的极反应物。
(2)化合物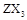 所含化学键种类为,属于化合物(填“离子”或“共价”)。
所含化学键种类为,属于化合物(填“离子”或“共价”)。
(3)写出实验室制备W单质的化学方程式为。
Ⅱ、铁及其化合物在生活、生产中有广泛应用。请回答下列问题:
(1)黄铁矿(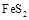 )是生产硫酸和冶炼钢铁的重要原料。其中一个反应为
)是生产硫酸和冶炼钢铁的重要原料。其中一个反应为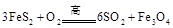 ,有3mol
,有3mol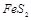 参加反应,转移mol电子。
参加反应,转移mol电子。
(2)氯化铁溶液常用作印刷电路铜板腐蚀剂,反应的离子方程式为
;从腐蚀废液回收得到金属铜,还需要的试剂是。
(3)与明矾相似,硫酸铁也可用作净水剂,其原理是
(4)钢铁的电化腐蚀简单示意图如下,将该图稍作修改即可成为钢铁电化学防护的简单示意图,请在下图虚线框内作出修改,并用箭头标出电子流动方向。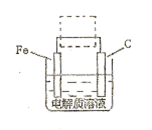
Ⅰ某化学过程的示意图如图所示。在装置工作过程中,甲池的总反应式为: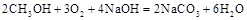 。试回答下列问题:
。试回答下列问题: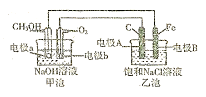
(1)甲池溶液中的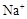 移向(填“a”或“b”)电极,
移向(填“a”或“b”)电极,
乙池溶液中的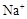 移向(填“ A”或“B”)电极;
移向(填“ A”或“B”)电极;
(2)电极a上发生的电极反应式为;
(3)乙池中发生反应的离子方程式为;
(4)当电极A处得到0.71g产物时,甲池中理论上消耗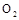
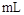 (标准状况下)。如何检验A处的产物。
(标准状况下)。如何检验A处的产物。
Ⅱ某研究性学习小组对铝热反应实验展开研究。现行高中化学教材对“铝热反应”的现象有这样的描述:“反应放出大量的热,并发出耀眼的光芒”、“纸漏斗的下部被烧穿,有熔融物落入沙中”。查阅《化学手册》知,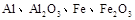 熔点、沸点数据如下:
熔点、沸点数据如下:
| 物质 |
Al |
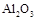 |
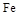 |
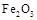 |
| 熔点/℃ |
660 |
2054 |
1535 |
1462 |
| 沸点/℃ |
2467 |
2980 |
2750 |
- |
某同学推测,铝热反应所得到的熔融物应是铁铝合金。理由是:该反应放出的热量使铁熔化,铝的熔点比铁低,此时液态的铁和铝熔合形成铁铝合金。你认为他的解释是否合理(填“合理”或“不合理”)
用一个简单的实验方案,证明上述所得的块状熔融物中含有金属铝。该实验所用试剂,反应的离子方程式为。
实验室溶解该熔融物,下列试剂中最适宜的试剂是
A.浓硫酸 B.稀硫酸 C.稀硝酸 D. 氢氧化钠溶液
“低碳循环”已经引起了国民的重视,试回答下列问题:
(1)煤的气化和液化可以提高燃料的利用率。
已知25℃,101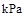 时:
时: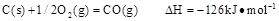
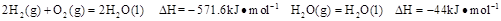
则在25℃,101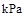 时:
时: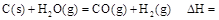 .
.
(2)高炉炼铁是CO气体的重要用途之一,其基本反应为: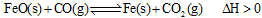 ,已知在1100℃时,该反应的化学平衡常数K=0.263。
,已知在1100℃时,该反应的化学平衡常数K=0.263。
①温度升高,化学平衡移动后达到新的平衡,此时平衡常数K值(填“增大”、“减小”或“不变”);
②1100℃时测得高炉时,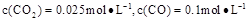 ,在这种情况下,该反应是否处于化学平衡状态?(填“是”或“否”),其判断依据是。
,在这种情况下,该反应是否处于化学平衡状态?(填“是”或“否”),其判断依据是。
③目前工业上可用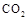 来生产燃料甲醇,有关反应为:
来生产燃料甲醇,有关反应为: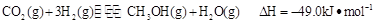 。现向体积为1L的密闭容器中,充入1mol
。现向体积为1L的密闭容器中,充入1mol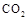 和3mol
和3mol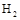 ,反应过程中测得
,反应过程中测得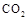 和
和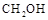 (g)的浓度随时间的变化如图所示。
(g)的浓度随时间的变化如图所示。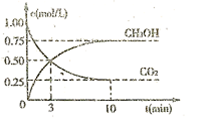
①从反应开始到平衡,氢气的平均反应速率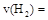 ;
;
②下列措施能使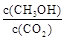 增大的是(填符号)。
增大的是(填符号)。
| A.升高温度 |
B.再充入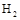 |
C.再充入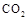 |
D.将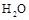 (g)从体系中分离 (g)从体系中分离 |
E.充入He(g),使体系压强增大
某强酸性溶液X含有Ba2+、Al3+、NH4+、Fe2+、Fe3+、CO32-、SO32-、SO42-、NO3-中的一种或几种,取该溶液进行连续实验,实验内容如下: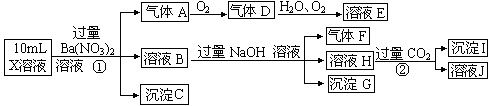
根据以上信息,回答下列问题:
(1)上述离子中,溶液X中除H+外还肯定含有的离子是____________________,不能确定是否含有的离子是___________,若要验证该离子是否存在,最可靠的化学方法是_______________________
(2)沉淀G的化学式为_____________。
(3)写出有关离子方程式:
①中生成A________________________。
②_________。