用石灰乳、石灰氮(CaCN2)和炼厂气(含H2S)反应,既能净化尾气,又能获得应用广泛的CS(NH2)2(硫脲),其部分工艺流程如下: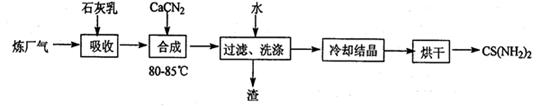
(1)高温下,H2S存在下列反应:2H2S(g)  2H2(g)+S2(g),其平衡常数表达式为K=。
2H2(g)+S2(g),其平衡常数表达式为K=。
(2)用石灰乳吸收H2S制取Ca(HS)2需要在低温下进行,其原因是 ;过滤得到的滤渣可再利用,滤渣的主要成分是 (填化学式)。
(3)合成硫脲需长时间搅拌,并在较高温度(80℃-85℃)下进行,其目的是 。
Ca(HS)2与CaCN2在水溶液中合成硫脉的化学方程式为 。
(4)化合物X与硫脲互为同分异构体,X加入FeCl3溶液中,溶液显红色,X的化学式为 。
有一包从海水中获得的粗盐,已经经过初步的提纯。课外活动小组对它的成分进行探究,并将粗盐进一步提纯。
探究一:这包粗盐中还含有什么杂质?
根据海水的成分和初步提纯的实验操作,估计该粗盐可能还含有的杂质是CaCl2和MgCl2。现用实验验证这种推测:取样并溶解,加入数滴NaOH溶液,目的是检验是否会有(填化学式,下同);接着再加入数滴Na2CO3溶液,目的是检验是否会有。实验证明这包粗盐含有的杂质是CaCl2 。
。
探究二:这包粗盐中NaCl的质量分数是多少?
按下面步骤进行实验:①称取一定质量的样品; ②将样品加水溶解,制成粗盐溶液;③向粗盐溶液中加入过量的某种试剂,过滤;④沉淀洗涤后小心烘干,得到纯净固体A;⑤溶液在进行某一操作后,移入蒸发皿蒸发,得到纯净固体B;⑥称量实验中得到的某种固体。
②将样品加水溶解,制成粗盐溶液;③向粗盐溶液中加入过量的某种试剂,过滤;④沉淀洗涤后小心烘干,得到纯净固体A;⑤溶液在进行某一操作后,移入蒸发皿蒸发,得到纯净固体B;⑥称量实验中得到的某种固体。
(1)②、③、⑤的步骤中,都使用到同一仪器(填名称),它在步骤②和⑤中的操 作方法相同,但目的不同。在步骤②中的目是,在步骤⑤中的目的是。
作方法相同,但目的不同。在步骤②中的目是,在步骤⑤中的目的是。
(2)步骤③中加入的试剂是(写化学式);步骤⑤中进行的“某一操作”是,目的是。
(3)步骤⑥中你认为需要称量的固体A 还是固体B,(填A或B),你不选择另一种固体的理由是。
还是固体B,(填A或B),你不选择另一种固体的理由是。
某校化学兴趣小组拟用浓盐酸与二氧化锰加热反应,制取并收集2瓶干燥、纯净的氯气。为防止换集气瓶时生成的氯气污染空气,设计了如下装置: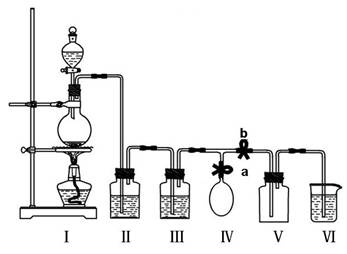
(1)写出装置Ⅰ烧瓶中发生反应的化学方程式:,写出氯原子结构示意图;
(2)装置Ⅱ中盛放的药品是饱和氯化钠溶液,其作用是;
装置Ⅲ的作用是干燥氯气,应盛放。
(3)实验开始后,先a b(填“关闭”或“打开”,下同);当集满一瓶氯气时,为减少换集气瓶时氯气的外逸,再a b,换好集气瓶后,继续收集氯气。
(4)兴趣小组的某些同学准备在烧杯中加入下列溶液中的一种来吸收残余氯气,你认为其中不恰当的(填字母)
A.氢氧化钠溶液 B.浓硫酸 C.水
写出下列反应化学方程式
1、重氢形成的盐酸和碳酸钙反应
2、漂白粉露置在空气中变质
3、电解饱和食盐水
4、次氯酸的不稳定性
5、适量的氯气与碘化钠溶液反应
(1)在标准状况下,将L NH3溶于水得到0.5 L 0.5 mol·L-1的氨水;配制100 mL 0.1mol·L-1 CuSO4溶液,需要CuSO4·5H2O于g。取出5 mL该溶液,它的物质的量浓度为,该100 mL溶液可以跟浓度为0.1 mol·L-1的NaOH溶液mL完全反应。
(2)在H、O、H+、H2、OH-、H2O六种微粒中,保持氢气化学性质的微粒是(填化学式,下同);电解水时变化的最小微粒是;水变成水蒸气时没有变化;带电的微粒是;质子数多于核外电子数的微粒是。
(3)有相同状况下的两种气体12C18O和14N2。若两种气体的质量相等,则12C18O和14N2气体所含质子数之比为;若两种气体的分子数相同,则12C18O和14N2的体积之比为。
燃烧法是测定有机化合物化学式的一种重要方法。在一定温度下取0.1 mol某气态烃A在O2中完全燃烧,生成CO2和水蒸汽,放出热量Q kJ,将生成物依次通过浓硫酸和碱石灰,浓硫酸增重7.2 g,碱石灰增重17.6 g。将烃A加入酸性KMnO4溶液或Br2的CCl4溶液,均能使它们褪色。
kJ,将生成物依次通过浓硫酸和碱石灰,浓硫酸增重7.2 g,碱石灰增重17.6 g。将烃A加入酸性KMnO4溶液或Br2的CCl4溶液,均能使它们褪色。
(1)写出烃A的分子式 ;
(2) 已知烃A分子结构高度对称且有两个甲基,请写出烃A的结构简式 ;
(3)写出烃A使Br2的CCl4溶液褪色的化学方程式 ;
(4)烃A在一定条件下可以通过加聚反应合成一种塑料,则该反应的化学方程式是 。