过氧化钙晶体[CaO2·8H2O]较稳定,呈白色,微溶于水,能溶于酸性溶液。广泛应用于环境杀菌、消毒等领域。
★过氧化钙晶体的制备
工业上生产CaO2·8H2O的主要流程如下: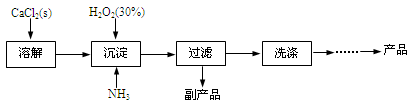
(1)用上述方法制取CaO2·8H2O的化学方程式是 。
(2)沉淀时常用冰水控制温度在10℃以下和通入过量的NH3,其可能原因分别是
① ;② 。
★过氧化钙晶体含量的测定
准确称取0.3000g产品于锥形瓶中,加入30 mL蒸馏水和10 mL 2.000 mol·L-1 H2SO4,用0.0200 mol·L—1KMnO4标准溶液滴定至终点。重复上述操作两次。H2O2和KMnO4反应的离子方程式为2MnO4-+5 H2O2+6H+ =2Mn2++5O2↑+8H2O
(3)滴定终点观察到的现象为 。
(4)根据表1数据,计算产品中CaO2·8H2O的质量分数(写出计算过程)
| 滴定次数 |
样品的质量/g |
KMnO4溶液的体积/mL |
|
| 滴定前刻度/mL |
滴定后刻度/mL |
||
| 1 |
0.3000 |
1.02 |
24.04 |
| 2 |
0.3000 |
2.00 |
25.03 |
| 3 |
0.3000 |
0.20 |
23.24 |
表1. KMnO4标准溶液滴定数据
莽草酸是合成治疗禽流感的药物——达菲(Tamiflu)的原料之一。莽草酸是A的一种异构体。A的结构简式如下: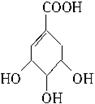 (提示:环丁烷
(提示:环丁烷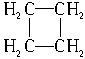 可简写成
可简写成 )
)
(1)A的分子式是_________。
(2)A与溴的四氯化碳溶液反应的化学方程式(有机物用结构简式表示)是_________________________。
(3)A与氢氧化钠溶液反应的化学方程式(有机物用结构简式表示)是___________________________。
(4)1.74 g A与足量碳酸氢钠溶液反应,计算生成二氯化碳的体积(标准状况)。
(5)A在浓硫酸作用下加热可得到B(B的结构简式为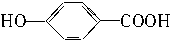 ),其反应类型是_________。
),其反应类型是_________。
(6)B的同分异构体中既含有酚羟基又含有酯基的共有__________种,写出其中一种同分异构体的结构简式___________________。
A和B两种物质的分子式都是C7H8O,它们都能跟金属Na反应放出H2;A不溶于NaOH溶液而B能溶于NaOH溶液,B能使适量浓溴水褪色,并产生白色沉淀,A不能;B的一溴代物有两种结构。则A和B的名称及结构简式为:A_____________,B_____________。
某工业反应混合液中仅可能含有的组分是:乙醚(C4H10O)、乙醇(C2H6O)和水。经分析,液体中各原子的物质的量之比为n(C)∶n(H)∶n(O)=16∶42∶5。
(1)若混合液中只含两种组分,则所有可能的组合是_________________。
(2)若混合液中含有三种组分,在628 g混合液中有1 mol H2O,此时乙醇和乙醚的物质的量各是_______________。
根据下面合成路线完成有关问题: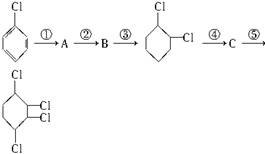
(1)写出A、B、C结构简式:A:____________,B:____________,C:____________。
(2)各步反应类型:①_________,②_________,③_________,④_________,⑤________。
(3)A→B的反应试剂及条件:____________________。
已知在催化剂作用下,苯和卤代烃反应可以在苯环上引入烷烃基,生成苯的同系物。如 +HCl,现从苯出发制取十二烷基苯,再进一步制取合成洗涤剂十二烷基苯磺酸钠,分子式为
+HCl,现从苯出发制取十二烷基苯,再进一步制取合成洗涤剂十二烷基苯磺酸钠,分子式为 。
。
提供的原料除苯外,还有水、浓硫酸、十二烷、食盐及催化剂等,试用化学方程式表示此制取过程。(已知电解食盐水生成Cl2、H2和NaOH)
(1)____________________________________;
(2)____________________________________;
(3)____________________________________;
(4)____________________________________;
(5)____________________________________。