碘及其化合物在生产、生活中具有广泛的用途。解答下列与碘元素有关的试题:
(1)碘是人体中的微量元素之一,是一种智力元素。国家推广“加碘食盐”,其中一般加入的是KIO3,而不是KI。其原因是 。
(2)常温下,NH4I是一种固体,一定温度下在密闭容器中发生下面的反应:
① NH4I(s)  NH3(g) + HI(g)
NH3(g) + HI(g)
② 2HI(g)  H2(g) + I2(g)
H2(g) + I2(g)
达到平衡时,缩小容器体积,增大体系压强,混合气体的颜色 (填“加深”或“变浅”或“不变”);达到平衡时,反应②的化学平衡常数表达式为 ;达到平衡时c(H2)=0.5mol/L,反应①的化学平衡常数为20,则 c (HI) = 。
(3)如图,在粗试管中加入饱和的KI溶液,然后再加入苯,插入两根石墨电极,接通直流电源。连接电源负极的电极为 极,电极反应式为 。通电一段时间后,断开电源,振荡试管,上层溶液为 色。
(4)已知Ksp(PbI2)=7.1×10-9mol3/L3。在盛有澄清的PbI2饱和溶液的试管中,滴加浓度为0.1mol/L的碘化钾溶液,振荡,可以观察到溶液中有黄色浑浊产生,这些黄色浑浊的成分是 。
某研究性学习小组将下列装置如图连接,a、b、c、d、g 、h都是惰性电极。A中盛有100mlCuSO4溶液;B中盛有100g质量分数为16%的氢氧化钠溶液;将电源接通后,在g极附近显红色。
、h都是惰性电极。A中盛有100mlCuSO4溶液;B中盛有100g质量分数为16%的氢氧化钠溶液;将电源接通后,在g极附近显红色。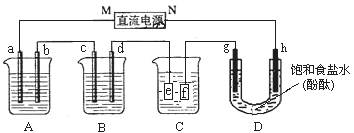
试回答下列问题:
(1)电源M极的名称是______。
(2)通电一段时间,取出电极,向A中加入4.9gCu(OH)2,溶液与电解前相同,则电解时电路中通过的电子为_________mol,原CuSO4溶液物质的量浓度为________mol•L-1;
(3)B中d的电极反应式为________________________________________________,
d极上产生的气体体积为____________L(标况)
(4)欲用C装置给铜镀银,f是__________(填银或铜),电镀液是__________溶液。
(5)电解后将D中溶液倒入烧杯,稀释至200ml,此时溶液的PH=_______。
铝和氢氧化钠都是重要的工业产品。请回答:
(1)工业冶炼铝的化学方程式是 ________________。
(2)可用阳离子交换膜法电解饱和食盐水制NaOH,其工作原理如左下图所示。
①请写出A、B两处物质的名称:A___________________、 B____________________
B____________________
②请写出电解食盐水的离子方程式__________________________________________
(3)以镁条、铝片为电极,以NaOH溶液为电解质溶液设计的原电池如上中图。
①负极材料为________(填Mg或Al)。
②该原电池的总反应式为____________________________________________
(要求用单线桥标出电子转移的方向和数目)
(4)铝—空气燃料电池可用于电动汽车,通常以NaOH溶液为电解液,铝合金为负极,通入空气的极为正极(如右上图),则
负极的电极反应式为 ______________________;
正极的电极反应式为_______________ ____________________。
____________________。
汽车的启动电源常用铅蓄电池,电池反应为:Pb+PbO2+4H++2SO2-4 2PbSO4+2H2O;据此判断:
2PbSO4+2H2O;据此判断:
(1)放电时,铅蓄电池的负极材料是________;电极反应为__________________________
(2)放电时,电解质溶液中阴离子移向________极。
(3)若用该铅蓄电池作电源电解足量的食盐水,阳极产生0.05molCl2时,理论上H2SO4的
物质的量减小_______mol。
(4)铅蓄电池上有两个接线柱,一个接线柱旁标有“+”,另一个接线柱旁标有“—”。
关于标有“—”的接线柱,下列说法中正确的是___________
A.充电时作阳极,放电时作负极 |
B.充电时作阳极,放电时作正极 |
C.充电时作阴极,放电时作负极 |
D.充电时作阴极,放电时作正极 |
(5)充电时的阳极反应式是____________________________________。
(1)粗制的CuCl2·2H2O晶体中常含有Fe3+、Fe2+杂质。在提纯时,常先加入合适的氧化剂,将Fe2+氧化为Fe3+,下列可选用的氧化剂是___________。
A.KMnO4 B.H2O2 C.Cl2水 D.HNO3
(2)己知:常温下Ksp[Fe(OH)3]=8.0×10-38,Ksp[Cu(OH)2]=2.2×10-20,㏒2=0.3。通常认为残留在溶液中的离子浓度小于1×10-5mol·L-1时就认为沉淀完全。试计算
①将溶液的pH调至PH=__________时Fe3+转化为Fe(OH)3而沉淀完全。
②若CuSO4溶液的浓度为2.2mol·L-1,则Cu(OH)2开始沉淀时溶液的pH为__________。
(3)调整溶液的pH可选用下列中的____________。
A.NaOH(aq) B.NH3·H2O C.CuO粉末 D.Cu(OH)2悬浊液 E.Cu2(OH)2CO3(s)
20℃时,醋酸的电离平衡常数为1.6×10-5。
(1)试计算20℃时0.01mol•L-1的醋酸溶液中氢离子浓度。
(2)室温时,向0.2mol•L-1的醋酸溶液中加入等体积的0.1mol•L-1的NaOH(aq),充分反应后所得溶液的PH=4,则:
①所得溶液中各离子(包括CH3COOH分子)浓度大小关系是:______________________,
②所得溶液中的物料守恒式为:________+________=__________=_________mol•L-1。
③c(CH3COOH)=_____________mol•L-1(写出算式,不做近似计算)