5—氨基酮戊酸盐是一种抗肿瘤药,其合成路线如下:
已知: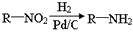
(1)5—氨基酮戊酸盐中非含氧官能团的名称是 。
(2)C→D的反应类型为 。
(3)已知A分子结构中有一个环,A不能使溴水褪色,且核磁共振氢谱图上只有一种环境的氢原子,则A的结构简式为 。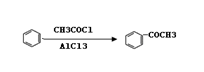
(4)G是B的一种同分异构体,能与NaHCO3溶液反应,能发生银镜反应,1molG与足量金属Na反应能生成1molH2,且G分子中不含甲基,写出一种符合上述条件的G的结构简式 。
(5)写出D→E反应的化学方程式 。
(6)已知,请结合题中所给信息,写出由CH3CH2COOH、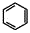 为原料合成
为原料合成  单体的第一步的合成路线和最后一步的化学方程式(无机试剂任选)。
单体的第一步的合成路线和最后一步的化学方程式(无机试剂任选)。
①第一步的合成路线:
②最后一步的化学方程式:
(1)科学家根据体系存在着力图使自身能量趋于 和由 变为 的自然现象,提出了互相关联的 判据和 判据,为最终解决“反应进行的方向”这一问题提供了必要的依据。
(2)在密闭条件下,体系有有序自发地转变为无序的倾向,因为与有序体系相比,无序体系更加稳定,科学家把这种因素称作 。
(3)判断下列过程熵变的正负(填“>0”或“<0”):
①溶解少量蔗糖于水中,ΔS ;
②纯碳和氧气反应生成CO(g),ΔS ;
③液态水蒸发变成水蒸气,ΔS ;
④CaCO3(s)加热分解生成CaO(s)和CO2(g),ΔS 。
在一定体积的密闭容器中,进行如下化学反应:CO2(g)+H2(g) CO(g)+H2O(g),其化学平衡常数K和温度t的关系如下表所示:
CO(g)+H2O(g),其化学平衡常数K和温度t的关系如下表所示:
| t/℃ |
700 |
800 |
830 |
1 000 |
1 200 |
| K |
0.6 |
0.9 |
1.0 |
1.7 |
2.6 |
回答下列问题:
(1)该反应的化学平衡常数表达式为K= 。
(2)该反应为 反应(填“吸热”或“放热”)。
(3)能判断该反应是否达到化学平衡状态的依据是( )
A.容器中压强不变
B.混合气体中c(CO)不变
C.v正(H2)=v逆(H2O)
D.c(CO2)=c(CO)
(4)某温度下,平衡浓度符合下式:c(CO2)·c(H2)=c(CO)·c(H2O),试判断此时的温度为 ℃。
Fe3+和I-在水溶液中的反应为:2I-+2Fe3+ 2Fe2++I2(水溶液)。
2Fe2++I2(水溶液)。
该反应的平衡常数K的表达式为K= 。当上述反应达到平衡状态后,加入CCl4萃取I2,且温度不变,上述平衡 移动(填“向右”“向左”或“不”)。
在2 L密闭容器内,800 ℃时反应2NO(g)+O2(g) 2NO2(g)体系中,n(NO)随时间的变化如下表:
2NO2(g)体系中,n(NO)随时间的变化如下表:
| 时间/s |
0 |
1 |
2 |
3 |
4 |
5 |
| n(NO)/mol |
0.020 |
0.010 |
0.008 |
0.007 |
0.007 |
0.007 |
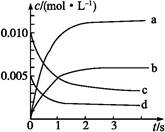
(1)上图表示NO2的浓度变化的曲线是 。用O2表示从0~2 s内该反应的平衡速率v= 。
(2)能说明该反应已达到平衡状态的是 。
a.v(NO2)=2v(O2) b.容器内压强保持不变
c.v逆(NO)=2v正(O2) d.容器内密度保持不变
下列可以证明H2(g)+I2(g) 2HI(g)已达平衡状态的是 。
2HI(g)已达平衡状态的是 。
①单位时间内生成n mol H2的同时,生成n mol HI
②一个H—H键断裂的同时有两个H—I键断裂
③百分含量w(HI)=w(I2)
④反应速率v(H2)=v(I2)=v(HI)
⑤c(HI)∶c(H2)∶c(I2)=2∶1∶1
⑥温度和体积一定时,生成物浓度不再变化
⑦温度和体积一定时,容器内压强不再变化
⑧条件一定,混合气体的平均相对分子质量不再变化