Fe3+和I-在水溶液中的反应为:2I-+2Fe3+ 2Fe2++I2(水溶液)。
2Fe2++I2(水溶液)。
该反应的平衡常数K的表达式为K= 。当上述反应达到平衡状态后,加入CCl4萃取I2,且温度不变,上述平衡 移动(填“向右”“向左”或“不”)。
可逆反应3A(g)3B(?)+C(?) ΔH>0达到化学平衡后,
(1)升高温度,用“变大”、“变小”、“不变”或“无法确定”填空。
①若B、C都是气体,气体的平均相对分子质量 。
②若B、C都不是气体,气体的平均相对分子质量 。
③若B是气体,C不是气体,气体的平均相对分子质量 。
如果平衡后保持温度不变,将容器体积增加一倍,新平衡时A的浓度是原来的60%,
则B是态,C是 态。
在一定条件下,可逆反应:mA+nBpC达到平衡,若:
(1)A、B、C都是气体,减少压强,平衡向正反应方向移动,则m+n和p的关系是 。
(2)A、C是气体,增加B的量,平衡不移动,则B为态。
(3)A、C是气体,而且m+n=p,增大压强可使平衡发生移动,则平衡移动的方向是 。
(4)加热后,可使C的质量增加,则正反应是反应(填“放热”或“吸热”)。
(1)写出下列物质在水溶液中电离的方程式
HNO3HClO
NaHCO3
(2)在25℃、101kPa下,1g甲醇燃烧生成CO2和液态水时放热22.68kJ。则表示甲醇燃烧热的热化学方程式为___________________________________________。
(3)己知:①H2(g)+1/2O2(g)=H2O(l) ΔH=-285.8 kJ·mol-1
②H2(g)+1/2O2(g)=H2O(g) ΔH=-241.8 kJ·mol-1
③C(s)+1/2O2(g)=CO(g) ΔH=-110.5 kJ·mol-1
④C(s)+ O2(g)=CO2(g) ΔH=-393.5 kJ·mol-1
回答下列问题:
①上述反应中属于放热反应的是_________________。
②H2的燃烧热为_______________,C的燃烧热为__________________.
③燃烧l0gH2生成液态水,放出的热量为_________________.
④CO的燃烧热为___________,其热化学方程式为_______________________.
(14分)金刚烷是一种重要的化工原料,工业上可通过下列途径制备: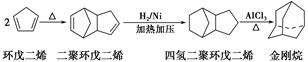
请回答下列问题:
(1)环戊二烯分子中最多有______个原子共平面。
(2)金刚烷的分子式为__________。
(3)下面是以环戊烷为原料制备环戊二烯的合成路线: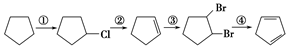
其中,反应②的反应试剂和反应条件是___________,反应③的反应类型是____________,反应④的化学方程式为。
(4)已知烯烃能发生如下反应: 。
。
请写出下列反应产物的结构简式: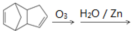 ____________________________。
____________________________。
(5)A是二聚环戊二烯的同分异构体,能使溴的四氯化碳溶液褪色,A经酸性高锰酸钾溶液加热氧化可以得到对苯二甲酸( )[提示:苯环上的烷基(—CH3,—CH2R,—CHR2)或烯基侧链经酸性高锰酸钾溶液氧化得羧基(—COOH)]
)[提示:苯环上的烷基(—CH3,—CH2R,—CHR2)或烯基侧链经酸性高锰酸钾溶液氧化得羧基(—COOH)]
写出A所有可能的结构简式(不考虑立体异构):___________________________________。
有A、B、C、D、E五种元素,其相关信息如下:
| 元素 |
相关信息 |
| A |
A原子的1s轨道上只有1个电子 |
| B |
B是电负性最大的元素 |
| C |
C基态原子的2p轨道中有3个未成对电子 |
| D |
D是主族元素且与E同周期,其最外能层上有2个运动状态不同的电子 |
| E |
E的+1价离子的M能层中所有能级各轨道都有电子且没有未成对电子 |
请回答下列问题:
(1)写出元素E的基态原子的电子排布式_________________。
(2)CA3分子中C原子的杂化类型是________;在元素E的硫酸盐溶液中逐渐通入CA3,可以观察到的实验现象是,发生的有关反应的离子方程式为。
(3)C与A还可形成C2A4、CA5等化合物,二者都能与盐酸反应。则C2A4与盐酸反应的离子方程式为。CA5还可与水反应产生无色气体,且所得溶液显碱性,则CA5的电子式为,与水反应的化学方程式。
(4)A、C、E三种元素可形成[E(CA3)4]2+,其中存在的化学键类型有____(填序号);
1mol该离子中含有个σ键。
①配位键 ②金属键 ③极性共价键 ④非极性共价键 ⑤离子键 ⑥氢键
若[E(CA3)4]2+具有对称的空间构型,且当[E(CA3)4]2+中的两个CA3被两个Cl-取代时,能得到两种不同结构的产物,则[E(CA3)4]2+的空间构型为_________(填序号)。
a.平面正方形B.正四面体 c.三角锥形 D.V形
(5)B与D可形成离子化合物,其晶胞结构如图所示。
其中D离子的配位数为 ________,该晶体的化学式为__________。