某些有机化合物之间具有如下转化关系: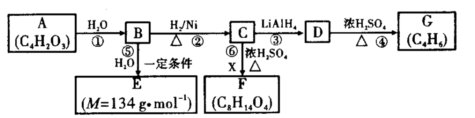
其中:A是一种五元环状化合物,其分子中只有一种化学环境的氢原子;F核磁共振氢谱显示有三种不同化学环境的氢原子,且峰面积之比为2:2:3;G是合成顺丁橡胶的主要原料。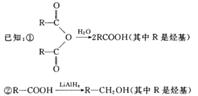
(1)A的结构简式是 。
(2)B中所含官能团的名称是 。
(3)写出反应类型:③ ,④
(4)⑥的化学方程式为
(5)E在一定条件下能够发生缩聚反应,写出链节是由四个原子组成的高聚物的结构简式 。有机物Y与E互为同分异构体,且具有相同的官能团种类和数目,则Y的结构简式可能有 种。
下列是元素周期表的短周期中的部分元素
| 族 周期 |
ⅠA |
ⅡA |
ⅢA |
ⅣA |
ⅤA |
ⅥA |
ⅦA |
0 |
| 1 |
A |
|||||||
| 2 |
B |
C |
D |
E |
||||
| 3 |
F |
G |
H |
I |
L |
(1)表中元素,原子半径最大的是________,原子半径最小的是________。(不包括稀有气体元素。填空均用元素符号或化学式回答,下同)
(2)金属性最强的是;化学性质最不活泼的是;最高正价和负价的绝对值相等的是;氢化物水溶液呈碱性的是。
(3)I和L最高价氧化物对应的水化物酸性较强的是,判断依据之一是
现有一包AlCl3和FeCl3的混合粉末,欲将其中的Al元素和Fe元素分开,可进行如下操作:
(1) 操作①名称是,操作②名称是(过滤/分液/蒸馏/溶解/结晶);
(2)溶液B是,沉淀C是
(3)若往溶液A中滴入KSCN溶液,预计会观察到溶液呈色;
(4)请写出在溶液中,FeCl3和NaOH反应的离子方程式:
某芳香烃A,分子式为C8H10;某烃类衍生物X,分子式为C15H14O3,能使FeCl3溶液显紫色:J分子内有两个互为对位的取代基。在一定条件下有如下的转化关系:
⑴A物质的结构简式为:________________;J中所含的含氧官能团的名称为_____________。
⑵E与H反应的化学方程式是;反应类型是___________。
⑶B、C的混合物在NaOH乙醇溶液中加热可以生成同一种有机物I,以I为单体合成的高分子化合物的化学方程式是。
⑷写出符合下列性质的J的所有同分异构体的结构简式。①与FeCl3溶液作用显紫色;②与新制Cu(OH)2悬浊液作用产生红色沉淀;③苯环上的一卤代物有2种。
(10分)写出下列反应的化学方程式:
(1)实验室制乙炔。
(2)TNT炸药制取。
(3)苯酚和溴水反应。
(4)乙醛与新制Cu(OH)2反应。
(5)溴乙烷消去反应。
下列有机化合物都含有多个官能团:
(1)能够与 NaOH溶液反应的有_________________。(填入字母编号,下同)
(2)能够与 Na2CO3溶液反应的有_______________________。
(3)能够与 NaHCO3溶液反应的有_______________________。