甲醇是一种很好的燃料,工业上用CH4和H2O 为原料,通过反应I和Ⅱ来制备甲醇。
⑴将1.0 mol CH4和2.0 mol H2O(g)通人反应室(容积为100L),在一定条件下发生反应:
CH4(g)+H2O(g) CO(g)+3H2(g)……I。CH4的转化率与温度、压强的关系如右图所示。
CO(g)+3H2(g)……I。CH4的转化率与温度、压强的关系如右图所示。
①已知100℃时达到平衡所需的时间为5min,则用H2表示的平均反应速率为 。
②图中的P1_ P2(填“<”、“>”或“=”),100℃时平衡常数为 。
③该反应的△H 0(填“<”、“>”或“=”)。
(2)在一定条件下,将a mol CO与3a mol H2的混合气体在催化剂作用下能自发反应生成甲醇: CO(g)+2H2(g) CH3OH(g) △H<0 ……Ⅱ
CH3OH(g) △H<0 ……Ⅱ
④若容器容积不变,下列措施可增加甲醇产率的是
A.升高温度 B.将CH3OH(g)从体系中分离
C.充人He,使体系总压强增大 D.再充人lmol CO和3 mol H2
⑤为了寻找合成甲醇的温度和压强的适宜条件,某同学设计了三组实验,部分实验条件已经填在下面实验设计表中。
A.下表中剩余的实验条件数据: a=_ ;b=_ 。
| 实验编号 |
T(℃) |
n(CO)/n(H2) |
P(Mpa) |
| 1 |
150 |
1/3 |
0.1 |
| 2 |
a |
1/3 |
5 |
| 3 |
350 |
b |
5 |
B.根据反应Ⅱ的特点,右下图是在压强分别为0.1 MPa和5MPa下CO的转化率随温度变化的曲线图,请指明图中的压强Px = Mpa。
虽然氟元素早在1810年就被发现,但170多年来化学家试图用化学方法制取氟单质的尝试一直未获成功。直到1986年,化学家Karl Chrisie首次用化学方法制得了F2,他提出的三步反应如下:
①KMnO4+KF+H2O2+HF―→K2MnF6+______+H2O
②SbCl5+HF===SbF5+5HCl
③2K2MnF6+4SbF5===4KSbF6+2MnF3+F2↑
请根据以上信息回答下列问题:
(1)反应①中空格上应填物质的化学式为__________________。
(2)反应②是否为氧化还原反应________(选填“是”、“否”或“无法确定”)。
(3)反应③中的氧化剂为________,被氧化的元素为________。
(4)每生成1mol F2,消耗KMnO4的物质的量为。
0.80 g CuSO4·5H2O样品受热脱水过程的热重曲线(样品质量随温度变化的曲线)如下图所示。
请回答下列问题:
(1)试确定200 ℃时固体物质的化学式______________。
(2)取270 ℃所得样品,于570 ℃灼烧得到的主要产物是黑色粉末和一种氧化性气体,该反应的化学方程式为_______________________________;把该黑色粉末溶解于稀硫酸中,经浓缩、冷却,有晶体析出,该晶体的化学式为____________,其存在的最高温度是________;
(3)上述氧化性气体与水反应生成一种化合物,该化合物的浓溶液与Cu在加热时发生反应的化学方程式为______________________________________________________
(1)23.75g某二价金属的氯化物(MCl2)中含有3.01×1023Cl-,则MCl2的摩尔质量是________,MCl2的相对分子质量是________,M的相对原子质量是________。
(2)2 mol 尿素[CO(NH2)2]所含氧原子跟________ g H2O所含氧原子个数相等。
(3)标准状况下,22.4 L CH4;②1.5 mol NH3;③1.806×1024个H2O;④标准状况下,73 g HCl。所含H原子个数由多到少的顺序是________。
食品安全关系国计民生,影响食品安全的因素很多.
(1)聚偏二氯乙烯(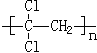 )具有超强阻隔性能,可作为保鲜食品的包装材料.它是由_______(写结构简式)发生加聚反应生成的.
)具有超强阻隔性能,可作为保鲜食品的包装材料.它是由_______(写结构简式)发生加聚反应生成的.
(2)劣质植物油中的亚油酸[CH3(CH2)4CH=CHCH2CH=CH(CH2)7COOH]含量很低.下列关于亚油酸的说法中,正确的是_________ .
A.分子式为C18H34O2
B.一定条件下能与甘油(丙三醇)发生酯化反应
C.能和NaOH溶液反应
D.能使酸性KMnO4溶液退色
(3)假酒中甲醇(CH3OH)含量超标,请写出Na和甲醇反应的化学方程式:____ __ .
(4)劣质奶粉中蛋白质含量很低.蛋白质水解的最终产物是______ ___ .
(5)在淀粉中加入吊白块制得的粉丝有毒.淀粉最终的水解产物是葡萄糖.请设计实验证明淀粉已经完全水解,写出操作、现象和结论:______ ___ .
(6)下列有关实验的叙述,正确的是_____(填序号)
A、用NaOH溶液除去乙酸乙酯中混有的乙酸、乙醇,然后分液
B、分馏石油时,温度计的末端必须插入液面下
C、用分液漏斗分离环己烷和水的混合液体
D、用浓氨水洗涤做过银镜反应的试管
E、配制银氨溶液时,将稀氨水慢慢滴加到稀硝酸银溶液中,产生白色沉淀后继续滴加到沉淀刚好溶解为止
F、蔗糖水解后,直接滴加新制氢氧化铜悬浊液并加热检验水解产物中的葡萄糖
(12分)推断下列化合物的化学式:
(1)X、Y两元素能形成XY2型化合物,XY2中共有38个电子,若XY2是离子化合物,其化学式是__________;若XY2是共价化合物,其化学式是__________。
(2)第三周期内,X、Y两元素的原子序数之差为4,它们组成的XY型化合物,其化学式为____。
(3)1 mol某共价化合物,含有三种短周期元素的原子各1 mol,且三种元素分别属于不同的周期,其质子总数为26 mol,其中一种元素的最外层有7个电子,则该物质的化学式为__________。
(4)某非金属X的最低负价为-2,它的最高价氧化物对应的水化物为强酸,则这种酸的化学式是__________。
(5)X元素的最高正价和负价绝对值之差为6,Y元素的化合价为+1,Y元素和X元素原子的次外电子层上都有8个电子,X和Y形成的化合物在水溶液中能电离出电子层结构相同的离子,则该化合物是__________。