中国尿素合成塔(尿塔)使用寿命仅为欧美国家的1/4。为此北京钢铁研究 院对四川泸天化尿塔腐蚀过程进行研究,得出下列腐蚀机理: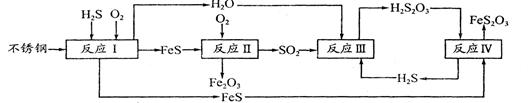
(1)H2S来自合成尿素的天然气。在380 K、体积为2 L的密闭容器中,存在如下反应:H2(g)+S(s) H2S(g) △H=+21.6kJ·mol-1。反应达到平衡时H2、S、H2S的物质的量均为3 mol,则380 K时该反应的化学平衡常数为______;下列对该反应分析正确的是______(填字母序号)。
H2S(g) △H=+21.6kJ·mol-1。反应达到平衡时H2、S、H2S的物质的量均为3 mol,则380 K时该反应的化学平衡常数为______;下列对该反应分析正确的是______(填字母序号)。
(2)在反应I中发生的化学反应为______。
(3)研究发现反应II是分别以Fe、FeS为电极,以水膜为电解质溶液的电化学腐蚀,其 负
极为______;
已知:Fe(s)+S(s)=FeS(s) △H1=-2.5akJ·mol-1
S(s)+O2(g)=SO2(g) △H2=-5akJ·mol-1
4Fe(s)+3O2(g)=2Fe2O3(s) △H3=-6akJ·mol-1
则反应II的热化学方程式为_____
(4)已知H2S2O3的K1=2.2×10-1、K2=2.8×10-2。Na2S2O3水溶液呈______性,该溶液中电荷守恒式为_____ ;反应IY的反应类型为______ ;该反应______(填“能”或“不能”) 说明FeS溶解性强于FeS2O3
(5)泸天化尿塔的最终腐蚀产物为______;为了有效防腐,北钢建议泸天化在生产中用 CuSO4溶液“脱硫(H2S)”,其中涉及的离子方程式为
__________________
工业上用CO生产燃料甲醇,一定条件下发生反应: CO(g)+2H2(g)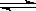 CH3OH(g)。
CH3OH(g)。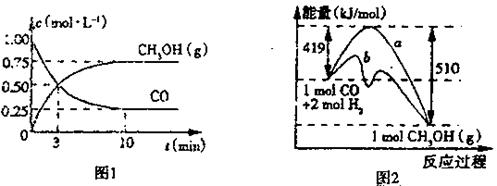
(1)图1是反应时CO和CH3OH(g)的浓度随时间变化情况。从反应开始到平衡,用CO浓度变化表示平均反应速率v(CO)=。
(2)图2表示该反应进行过程中能量的变化。曲线(填“a”或“b”)表示不使用催化剂时反应的能量变化,不使用催化剂时该反应的逆反应的活化能为。
(3)该反应平衡常数K的表达式为,温度升高,平衡常数K(填“增 大”、“不变”或“减小”)
大”、“不变”或“减小”)
(4)恒容条件下,下列措施中能使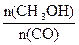 增大的有。
增大的有。
| A.升高温度 | B.充入He气 |
| C.再充入1molCO和2molH2 | D.使用催化剂 |
甲、乙、丙、丁是4种短周期元素,它们的原子序数依次增大;其中甲和丙、乙和丁分别 是同主族元素,又知乙、丁两元素的原子核中质子数和是甲、丙原子核中质子数之和的2倍,甲元素的一种同位素核内无中子。
是同主族元素,又知乙、丁两元素的原子核中质子数和是甲、丙原子核中质子数之和的2倍,甲元素的一种同位素核内无中子。
(1)过量的乙与丁组成的一种化合物通入紫色石蕊试液中的现象是。写出均含甲、乙、丙、丁四种元素的两种化合物相互间发生反应,且生成气体的离子方程式 。
。
(2)甲与乙组成的化合物与乙和丙组成的化合物反应能产生乙单质,写出该反应的化学方程式。
(3)用甲元素的单质与乙元素的单质可以制成电池,电池中装有KOH浓溶液,用多孔的金属惰性电极浸入KOH溶液,在A极通入甲的单质,B极通入乙的单质,则A极是该电池的极;B极的电极反应式是: 。
。
(4)将丁与乙元素以原子个数1:2组成的化合物6.4g与80mL2mol/L的NaOH溶液恰好反应,则所生成溶质总质量为g。
丙烯酰胺是一种重要的有机合成的中间体。它的球棍模型如下图所示:(图中“棍”代表单键或双键或三键,不同颜色球表示不同原子:C、H、O、N)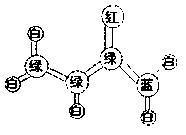
(1)丙烯酸胺的分子式为,结构简式为。
(2)有关丙烯酸胺的说法正确的是
A.丙烯酸胺分子内所有原子不可能在同一平面内
B.丙烯到胺属于烃的含氧衍生物
C.丙烯酰胺能够使酸性高锰酸钾溶液褪色
D.丙烯酸胺能够使溴的四氯化碳溶液褪色
(3)工业上生产丙烯酸胺的方法之一是 (反应均在一定条件下进行):
(反应均在一定条件下进行):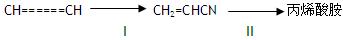
反应I和反应I I都是原子利用率100%的反应,反应I所需另一反应物的分子式为,反应II的方程式为。
I都是原子利用率100%的反应,反应I所需另一反应物的分子式为,反应II的方程式为。
(4)聚丙烯酰胺(PAM)是一种合成有机高分子絮凝剂,写出由丙烯酰胺合成聚丙烯酰胺的化学方程式并注明反应类型。
(10分)按照下图连接线路,反应一段时间后,回答下列问题(假设原电池所提供的电能可以保证电解反应的顺利进行):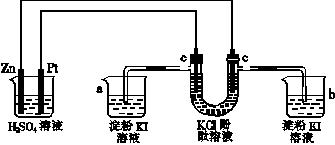
(1)写出U形管内出现的现象:右侧管 。
(2)写出有关反应的化学方程式: 、
、 。
(3)写出a烧杯中出现的现象: 。
氨是氮循环过程中的重要物质,氨的合成是目前普遍使用的人工固氮方法。
(1)已知:H—H键能为436 kJ/mol, N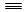 N键能为945 kJ/mol,N—H键能为391 kJ/mol。写出工业合成氨反应的化学方程式;由键能计算说明此反应是反应(填“吸热”或“放热”),合成氨反应(消耗1molN2 时)的△H =。
N键能为945 kJ/mol,N—H键能为391 kJ/mol。写出工业合成氨反应的化学方程式;由键能计算说明此反应是反应(填“吸热”或“放热”),合成氨反应(消耗1molN2 时)的△H =。
(2)恒温下,向一个2L的密闭容器中充入1 mol N2和2.6 mol H2,反应过程中对NH3的浓度进行检测,得到的数据如下表所示:
| 时间/min |
5 |
10 |
15 |
20 |
25 |
30 |
| c(NH3)/(mol/L) |
0.08 |
0.14 |
0.18 |
0.20 |
0.20 |
0.20 |
5min内,用N2浓度的变化表示的反应速率为,此条件下, 反应达到平衡的时间为:,其化学平衡常数K=;达到平衡后氨气的转化率为:。