I.高炉炼铁的主要反应为Fe2O3+3CO2Fe+3CO2。
已知该反应的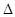 H,在1000℃时,K=64。在1000℃的条,在容积10 L的密闭容器中,加入Fe、Fe2O3、CO、CO2各1.OmoI,反应经10 min后达到平衡。
H,在1000℃时,K=64。在1000℃的条,在容积10 L的密闭容器中,加入Fe、Fe2O3、CO、CO2各1.OmoI,反应经10 min后达到平衡。
(1)该时间范围内的平均反应速率v(CO2)=_________mol/L min
min
(2) 的最大转化率_________________。
(3)欲提高CO的平衡转化率,可采取的措施是_______________。
| A.减少Fe的量 | B.增加Fe2O3的量 |
| C.升高反应温度 | D.移出部分CO2 |
E.使用合适的催化剂 F.减少容器的容积
Ⅱ.已知化学反应①:Fe(s)+CO2(g) FeO(s)+CO(g),其平衡常数为K1;化学反应②:Fe(s)+H2O(g)
FeO(s)+CO(g),其平衡常数为K1;化学反应②:Fe(s)+H2O(g) FeO(s)+H2(g),其平衡常数K2.在温度973K和1173K情况下,K1、K2的值分别如下:
FeO(s)+H2(g),其平衡常数K2.在温度973K和1173K情况下,K1、K2的值分别如下:
| 温度 |
K1 |
K2 |
| 973K |
1.47 |
2.38 |
| 1173K |
2.15 |
1.67 |
(4)通过表格中的数值可以推断:反应①的△H_ O。(填“>”“<”)
(5)现有反应③:该反应的平衡常数的数学表
达式K3=____。
(6)根据反应①和②可以推导出Ki,Kz和玛之间的关系式。K3=__________。据此关系式和上表数据,也能推断出反应③的△H_ _0(填“>”“<”)。
有一包白色粉末可能由K2SO4、NaHCO3、BaCl2、FeCl3、KCl五种物质中的某几种组成,现进行如下实验:
①将白色粉末加水溶解,得无色溶液。
②向①中所得的无色溶液中加入NaOH溶液,观察到有白色沉淀A生成,过滤后,向滤液中滴加硝酸酸化的AgNO3溶液,又得到白色沉淀B。
根据上述现象判断:
(1)A的化学式是
(2)B的化学式是
(3)原白色粉末中一定含有,可能含有,对可能含有的物质,可通过(填实验名称)进一步检验。
古老但仍然是最有用的制备联氨(N2H4)溶液的方法如下:
NaClO+NH3·H2O  N2H4 +NaCl+H2O
N2H4 +NaCl+H2O
(1)请配平上述化学方程式。并用单线桥法标出电子转移的方向和数目。
(2)NH3·H2O在上述反应中显示出来的性质是。
| A.氧化性 | B.还原性 | C.酸性 | D.碱性 |
(3)该反应的氧化产物是,NaClO发生反应。
(4)若生成 0.2 mol N2H4,则转移的电子为mol。
在浓HNO3中放入铜片:
(1)反应开始时的化学方程为。
(2)若有铜剩余,则反应快要结束时的化学方程式为。
(3)待反应停止时,再加入少量25%的稀硫酸,这时铜片上又有气泡产生,其原因和离子方程式是。
(4)若将12.8g铜与一定质量的浓硝酸反应,铜耗完时,共产生气体5.6 L(标准状况),则消耗硝酸的物质的量是,所得气体的平均相对分子质量为。
(5)若将(4)中所得物质配成100mL 溶液,下列操作可能使所配溶液浓度偏小的是_______ ___(填写序号)。
①未洗涤烧杯和玻璃棒②定容摇匀静置后,发现液面低于刻度线后继续加水至凹液面与刻度线相切③配溶液前容量瓶中有少量蒸馏水④定容时俯视容量瓶的刻度线
所得硝酸铜的物质的量浓度为mol/L。
(每空2分,共8分)
(1) 除去NaHCO3溶液中混有的Na2CO3,相应的化学方程式_____________。
(2) 除去Na2CO3固体中混有的NaHCO3,相应的化学方程式_____________。
(3) 除去CO2气体中混有的HCl,相应的离子方程式___________________。
(4) 除去Fe2O3中混有的Al2O3,相应的离子方程式_____________________。
(8分)在一容积固定的密闭容器中,保持一定条件进行以下反应:X(g)+2Y(g) 3Z(g),已知向容器中加入2molX和3molY达到平衡后,生成amolZ。
3Z(g),已知向容器中加入2molX和3molY达到平衡后,生成amolZ。
(1)在相同实验条件下,若在同一容器中改为加入4molX和6molY,达到平衡后,z的物质的量为。
(2)在相同实验条件下,若在同一容器中改为加入3molX和2molY,若要求平衡时混合气体中Z的体积分数不变,则还需加入Zmol。
(3)在相同的实验条件下,若在同一容器中改为加入0.5molX,则需加molY,molZ,才能使平衡时Z为0.6amol。