已知2A2(g)+B2(g) 2C(g);△H=" -a" kJ/mol(a >0),在一个有催化剂的固定容积的容器中加入2mol A2和1mol B2,在500℃时充分反应达平衡后C的浓度为w mol/L,放出热量b kJ。请回答下列问题:
2C(g);△H=" -a" kJ/mol(a >0),在一个有催化剂的固定容积的容器中加入2mol A2和1mol B2,在500℃时充分反应达平衡后C的浓度为w mol/L,放出热量b kJ。请回答下列问题:
(1)比较a______b(填>、=、<)
(2)此反应的平衡常数表达式为______________________;若将反应温度升高到700℃,反应的平衡常数将_____________(增大、减小或不变)。
(3)若在原来的容器中,只加入2mol C,500℃时充分反应达平衡后,吸收热量ckJ,a、b、c之间满足何种关系__________________(用代数式表示)。
(4)能说明该反应已经达到平衡状态的是 (填序号,有一个或多个选项符合题意,下同)。
a、v(C)=2v(B2) b、容器内气体压强保持不变
c、v逆(A2)=2v正(B2) d、容器内的气体密度保持不变
(5)为使该反应的反应速率增大,且平衡向正反应方向移动的是_____________。
a、及时分离出C气体 b、适当升高温度
c、增大B2的浓度 d、选择高效的催化剂
(6)若将上述容器改为恒压容器(反应前体积相同),起始时加入2mol A2和1mol B2, 500℃时充分反应达平衡后,放出热量dkJ,则d_________b(填>、=、<)。
A、B、C、D、E、F为原子序数依次增大的同 一短周期的主族元素,已知A、C、F三种元素原子的最外层共有11个电子,且这三种元素的最高价氧化物对应的水化物之间两两皆能反应生成盐和水,D元素原子次外层电子数是最外层电子数的2倍,E的气态氢化物的化学式为H2E。G元素是与以上元素既不在同一周期也不在同一主族的短周期主族元素,请回答:
一短周期的主族元素,已知A、C、F三种元素原子的最外层共有11个电子,且这三种元素的最高价氧化物对应的水化物之间两两皆能反应生成盐和水,D元素原子次外层电子数是最外层电子数的2倍,E的气态氢化物的化学式为H2E。G元素是与以上元素既不在同一周期也不在同一主族的短周期主族元素,请回答:
(1)写出E元素在元素周期表中的位置为
(2)D的原子结构示意图为
(3)用电子式表示出B、F形成化合物的电子式
(4)以上元素中原子半径最大的是金属性最强的元素是(均用元素名称回答)
(5)实验室制备G的氢化物的化学方程式:
(6)如果向D的最高价氧化物对应水化物的钠盐溶液中滴入1—2滴酚酞,再逐滴滴入稀盐酸 ①这个过程中相应的现象是
②相应的化学方程式:
现有一种溶液,其中可能含有Mg2+、Al3+、Fe2+、Cu2+、NH4+。当加入一种淡黄色固体并加热溶解时,有刺激性气味的气体放出和白色沉淀生成,加入淡黄色固体的物质的量(横坐标)与析出的沉淀和产生气体的物质的量(纵坐标)的关系如图所示。试回答下列问题: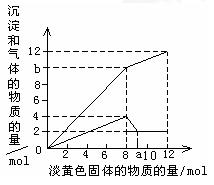
(1)最终的白色沉淀的成分是(填化学式),你的理由是
(2)试确定该溶液中可能含有以上离子中的哪些离子并计算其相应的物质的量,完成下表(可以不填满)
| 可能含有的离子 (填离子符号) |
|||||
| 相应的物质的量 |
(4)图中a点的值为
(5)图中b点的气体组成成分是(填化学式),其物质的量之比是
有一混合气体,可能由H2、O2、NH3、N2、CO2、HCl和He中的两种或多种组成。常温下,取此气体200mL进行实验,实验的过程和结果如下:
(1)观察此混合气体为无色。
(2)将此气体通过浓H2SO4,气体体积减少了40mL。
(3)将(2)中剩余的气体,通过Na2O2固体,气体体积变为120mL。
(4)将(3)中剩余的气体引燃充分反应后,冷却至常温,气体体积又减少了105mL。
(5)又将(4)中剩余的气体通过炽热的铜网,气体的体积又减少了三分之一(上述气体的体积都是相同条件下测定的)。
根据上述实验,试推断:
(1)混合气体中肯定存在的气体是,它们的体积分别为
。
(2)混合气体中肯定不存在的气体是。
(3)混合气体中可能含有的气体是,其体积共为
。
某学生利用氯酸钾分解制氧气的反应,测定氧气的摩尔质量。实验步骤如下:
|


①检查装置气密性
②把适量的氯酸钾粉末和少量二氧化锰粉末混合均匀,放入干燥的试管中,准确称量,质量为ag。
③装好实验装置。
④加热,开始反应,直到产生一定量的气体
⑤停止加热,测量收集到气体的体积
⑥准确称量试管和残留物的质量为b g。
⑦测量实验室的温度。
⑧处理实验数据,求出氧气的摩尔质量。
回答下列问题:
(1)如何检查装置的气密性? 。
(2)以下是测量收集到气体体积必须包括的几个步骤:
①调整量筒内外液面高度使之相同;
②使试管和量筒内的气体都冷却至室温;
③读取量筒内气体的体积。
这三 步操作的正确顺序是: (请填写步骤代号)。
步操作的正确顺序是: (请填写步骤代号)。
(3)如果实验中得到的氧气体积是cL(25℃、1.0l×l05Pa,该条件下气体的摩尔体积为Vm).氧气的摩尔质量的计 算式为(含a、b、c,不必化简):M(O2)= 。
算式为(含a、b、c,不必化简):M(O2)= 。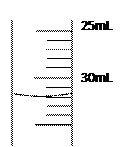 (4)若50mL量筒内液面如右图所示,则所测得气体的体积约为____________________mL.
(4)若50mL量筒内液面如右图所示,则所测得气体的体积约为____________________mL.
(5)若计算所得结果比实际值偏大,则可能的原因是___________
| A.氯酸钾中混有不产生氧气的固体杂质 |
| B.第一次称量时药品、砝码反置 |
| C.药品未完全分解 |
| D.量筒内液体被排尽 |
E.装置漏气
F.读数时俯视量筒刻度
现有A、B、C、D、E五种可溶性强电解质,它们在水中可电离产生下列离子(各种离子不重复)。
| 阳离子 |
H+、Na+、A13+、Ag+、Ba2+ |
| 阴离子 |
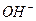 、 、 、 、 、 、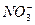 、 、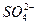 |
已知:① A、B两溶液呈碱性,等物质的量浓度时,B溶液的碱性强于A溶液。
② C是酸,只与D产生沉淀。
③ A溶液与E溶液反应既有气体又有沉淀产生
试回答下列问题:
(1)分别写出A、B、C、D、E的化学式:A、B、C、D 、E;
(2)写出A、E反应的离子方程式:;
(3)将C溶液逐滴加入等体积、等物质的量浓度的A溶液中至反应完全,离子方程式为:。
(4)在100 mL 0.1 mol·L-1 E溶液中,逐滴加入40 mL 1.6 mol·L-1 NaOH溶液,最终得到沉淀物质的量为____mol。