用NA表示阿伏加德罗常数的值。下列叙述中不正确的是
| A.16. 9 g过氯化钡(BaO2)固体中阴、阳离子总数约为0. 2NA |
| B.常温常压下,28 g乙烯和环丁烷(C4H8)的混合气体中含有的碳原子数为2 NA |
| C.a g某气体含分子数为b,c g该气体在标况下的体积为22. 4bc/ aNAL |
| D.某密闭容器盛有0. l molN2和0. 3 mol H2,在一定条件下充分反应,转移电子的数目为0. 6NA |
在下列各溶液中通入足量CO2气体,最终有浑浊产生的是
①饱和Na2CO3溶液 ②澄清石灰水 ③Ca(ClO)2溶液
④CaCl2溶液⑤Na2SiO3溶液 ⑥NaAlO2溶液
| A.全部 | B.除①④外 | C.除①②③④外 | D.除②③④外 |
食品香精菠萝酯的生产路线(反应条件略去)如下图所示。下列叙述错误的是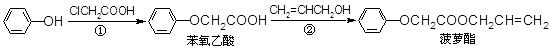
| A.步骤①产物中残留的苯酚可用FeCl3溶液检验 |
| B.步骤②产物中残留的CH2=CHCH2OH可用溴水检验 |
| C.苯酚和菠萝酯均可与酸性KMnO4溶液发生反应 |
| D.苯氧乙酸和菠萝酯均可与H2在一定条件下发生反应 |
某同学设计下列方法对A盐的水溶液进行鉴定: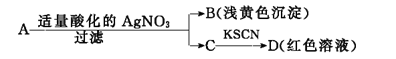
由此得出的结论中,不正确的是
| A.D溶液中存在Fe(SCN)3 | B.滤液C中有Fe3+ |
| C.B为AgBr | D.A一定是FeBr2 |
硼酸(H3BO3)分子的中心原子B最外层电子并未达到饱和,它在水中结合水分子电离出来的OH-使B原子最外层电子达到饱和,电离过程如图所示。下列表述正确的是
| A.硼酸加入水中抑制水的电离 |
| B.硼酸是三元酸 |
| C.硼酸与强碱在溶液中反应:H3BO3+OH-=[B(OH)4]- |
| D.硼酸是两性化合物 |
在一体积可变的密闭容器中,通入1molN2和3molH2,发生反应N2+3H2 2NH3,在t1时刻达到平衡。保持温度和压强不变,在t2时刻,再通入一部分NH3,反应速率与时间的关系曲线正确的是
2NH3,在t1时刻达到平衡。保持温度和压强不变,在t2时刻,再通入一部分NH3,反应速率与时间的关系曲线正确的是