铁是人体不可缺少的微量元素,硫酸亚铁晶体(FeSO4·7H2O)在医药上作补血剂。某课外小组测定该补血剂(每片b克)中铁元素的含量。实验步骤如下: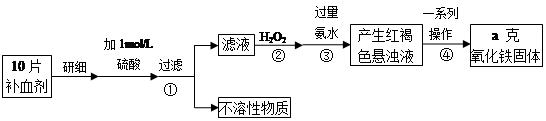
请回答下列问题:
(1)步骤②中H2O2的作用是使Fe2+完全被 (填“氧化”或“还原”)为 Fe3+.
(2)步骤③所得的红褐色悬浊液中除H2O2、氨水外主要还含 和 (填化学式).
(3)步骤④中一系列处理的操作步骤为 、洗涤、灼烧、冷却、称量.
(4)实验中用已经准确量取的浓硫酸配制100 mL 1 mol/L的硫酸溶液,则配制时用到的仪器除烧杯、玻璃棒,还有两种仪器是 .
(5)若实验无损耗,则每片补血剂含铁元素的质量分数为 .
(6)下列操作会导致所测定的铁元素含量偏高的是
A. 步骤③所加氨水量不足 B. 步骤④洗涤不充分 C. 步骤④灼烧不充分
如图为实验室制取蒸馏水的装置示意图,根据图示回答下列问题。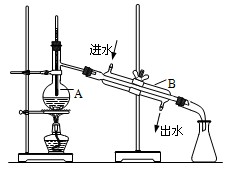
(1)图中有两处明显的错误是
①②
(2)A仪器的名称是B仪器的名称是
(3)实验时A中除加入少量自来水外,还需要加入少量的,其作用是(
下列说法中,正确的是____
| A.选用酒精作为萃取剂从碘水中萃取碘 |
| B.分液操作时,分液漏斗中下层液体从下口放出,上层液体从上口倒出 |
| C.在做蒸馏实验时,冷凝器中的水流方向应该与馏分的流动方向相反 |
| D.蒸发操作时,待蒸发皿中的水分完全蒸干后再停止加热 |
E.分液漏斗使用前不需要检查是否漏水,但需要用蒸馏水润洗2~3次
F.浓硫酸不慎沾在皮肤上,立即用稀氢氧化钠溶液冲洗
G.蒸馏操作时,应使温度计水银球插入蒸馏烧瓶中液面下,但不能接触瓶底
溴乙烷是一种重要的有机化工原料,其沸点为38.4℃。制备溴乙烷的一种方法是乙醇与氢溴酸反应,该反应的化学方程式是
实际通常是用溴化钠与一定浓度的硫酸和乙醇反应。某课外小组欲在实验室制备溴乙烷的装置如图,实验操怍步骤如下:
①检查装置的气密性;
②在圆底烧瓶中加入95%乙醇、80%硫酸,然后加入研细的溴化钠粉末和几粒碎瓷片;
③小心加热,使其充分反应。
请问答下列问题。
⑴装置A的作用是。
⑵反应时若温度过高,则有SO2生成,同时观察到还有一种红棕色气体产生,该气体的分子式是
⑶反应结束后,得到的粗产品呈棕黄色。为了除去粗产品中的杂质,可选择下列试剂中的 _____________(填写上正确选项的字母)。
a.稀氢氧化钠溶液 b.乙醇 c.四氯化碳
该实验操作中所需的主要玻璃仪器是(填仪器名称)。
⑷要进一步制得纯净的溴乙烷,可继续用蒸馏水洗涤,分液后,再加入无水CaCl2,然后进行的实验操作是(填写正确选项的字母)。
a.分液 b.蒸馏 c.萃取
⑸为了检验溴乙烷中含有溴元素,不能直接向溴乙烷中滴加硝酸银溶液来检验,其原因是
通常采用的方法是取少量溴乙烷,然后(按实验的操作顺序选填下列序号)。
①加热②加入AgNO3溶液③加入稀HNO3酸化④加入NaOH溶液
在量热计中(如图)将100 mL 0.50 mol·L-1的CH3COOH溶液与100 mL 0.55 mol·L-1的NaOH溶液混合,温度从298.0 K升高至300.7 K。已知量热计的热容常数(量热计各部件每升高1 K所需要热量)是150.5 J·K-1,溶液密度均为1 g·mL-1,生成溶液的比热容c=4.184 J·(g·K)-1。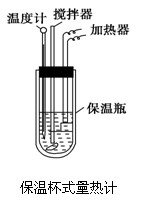
(1).试求CH3COOH的中和热ΔH表达数值式。
(2).上述数值结果与57.3 kJ/mol有偏差,产生原因可能是
a.实验装置保温、隔热效果差
b.配制0.55 mol/L NaOH溶液时俯视刻度线读数
c.分多次把NaOH溶液倒入盛有硫酸的小烧杯中
d.用温度计测定NaOH溶液起始温度后直接测定H2SO4溶液的温度
e.用量筒量取NaOH溶液的体积时仰视读数
某课外兴趣小组对双氧水(H2O2水溶液)做了如下实验探究。
(1)将质量相同但聚集状态不同的MnO2分别加入5mL 5%的双氧水中,并用带火星的木条试之。测定结果如下:
| 催化剂(MnO2) |
操作情况 |
观察结果 |
反应完成所需的时间 |
| 粉末状 |
混合不振荡 |
剧烈反应,使木条复燃 |
3.5分钟 |
| 块状 |
反应较慢,火星红亮但木条未复燃 |
30分钟 |
①写出H2O2反应的化学方程式。
②实验结果说明催化剂作用的大小与有关。
(2)取三份含有等量H2O2,但质量分数不同的双氧水,分别向其中加入1克MnO2粉末。测定结果如下:
| 双氧水体积 |
操作情况 |
反应完成所需的时间 |
收集到气体体积 |
反应后液体温度 |
| a1%的150mL |
11分钟 |
539mL |
24℃ |
|
| a2%的15mL |
混合不振荡 |
1分20秒 |
553mL |
56℃ |
| a3%的7.5mL |
9秒 |
562mL |
67℃ |
请简要说明:
①反应完成所需的时间不同的原因。
②反应后液体温度不同的原因。
③收集到气体体积不同的原因。
(3)向含有酚酞的NaOH稀溶液中,逐滴滴入10%的双氧水,红色褪去。
①已知双氧水显弱酸性,试写出H2O2的电离方程式:。
②小组讨论红色褪去的原因时,甲同学认为是双氧水显酸性所致;乙同学认为是双氧水有较强氧化性所致。请你设计一个简单实验来说明是甲对还是乙对。(简要文字说明)