如图是制取无水氯化铜的实验装置图,将浓盐酸滴加到盛有二氧化锰粉末的圆底烧瓶中。请回答下列问题: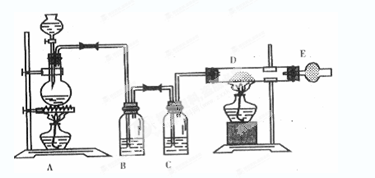
(1)盛放浓盐酸的仪器名称为____;
(2)烧瓶中发生反应的化学方程式 ;
(3)C瓶中的试剂是____;其作用是____;
(4)玻璃管D中发生反应的化学方程式 ;反应现象是___;
(5)干燥管E中盛有碱石灰(CaO+NaOH),其作用是____。
NaCI在生活、生产和科研中都有广泛的用途。
I.从海水中提取的粗盐含有Ca2+、Mg2+、SO42-等离子,为制备精盐可使用以下四种试剂:①Na2CO3溶液②BaCl2溶液③NaOH溶液④盐酸(用于沉淀的试剂均稍过量)。
(1)加入试剂的合理顺序是__________(填选项)。
A.①②③④ B.③①②④ C.②①③④ D.③②①④
(2)加入过量Na2CO3溶液的作用是________。
II.实验室要配制100 mL 0.2 mol NaCl溶液。
NaCl溶液。
(1)用托盘天平称氯化钠固体的质量是______g。
(2)配制溶液需要使用的主要玻璃仪器有烧杯、玻璃棒、胶头滴管和_________。
(3)下列操作中,可能造成所配制溶液的浓度偏低的是________(填选项)。
A.没有洗涤烧杯和玻璃棒 b.定容时,俯视刻度线
C.洗涤后的容量瓶中残留少量蒸馏水
柠檬酸亚铁(FeC6H6O7)是一种易吸收的高效铁制剂,可由绿矾(FeSO4·7H2O)通过下列反应制备:FeSO4+Na2CO3 FeCO3↓+Na2SO4FeCO3+C6H8O7
FeCO3↓+Na2SO4FeCO3+C6H8O7 FeC6H6O7+CO2↑+H2O
FeC6H6O7+CO2↑+H2O
下表列出了相关金属离子生成氢氧化物沉淀的pH(开始沉淀的pH按金属离子浓度为1.0 mol·L-1计算)。
| 金属离子 |
开始沉淀的pH |
沉淀完全的pH |
| Fe3+ |
1.1 |
3.2 |
| Al3+ |
3.0 |
5.0 |
| Fe2+ |
5.8 |
8.8 |
(1) 制备FeCO3时,选用的加料方式是 (填字母)
a.将FeSO4溶液与Na2CO3溶液同时加入到反应容器中
b.将FeSO4溶液缓慢加入到盛有Na2CO3溶液的反应容器中
c.将Na2CO3溶液缓慢加入到盛有FeSO4溶液的反应容器中
(2)生成的FeCO3沉淀需经充分洗涤,检验洗涤是否完全的方法____________________
(3)将制得的FeCO3加入到足量柠檬酸溶液中,再加入少量铁粉,80 ℃下搅拌反应。
①铁粉的作用是 。
②反应结束后,无需过滤,除去过量铁粉的方法是 。
(4)最后溶液经浓缩、加入适量无水乙醇、静置、过滤、洗涤、干燥,获得柠檬酸亚铁晶体。分离过程中加入无水乙醇的目的是 。
(5)某研究性学习小组欲从硫铁矿烧渣(主要成分为Fe2O3、SiO2、Al2O3)出发,先制备绿矾,再合成柠檬酸亚铁。结合下图的绿矾溶解度曲线,完成由烧渣制备绿矾晶体的操作
绿矾溶解度曲线
试剂i_________加入试剂i反应的离子方程式为 ________________________________
操作a为__________________________、____________________、_________________
按以下实验方案可以从海洋动物柄海鞘中提取具有抗肿瘤活性的天然产物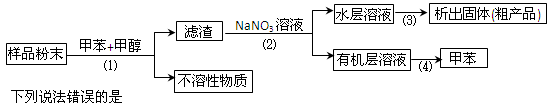
| A.步骤(1)需要过滤装置 | B.步骤(2)需要用到分液漏斗 |
| C.步骤(3)需要用到坩埚 | D.步骤(4)需要蒸馏装置 |
实验题:
I、下列方法适用于实验室中制备氨气的是____________________
A.固态氯化铵加热分解 B.向固体氢氧化钠中滴加浓氨水
C.氯化铵溶液与氢氧化钠溶液共热 D.固体氯化铵与氢氧化钙固体混合加热
II、为了在实验室中利用工业原料制备少量氨气,有人设计了如图所示的装置(图中夹持装置均已略去)。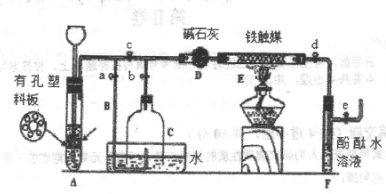
实验操作如下:
①检查装置的气密性后,关闭弹簧夹A.B.C.D.e。在A中加入锌粒,向长颈漏斗注入一定量的稀硫酸。打开弹簧夹C.D.e,则A中有氢气产生。在F出口处收集到氢气并检验其纯度。
②关闭弹簧夹c,取下截去底部的细口瓶C,打开弹簧夹a,将氢气经导管B验纯后点燃,然后立即罩上无底细口瓶C,塞紧瓶塞,如图所示。氢气继续在瓶内燃烧,几分钟后火焰熄灭。
③用酒精灯加热反应管E,继续通入氢气,待无底细口瓶C内水位下降到液面保持不变时,打开弹簧夹b,无底细口瓶C内气体经D进入反应管E,片刻后F中的溶液变红。
请回答下列问题:
(1)写出反应管E中发生反应的化学方程式_______________________________________
用方程式解释F中溶液变红的原因______________________________________________
(2)C瓶内水位下降到液面保持不变时,A装置内发生的现象为____________________________,防止了实验装置中压强过大。此时再打开弹簧夹b的原因是___________________________,,C中气体的主要成分为.__________________________________________.
(3)为什么用酒精灯加热反应管E-段时间后再打开弹簧夹b____________________________
(4)为什么F装置不用防倒吸的装置_________________________________________________
(15分)某研究小组利用下图装置探究铜与浓硫酸反应的产物。
实验步骤与现象如下:
①检查装置气密性,向A中加入5 mL浓硫酸,打开K,将铜丝伸入浓硫酸中,给A处加热,观察到B中品红溶液褪色,再关闭K。
②实验观察到A中液面下铜丝变黑,产生气泡,液面上方产生大量白雾,一段时间后溶液中有白色固体出现,拉出铜丝,停止加热。回答下列问题:
(1)溶液中白色固体是_______ (填化学式),C中CCl4的作用是______________。
(2)取出铜丝,用蒸馏水洗净后伸入到稀硫酸中,铜丝变亮、溶液变蓝。写出A中可能发生反应的化学方程式:_____________________、_____________________。
(3)分离出C中的上层液体,滴加过量稀盐酸和BaCl2溶液,有白色沉淀产生。①分离的操作名称为:______________:②白色沉淀为:______________; ③产生白色沉淀的原因可能是___________________。