以食盐为原料进行生产并综合利用的某些过程如下图所示: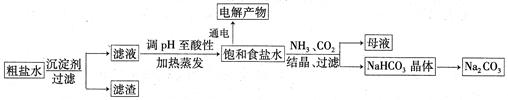
(1)为除去粗盐中的Ca2+、Mg2+和SO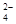 ,得到纯净的NaCl晶体,需加入以下试剂:
,得到纯净的NaCl晶体,需加入以下试剂:
| A.过量的NaOH溶液; | B.过量的Na2CO3溶液; | C.适量的盐酸; | D.过量的BaCl2溶液。 |
正确的加入顺序是_______,还缺少的操作步骤是__________和___________。
(2)将滤液的pH调至酸性除去的离子是________,发生反应的离子方程式为________。
(3)若用惰性电极电解200mL1.5mol/L食盐水,当电解2min时,两极共收集到448mL气体(标准状况下)。假设电解前后溶液的体积不变,则电解后该溶液的pH为______。
(4)若向分离出NaHCO3晶体后的母液中加入过量生石灰,则可获得一种可以循环使用的物质,其化学式是___________。
(5)纯碱在生产生活中有广泛的应用。
①纯碱可用于除灶台油污。其原因是(结合离子方程式表述)_____________。
②常温下,向某pH=11的Na2CO3溶液中加入过量石灰乳,过滤后所得溶液pH=13。则反应前的溶液中与反应后的滤液中水电离出的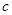 (OH-)的比值是_________。
(OH-)的比值是_________。
A、B、C、D、E、F、G为由七种短周期元素构成的粒子,它们都有10个电子,其结构特点如下表:
| 粒子代号 |
A |
B |
C |
D |
E |
F |
G |
| 原子核数 |
单核 |
单核 |
双核 |
4核 |
单核 |
多核 |
多核 |
| 电荷数 |
0 |
1+ |
1— |
0 |
2+ |
1+ |
0 |
其中,B的离子半径大于E的离子半径;C常用作F的检验(加热)。请填写下列空白:
(1)A粒子的结构示意图。
(2)比较BC和EC2的碱性强弱BCEC2(填<、>、="" )。
(3)F与C反应的离子方程式
已知溴单质的 氧化性介于氯和碘之间,利用这一性质解决下面问题
氧化性介于氯和碘之间,利用这一性质解决下面问题
(1)下列可以氧化Br-微粒是(填序号)。
A.I2 B. I- C.Cl2 D.Cl-
(2)把滤纸用淀粉和碘化钾的溶液浸泡、晾干后可获得实验常用的淀粉碘化钾试纸。这种试纸润湿后遇氯气变化的现象是 ,用化学方程式解释该现象: 。
(3)下列试剂不能把NaCl和KI两种无色溶液区别开的是(填序号)。
A. 氯水 B. 溴水 C. 淀粉溶液
在第3周期中,置换酸中氢的能力最强的元素的元素符号为,化学性质最稳定的元素符号是,最高价氧化物对应的水化物的酸性最强的化合物的化学式是,碱性最强的化合物的化学式是,显两性的氢氧化物的化学式是,该两性氢氧化物与氢氧化钠溶液反 应的离子方程式为,用作半导体材料元素的名称是,离子半径最小的离子结构示意图是
应的离子方程式为,用作半导体材料元素的名称是,离子半径最小的离子结构示意图是
[化学——选修有机化学基础]
柠檬酸三丁酯(TBC)是绿色环保的增塑剂,应用极其广泛,它的结构式如左下图,
已知柠檬酸的结构简式为 ,1—丙醇的键线式可表示为
,1—丙醇的键线式可表示为
试回答:
(1)TBC的分子式为,在研究TBC的结构时要用到一种谱图(如下),用于推测等信息,它是图(填序号);
A.核磁共振氢谱 B.红外光谱 C.质谱
(2)1—丁醇在一定条件下可生成1—丁醇,反应类型为,化学方程式为,TBC在该条件下(填“能”或“不能”)生成含醛基的化合物;
(3)柠檬酸与甲醇反应生成柠檬酸三甲酯的化学方程式;
(4)合成TBC时,不同条件对酯化学率的影响如下表:
| n(酸):n(醇) |
1:5.0 |
1:5.5 |
1:6.0 |
1:6.5 |
1:7.0 |
| 酯化率/% |
95.1 |
96.3 |
97.0 |
97.4 |
97.2 |
| 时间/h |
0.5 |
1.0 |
2.0 |
3.0 |
5.0 |
| 酯化率/% |
40.0 |
70.2 |
94.3 |
97.4 |
97.4 |
| 温度/°C |
130 |
140 |
145 |
150 |
160 |
| 酯化率/% |
89.5 |
96.2 |
97.4 |
97.4 |
97.2 |
酯化反应时应选择的条件如下:它们分别是n(酸):(醇)、时间、温度,其中最佳的是:(填序号)。
A.1:5,1h,130° B.1:5.5,1h,140°C
C.1:7,2h,160°C D.1:6.5,3h,145°C
(5)TBC与足量NaOH溶液反应的化学方程式:。
[化学——选修物质结构与性质]
A、B、C、D是原子序数依次递增的短周期元素,四种元素的质子数之和小于23。
A元素原子的电子总数等于其基态原子的电子层数。B元素原子的价电子结构为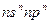 。C元素的第一电离能在同族元素中最大,并且高于同周期左右相邻的元素,但
。C元素的第一电离能在同族元素中最大,并且高于同周期左右相邻的元素,但
其单质的熔点却低于同周期左右相邻元素的单质。D的电负性大于C。
(1)B、C、D分别是、、;
(2)C、D分别与A形成的最简单分子中,稳定性较高的是(填化学式)分子;该分子再与A+结合成离子时,ACA键的键角会发生改变,其原因是。
(3)BD2分子的晶体结构为密堆积,则每个BD2分子周围紧邻的分子有个;
(4)上图为B元素的某种单质晶体X的晶胞,其中含有个B原子,该晶体
(填“形成”或“没有形成”)最密堆积结构,原因是。试分析比较晶体X与晶体BD2的熔点。