某小组同学将一定浓度NaHCO3溶液加入到CuSO4溶液中发现生成了沉淀.甲同学认为沉淀是CuCO3;乙同学认为沉淀是CuCO3和Cu(OH)2的混合物,设计实验测定沉淀中CuCO3的质量分数.
(1)按照甲同学的观点,发生反应的离子方程式为 ;
(2)乙同学认为有Cu(OH)2生成的理论依据是 (用离子方程式表示);
(3)两同学利用下图所示装置进行测定
①组装好仪器后如何检查气密性
在研究沉淀物组成前,须将沉淀从溶液中分离并净化.具体操作依次为 ,洗涤,干燥;
②装置E中碱石灰的作用是 ;
③实验过程中有以下操作步骤:
a.关闭K1,K3,打开K2,K4,充分反应
b.打开K1,K4,关闭K2,K3,通入过量空气
c.打开K1,K3,关闭K2,K4,通入过量空气.
正确的顺序是 (填选项序号,下同);
若未进行步骤 将使测量结果偏低;
④若沉淀样品的质量为m g,装置D的质量增加了n g,则沉淀中CuCO3的质量分数为 ;
实验室需要配制2.0mol·L-1的NaCl溶液500 ml 。
(1) 本实验所必需的仪器有托盘天平(精确到0.1g)、药匙、烧杯、量筒、玻璃棒、胶头滴管、以及等质量的两片滤纸。
(2)某学生在摇匀后发现液面低于刻度线再加水,会导致结果(填“偏高”、“偏低”、“无影响”)。
某化学实验小组的同学为探究和比较SO2和氯水的漂白性,设计了如下的实验装置。
(1)实验室用装置A制备SO2。某同学在实验时发现打开A的分液漏斗活塞后,漏斗液体未流下,你认为原因可能是
(2)实验室用装置E制备Cl2,其反应的化学化学方程式为:MnO2+4HCl(浓) MnCl2+Cl2↑+2H2O请指出该反应中的液体反应物在反应中所表现出的化学性质:
MnCl2+Cl2↑+2H2O请指出该反应中的液体反应物在反应中所表现出的化学性质:
__________________________________________________________________;
(3)①反应开始一段时间后,观察到B、D两个试管中的品红溶液出现的现象是:
B:________________________,D:____________________________。
②停止通气后,再给B、D两个试管分别加热,两个试管中的现象分别为
B:_________________________,D:____________________________。
(4)另一个实验小组的同学认为SO2和氯水都有漂白性,二者混合后的漂白性肯定会更强,他们将制得的SO2和Cl 2按1:1同时通入到品红溶液中,结果发现褪色效果并不像想象那样。请你分析该现象的原因(用化学方程式表示)
2按1:1同时通入到品红溶液中,结果发现褪色效果并不像想象那样。请你分析该现象的原因(用化学方程式表示)
(1)下图为常见仪器的部分结构(有的仪器被放大)A图中液面所示溶液的体积为mL,用上述四种仪器中的某种测量一液体的体积,平视时读数为N mL,仰视时读数为M mL,若M>N,则所使用的仪器是____(填字母标号)。
(2)在化学分析中,常需用KMnO4标准溶液,由于KMnO4晶体在室温下不太稳定,因而很难直接配制准确物质的量浓度的KMnO4溶液。实验室一般先称取一定质量的KMnO4晶体,粗配成大致浓度的KMnO4溶液,再用性质稳定、相对分子质量较大的基准物质草酸钠[Mr(Na2C2O4)=134.0]对粗配的KMnO4溶液进行标定,测出所配制的KMnO4溶液的准确浓度,反应原理为:5C2O42-+2MnO4-+16H+→10CO2↑+2Mn2++8H2O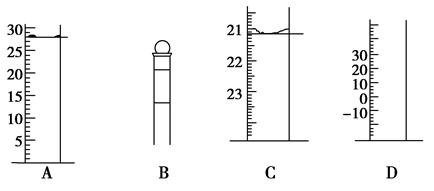
以下是标定KMnO4溶液的实验步骤:
步骤一:先粗配浓度约为0.15mol·L-1的高锰酸钾溶液500 mL。
步骤二:准确称取Na2C2O4固体m g放入锥形瓶中,用蒸馏水溶解并加稀硫酸酸化,加热至70~80℃,用步骤一所配高锰酸钾溶液进行滴定。记录相关数据。
步骤三:。
步骤四:计算得高锰酸钾的物质的量浓度。试回答下列问题:
①该滴定实验(“需要”或“不需要”)加指示剂。
②步骤二中滴定操作图示正确的是__________(填编号)。
③步骤二的滴定过程温度变化并不明显,但操作过程中发现前一阶段溶液褪色较慢,中间阶段褪色明显变快,最后阶段褪色又变慢。试根据影响化学反应速率的条件分析,溶液褪色明显变快的原因可能是_______,最后又变慢的原因是。④请写出步骤三的操作内容。⑤若m的平均数值为1.340g,滴定的KMnO4溶液平均用量为25.00mL,则KMnO4溶液的浓度为mol·L-1。
请回答有关下列五种气体:H2、O2、NO、NH3、NO2的问 题。
I.(1)与制取O2的发生装置相同的是;______________只能用一种方法收集的是______________________________
(2)以上气体制备反应中,有一反应在原理上与其它反应都不能归为同一类型,请写出实验室制取该气体的方程式_________________________________
II. 用右图装置进行喷泉实验(图中夹持装置均已略去)。
(1)若用图1装置进行喷泉实验,上部烧瓶已装满干燥的氨气,引发水上喷的操作是_____________________该实验的原理是______________________________________
(2)若用图2的装置,请举一例说明引发喷泉的方法___________________________
III:若用同一烧瓶分别充满如下气体:① HCl② NH3③ NO2进行喷泉实验,实验后烧瓶内溶液液面的高度关系为____________________________ (用序号和“>,<或=”表示,下同),所得溶液物质的量浓度大小关系为 ____________________________ 。
(5分)实验室用氢氧化钠固体配制l00 mL 2 mol·L-1的NaOH溶液,回答下列问题:
(1)配制操作中,用不到的仪器是(填字母)。
A.烧杯 B.200 mL容量瓶 C.量筒 D.胶头滴管
E.玻璃棒 F.100 mL容量瓶
(2)下列操作的顺序是(每项限选一次)。
A.称量 B.溶解 C.洗涤 D.定容 E.转移 F.摇匀 G.冷却
(3)(以下小题填“偏大”、“偏小”或“无影响”)
若容量瓶中有少量蒸馏水,所配溶液的浓度将;
若用2 mol·L-1的NaOH溶液先润洗容量瓶,再转移溶液,所配溶液的浓度将。