已知:Cu+2Fe3+=Cu2++2Fe2+;Zn+2Fe3+=2Fe2++Zn2+。现将等物质的量的CuSO4、FeCl3和Zn于水中充分反应,所得混合物中除了SO42—、Cl—外,还含有( )
| A.Zn2+、Fe3+、Cu | B.Cu2+、Fe3+、Zn |
| C.Zn2+、Cu2+、Fe2+、Fe | D.Zn2+、Fe2+、Cu2+、Cu |
下列图象能正确表示相关反应中产物物质的量的变化的是()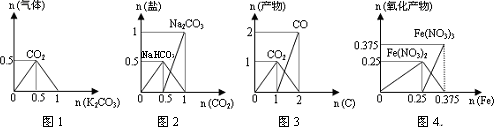
(横、纵坐标单位:mol)
| A.图1:n(HCl)=1mol,K2CO3逐步加入到HCl溶液中,在敞口容器中生成的气体 |
| B.图2:n(NaOH)=1mol,CO2逐步通入到NaOH溶液中反应生成的盐 |
| C.图3:n(O2)=1mol,高温下C和O2在密闭容器中的反应产物 |
| D.图4:n(HNO3)=1mol,Fe和稀HNO3反应生成的氧化产物(还原产物为NO) |
水热法制备Fe3O4纳米颗粒的反应是3Fe2++2S2O +O2+xOH—
+O2+xOH—Fe3O4+S4O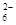 +2H2O,
+2H2O,
下列说法中,正确的是()
| A.每生成1mol Fe3O4,反应转移的电子总数为3mol ; |
| B.x="6" |
| C.1mol Fe2+被氧化时,被Fe2+还原的O2的物质的量为1/3mol; |
| D.Fe2+和S2O32—-都是还原剂; |
常温下,下列各组离子在指定溶液中一定能大量共存的是()
| A.1.0 mol·L-1的KNO3溶液:H+、Fe2+、Cl-、SO42- |
| B.饱和氯水中:NH4+、SO32-、AlO2-、Cl- |
| C.与铝反应产生大量氢气的溶液:Na+、K+、CO32-、NO3- |
| D.c(H+)=1.0×10-13mol/L溶液中:K+、Na+、CH3COO-、Br- |
实验用含有杂质(FeO、Fe2O3)的废CuO制备胆矾晶体经历下列过程,Fe3+在PH=5时已完全沉淀,其分析错误的是()
| A.若要用实验测定所得硫酸铜晶体中结晶水的数目要用到坩埚和坩埚钳。 |
| B.利用Cu(OH)2替代CuO也可调试溶液pH不影响实验结果; |
| C.洗涤晶体:向滤出晶体的漏斗中加少量水浸没晶体,自然流下,重复2-3次; |
| D.用18mol/L浓硫酸配制溶解所用4mol/L的稀硫酸,玻璃仪器一般只有3种; |
下列过程中,最终的白色沉淀不一定是BaSO4的是()