含氯消毒剂和过氧化物等强氧化性消毒剂可防甲型H1N1流感。
(1)过碳酸钠是一种有多种用途的新型氧系固态漂白剂,化学式可表示为Na2CO3·3H2O2,它具有Na2CO3和H2O2的双重性质。
①H2O2有时可作为矿业废液消毒剂,如消除采矿业废液中的氰化物(如NaCN),经以下反应实现:NaCN+H2O2+H2O=A+NH3↑,则生成物A的化学式______________
②某强酸性反应体系中,反应物和生成物共六种物质:
O2、MnO4-、H2O、Mn2+、H2O2、H+。已知该反应中H2O2只发生了如下过程:H2O2→ O2。
写出该反应的离子方程式:_______________________________________________。
(2)某天然碱的化学式可表示为:aNa2CO3·bNaHCO3·2H2O,取m g天然碱溶于水配成溶液,再向溶液中逐滴加入1 mol/L的盐酸,标准状况下产生的CO2的体积与所加盐酸体积之间的关系某同学作出了如图所示的A和B曲线,试回答下列问题: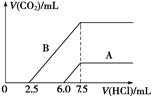
①_______曲线正确,天然碱的化学式为___________,
②加盐酸后产生CO2气体体积(标准状况)的最大值为 _____________mL。
(3) 常温下用氧缺位铁酸锌ZnFe2Oy可以消除NOx污染,使NOx转变为N2,同时ZnFe2Oy转变为ZnFe2O4。若2 mol ZnFe2Oy与足量NO2可生成0.5 mol N2,则y=_______________。
(10分)Ⅰ、可逆反应:aA(g) + bB(g)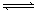 cC(g) + dD(g);根据图回答:
cC(g) + dD(g);根据图回答: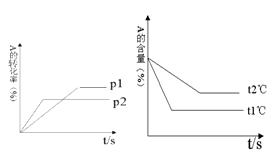
①压强 P1P2;(a +b)(c +d)(填“>”或“<”下同)。
②温度t1℃t2℃;△H0。
③保持体积和温度不变,通入He,平衡会____移动(填“正向”、“逆向”或“不”)。
Ⅱ、写出下列元素基态原子的电子排布式:
①29Cu
②32Ge(简式)
(11分)(1)常温下,0.10 mol·L-1 NH4Cl溶液pH______7(填“>”、“=”或“<”)。
(2)相同物质的量浓度的Na2CO3溶液与NaHCO3溶液,pH大小:Na2CO3________NaHCO3(填“>”、“=”或“<”)。
(3)在配制FeCl3溶液时,应加入__________,目的是_____________。
(4)Na2S溶液中滴入酚酞溶液显______色,原因是__________________。(用离子方程式表示),
(5)将氯化铝溶液蒸干并灼烧得到的固体物质是;(填化学式,下同)将硫酸铝溶液蒸干得到的固体物质是。
(10分)Ⅰ、在A、B、C三个烧杯中分别盛有相同浓度的稀硫酸,如图所示:
①A中反应的离子方程式为:_______________________________。
②B中Sn极附近溶液的pH________(填“增大”、“减小”或“不变”)。
③比较A、B、C中铁被腐蚀的速率,由快到慢的顺序是________________。
Ⅱ、如图所示,甲、乙两池电极材料都是铁棒和碳棒,请回答下列问题: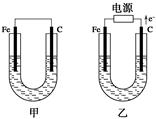
(1)若两池中电解质溶液均为CuSO4溶液,则反应一段时间后:
①有红色物质析出的是甲池中的________棒。
②乙池中阳极的电极反应式是___________________。
(2)若两池中电解质溶液均为饱和NaCl溶液:
①甲池中碳棒上电极反应式是_____________________,
②乙池电解一段时间后,测知溶液体积为200ml,PH=13,则阴极生成的气体在标准状况下体积是______L。
有一包白色粉末,可能是CuSO4、CaCO3、BaCl2、Na2SO4、KOH中的一种或几种,为证明其组成,进行如下实验:
(1)取少量白色粉末,向其中加入足量的水,充分搅拌后过滤,得到白色沉淀和无色滤液,则白色沉淀可能是,原混合物中一定不含有;
(2)向实验(1)滤出的白色沉淀中加入足量的盐酸,沉淀全部溶解,并产生无色气体。则原混合物中一定含有。 该反应的离子方程式为;
(3)将实验(1)中得到的滤液分成两份,将实验(2)中产生的无色气体先通入其中的一份,无沉淀产生。气体导出后再通入另一份滤液中,立即产生白色沉淀,再过滤。出现上述现象的原因是实验(2)中产生的气体里含有 。
(4)向实验(3)中过滤后所得的滤液里加入AgNO3溶液和稀硝酸,又产生白色沉淀,根据此现象推断,原混合物中一定还含有,根据实验全过程推断,原混合物中还含有。
某学生为了测定由两种元素形成的气态化合物X的组成,进行了如图所示的实验,将装置内空气排尽后,把气体X由注射器A缓慢送入装有CuO的B装置,使之完全反应(气态化合物X与CuO均无剩余),得到如下结果: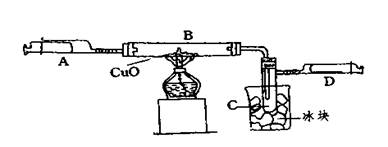
①实验前B管及药品的质量为21.32克,实验后为21.16克
②C管中收集到的物质电解后可得到H2和O2,在D中收集到的是N2。
③X中两元素的质量比是14:3。问:
(1)C中收集到的液体,物质的量是mol;
(2)在实验中看到的现象是。
(3)B中反应的化学方程式是。