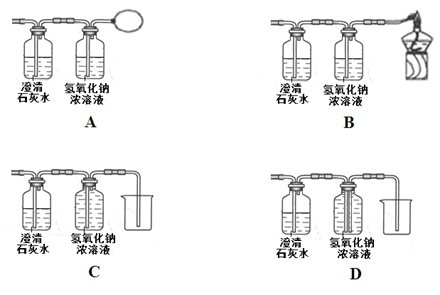
化学是以实验为基础的自然科学,通过实验现象的观察和分析得到结论。结合下列实验回答问题。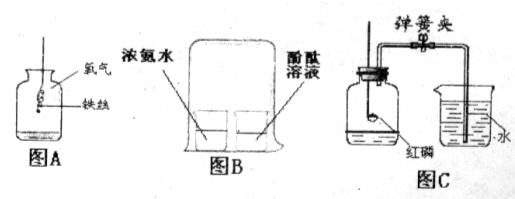
图A所示实验集气瓶中的现象是:铁丝在氧气中剧烈燃烧,__________,放出大量的热,有黑色固体生成,该反应的符号表达式是_____________。
图B所示实验可观察到酚酞溶液由________色变为__________色,该实验中没有涉及的性质是_________(填字母)。
A.氨分子是不断运动的 B.氨分子有一定质量 C.浓氨水具有挥发性
图C所示实验用于测定空气中氧气的含量。红磷在空气中燃烧的符号表达式是______________,关于该实验的下列说法中正确的是__________(填字母)。
A.实验时红磷一定要足量 B.点燃红磷前先用弹簧夹夹紧乳胶管
C.红磷熄灭后立刻打开弹簧夹 D.最终进入瓶中水的体积约为氧气的体积
E. 该实验必须检查装置的气密性
某同学在电视寻宝节目中,看到一些铜制文物上有绿色的锈迹,并对绿色锈迹产生了探究兴趣。
【查阅资料】①绿色锈迹是碱式碳酸铜[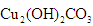 ],受热易分解。
],受热易分解。
②无水硫酸铜为白色粉末,遇水变蓝。
③碱石灰是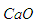 和
和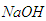 的固体混合物,
的固体混合物,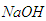 与
与 反应生成碳酸钠固体和水。
反应生成碳酸钠固体和水。
④氧化铜与稀硫酸反应生成蓝色溶液,碳粉不与稀硫酸反应也不溶解在稀硫酸中。
【发现问题】
查阅资料后,该同学将少量碱式碳酸铜放入试管中加热,发现试管中的固体由绿色变成黑色,同时试管壁
上有无色液滴生成。为了进一步确定碱式碳酸铜受热分解的产物,进行了如下探究:
探究一:碱式碳酸铜受热分解生成的黑色固体的成分。
【猜想与假设】该黑色固体可能是①碳粉;② ;③碳和氧化铜的混合物。
【设计方案】请帮助该同学完成下述实验报告。
| 实验操作与现象 |
实验结论 |
| 猜想②正确 |
探究二:碱式碳酸铜受热分解还会生成CO2和H2O。
【进行实验】选择如下图所示装置进行验证。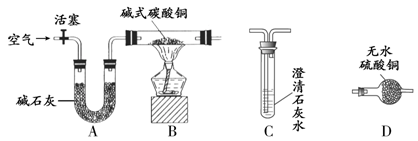
步骤一:连接A和B,打开活塞,通入一段时间的空气。
步骤二,关闭活塞,依次连接装置A→B→ → (填“C”、“D”)。
步骤三:点燃酒精灯,观察到明显现象后,停止加热。
【解释与结论】
①当观察到 ,说明碱式碳酸铜受热分解生成了 和
和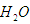 ,写出C中反应的化学方程式 。
,写出C中反应的化学方程式 。
②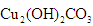 受热分解的化学方程式 。
受热分解的化学方程式 。
【反思与评价】
上述装置中A的作用是 。
“滴水生火”魔术:向包有淡黄色过氧化钠(Na2O2)粉末的脱脂棉上滴加水,脱脂棉随即燃烧。某同学对该“魔术”很感兴趣,设计实验进行探究。
【提出问题】过氧化钠与水反应生成什么物质?脱脂棉为什么会燃烧?
【实验1】取一支干燥的大试管,加入少量过氧化钠粉末,滴加蒸馏水,观察到试管内发生剧烈反应,产生大量气泡,用手触摸,试管底部发烫。
【提出猜想】生成的气体产物可能是:① ;② 。
【实验2】为探究气体产物,进一步设计并完成如下实验。
请完成表中空格:
| 操作 |
现象 |
结论 |
| 将带火星的木条伸入试管 |
带火星的木条复燃 |
气体产物是 |
【查阅资料】脱脂棉是经过化学处理去掉脂肪的棉花,极易燃烧;过氧化钠与二氧化碳反应生成碳酸钠和氧气。
【实验结论】
①过氧化钠与水的反应是 反应(填“吸热”或“放热”)。
②脱脂棉燃烧的原因 。
③扑灭由过氧化钠引发的火灾时,可以选择的灭火材料是 。
A.二氧化碳B.水C.沙子
《蜡烛的化学史》是英国科学家法拉第所著的传世科普经典,今天我们沿着大师的足迹进行探究.蜡烛是由石蜡和棉线组成的.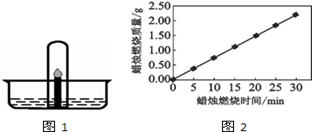
(1)石蜡放入水中,浮在水面上,说明石蜡的密度比水的密度(填“大”或“小”).
(2)点燃蜡烛在其燃烧过程中,属于物理变化的是.
(3)取一火柴梗,拿住一端迅速平放入火焰中约1秒后取出,可观察到两端变黑,中间无明显变化.说明火焰的(填“外焰”“内焰”或“焰心”)部分温度最高.
(4)轻轻一吹即可使蜡烛熄灭,原因是(填序号).
A.降低石蜡的着火点
B.隔绝了空气
C.温度降到了着火点以下.
(5)点燃一根直径为4cm的蜡烛,观察到烛芯周围有一杯状的烛油.蜡烛燃烧的质量与燃烧的时间呈现如图2所示的关系.
①据图判断蜡烛燃烧的化学反应速率是(选填“稳定”或“不稳定”)
②烛芯周围的烛油没能发生燃烧的原因是.
③事实上,人的呼吸与蜡烛的燃烧在某些化学原理论,人的呼吸与蜡烛的燃烧在某些化学原理上相似,请写出其中的一点.
实验室有一瓶长期暴露在空气中的氢氧化钠固体样品,观察发现,样品表面有白色粉末。某兴趣小组的同学对该样品的成分及含量进行了探究。
【提出问题1】该样品中含有那些物质?
【提出猜想】通过分析,提出如下猜想:
猜想Ⅰ:全部是NaOH猜想Ⅱ:已完全变质,该样品中只含Na2CO3;
猜想Ⅲ:部分变质,该样品中含有①。
【查阅资料】CO2在饱和碳酸氢钠溶液中几乎不溶解。
【实验探究1】为确定该样品的成分,小明设计了如下实验方案,请你一起完成下列实验报告。
| 实验操作 |
实验现象 |
实验结论 |
| 1)取少量样品溶于水,加入② |
白色沉淀产生 |
该反应的化学方程式:③ 氢氧化钠已经变质 |
| 2)将上述反应后的混合物过滤,取滤液加入④ |
⑤ |
证明猜想Ⅲ正确 |
回答下列问题
(1)实验室中,氢氧化钠固体应怎样保存?⑥
(2)用酚酞试液⑦(填“能”或“不能”)检验氢氧化钠变质。
(3)若取少量的固体溶于水, 滴加几滴稀盐酸,没有气泡产生。__⑧___(填“能”或“不能”)证明氢氧化钠固体没有变质。
【提出问题2】如何测量该部分变质样品中碳酸钠的质量分数?
【实验探究2】小红同学设计如图所示装置(铁架台略去),实验在20℃,101kPa下进行,步骤如下: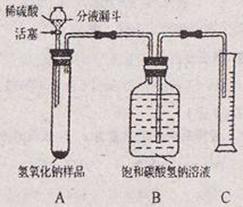
①按图连接好装置;
②检查装置气密性
③用托盘天平准确称取该样品2g,放入A中试管内,向B中集气瓶中倒入饱和碳酸氢钠溶液至瓶颈处;
④向分液漏斗中加入稀硫酸,打开活塞,让稀硫酸滴入试管中至过量,关闭活塞。反应结束后,量筒中收集到饱和碳酸氢钠溶液224mL。
请回答下列问题:
(1)B中集气瓶盛放的饱和碳酸氢钠溶液不能用水代替,其理由⑨
(2)试管中原有的空气对实验结果没有明显影响理由是⑩
(3)变质氢氧化钠样品中碳酸钠的质量分数为⑪(20℃,101kPa下,22.4L二氧化碳的质量为44g)
【拓展提高】已知Na2CO3溶液与稀硫酸反应先生成NaHCO3,当Na2CO3全部转化为NaHCO3后,生成的NaHCO3能继续与稀硫酸反应生成CO2。现向样品中加一定量的稀硫酸,反应后产生无色气体并得到X溶液。请分析推断反应后所得X溶液的溶质,其所有的可能组成Na2SO4和NaHCO3、⑫、。
某化学兴趣小组用下图装置完成木炭还原氧化铜的实验,并对生成的红色固体成分进行探究。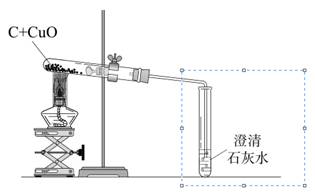
【提出问题】木炭与氧化铜反应生成的红色固体中含有什么物质?
【查阅资料】木炭与氧化铜反应也可能生成氧化亚铜(Cu2O);氧化亚铜是红色固体,能与稀硫酸反应:Cu2O+H2SO4 Cu+CuSO4+H2O。
Cu+CuSO4+H2O。
【进行猜想】木炭与氧化铜反应生成的红色固体成分:
①全部是铜; ②全部是; ③是两者的混合物。
【实验探究】
(1)用上图装置完成木炭还原氧化铜的实验,观察到澄清石灰水。
(2)试管冷却后,观察到黑色固体全部变为红色,对生成的红色固体成分进行探究:
| 步 骤 |
现 象 |
结 论 |
| ①取1.8g红色固体于试管中, 滴加足量,充分反应 |
猜想①错误 |
|
| ②过滤,将滤渣洗涤、干燥、称量 |
所得固体质量 |
猜想③正确 |
【反思与评价】木炭还原氧化铜的实验中,生成的气体可能含有一氧化碳,为了防止对空气造成污染,可将上图虚线方框内的装置改为(选填字母)。