已知:A为常见的短周期轻金属,含A的合金材料常用于火箭、飞机等制造业;B是一种盐,在工农业生产中用途较广;C、F、H为常见非金属单质;常温下C、F、I、E、J和K为气体;E对空气的相对密度为0.586;常温常压下G为液体。有关物质间的转化关系如下(图中部分反应物或产物已省略):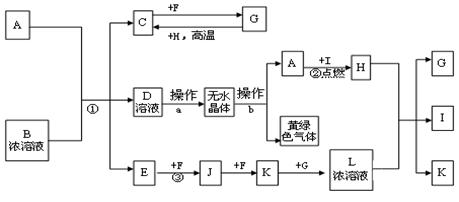
请填空:
(1)B的化学式为 。
(2)操作a必须在HCl气流中加热得无水物而不能直接加热浓缩,其原因是 ;操作b为 。
(3)反应①的离子反应方程式为 。反应③的化学反应方程式为 。
水是一种重要的自然资源,是人类赖以生存不可缺少的物质,水质优劣直接影响人体健康。请回答下列问题:
(1)某贫困山区,为了寻找合适的饮用水,对山上的泉水进行了分析化验,结果显示水中主要含钙离子、镁离子、氯离子和硫酸根离子。则该硬水属于____(填“暂时”、“永久”)硬度,若要除去Ca2+、Mg2+,可以往水中加入石灰和纯碱,试剂加入时先加______后加___。
(2)我国规定饮用水的硬度不能超过25度。硬度的表示方法是:将水中的Ga2+和Mg2+都看作Ca2+,并将其折算成CaO的质量,通常把l升水中含有10mg CaO称为1度。某化学实验小组对本地区地下水的硬度进行检测,实验过程如下:
实验中涉及的部分反应:M2+(金属离子)+EBT-(铬黑T)= MEBT+
蓝色酒红色
M2+(金属离字)+Y4-(EDTA):MY2-
MEBT++Y4-(EDTA)=MY2-+ EBT-(铬黑T)
①取地下水样品25.00进行预处理。写出由Mg2+引起的暂时硬度的水用加热方法处理时所发生反应的化学方程式。
②预处理的方法是向水样中 加入浓盐酸,煮沸几分钟,煮沸的目的是。
加入浓盐酸,煮沸几分钟,煮沸的目的是。
③将处理后的水样转移到250mL的锥形瓶中,加入氨水一氯化铵缓冲溶液调节pH为10,滴加几滴铬黑T溶液,用0.01000·L-1的EDTA标准溶液进行滴定,滴定时眼睛应__ __,滴定终点时的实验现象是
__,滴定终点时的实验现象是 。
。
④滴定终点时共消耗EDTA溶液15.00mL,则该地下水的硬度=。
⑤若实验时装有EDTA标准液的滴定管只用蒸馏水润洗而未用标准液润洗,则测定结果将
(填“偏高”、“偏低”或“无影响”)
某反应中反应物与生成物有:FeCl2、FeCl3、CuCl2、Cu。
(1)已知FeCl3在反应中得到电子,则该反应的还原剂是。
(2)将上述反应设计成的原电池如图甲所示,请回答下列问题:
①电解质溶液X是;
②Cu电极上发生的电极反应式为;
③原电池工作时,盐桥中的离子(填“K+”或“Cl—”)不断进入X溶液中。
(3)将上述反应设计成的电解池如图乙所示,乙烧杯中金属阳离子的物质的量与电子转移的物质的量的变化关系如图丙,请回答下列问题: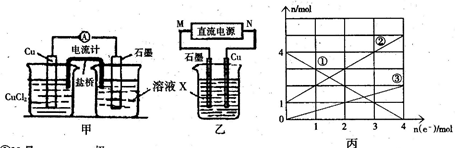
①M是极;
②图丙中的②线是____离子的变化。当电子转移为2mol时,向乙烧杯中加入L 5mol·L-1NaOH溶液才能使所有的金属阳离子沉淀完全。
现有某金属硝酸盐化学式为M(NO3)2,为了探究其热分解产物,某化学小组开展探究性学习:
金属活泼性不同,其硝酸盐分解产物不同。如 :2KNO3
:2KNO3 2KNO2+O2↑
2KNO2+O2↑
2Cu(NO3)2 2CuO+4NO2↑+O2↑,2AgNO3
2CuO+4NO2↑+O2↑,2AgNO3 2Ag+2NO2↑+O2↑
2Ag+2NO2↑+O2↑
猜想1:M(NO3)2 M(NO2)2+O2↑
M(NO2)2+O2↑
猜想2:2M(NO3)2 2MO+4NO2↑+O2↑
2MO+4NO2↑+O2↑
猜想3:(此处不写)。
为了探究上述猜想,设计如下实验装置:
实验步骤:①连接仪器;②检查装置气密性;③取一定量的样品装于大试管中,并重新连接好仪器;④加热;⑤……
(1)写出猜想3的化学方程式: ;
;
(2)测定气体体积应选择(填A或B);
(3)实验收集到一定量气体,为了检验收集到的气体的成分,其操作方法是;
(4)在实验后的水里加入适量碳酸氢钠粉末,溶液中产生大量气体,说明正确(填:猜想l、猜想2或猜想3);
(5)该小组测得一组数据:实验前样品质量为Wg,收集到气体体积为VL(已折算成标准状况 ),则M的相对原子质量为____;
),则M的相对原子质量为____;
(6)已知4Fe(NO3)2 2Fe2O3+8NO2↑+O2↑,现在对KNO3、Cu(NO3)2、Fe(NO3)2的混合粉末充分加热后未收集到任何气体,则KNO3、Cu(NO3)2、Fe(NO3)2的物质的量之比可能是()
2Fe2O3+8NO2↑+O2↑,现在对KNO3、Cu(NO3)2、Fe(NO3)2的混合粉末充分加热后未收集到任何气体,则KNO3、Cu(NO3)2、Fe(NO3)2的物质的量之比可能是()
A.1:2:2 B.2:1:4 C.1:2:3 D.3:8:6
A、B、C、D是短周期元素形成的四种气体单质,其它物质为化合物。H常作为普通锌锰干电池的电解质。有关的转化关系如下图所示(反应条件均已略去)。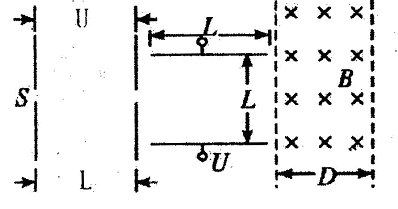
请回答下列问题:
(1)B的结构式为____,G的化学式为。
(2)Y和E在一定条件下可反应生成B和Z,该反应的化学方程式为。
(3)在体积为0.5L的恒容密闭容器中,充人1.25molB和1.25molD进行如下化学反应:
B(g)+3D(g) 2Y(g),其化学平衡常数K与T的关系如下表所示:
2Y(g),其化学平衡常数K与T的关系如下表所示:
| T/℃ |
300 |
400 |
| K |
3.41 |
0.50 |
①若反应在400℃下进行,下列各项中能作为判断该反应达到化学平衡状态依据的是
(填字母)。
A.Y、B、D的物质的量分别为0.50mol、l.0mol、0.50mol
B.v正(B)=" 3v" 逆(D)
C.容器内压强保持不变
D.混合气体的密度保持不变
②在一定条件下B(g)+3D(g) 2Y(g)达到平衡状态,时间为t
2Y(g)达到平衡状态,时间为t 1时改变条件。化学反应速率与反应时间的关系如图。下列说法中正确的是()
1时改变条件。化学反应速率与反应时间的关系如图。下列说法中正确的是()
A.维持温度、反应体系体积不变,t1时充入Y(g)
B.维持压强不变,tl时升高反应体系温度
C.维持温度不变,t1时扩大反应体系体积
D.维持温度、压强不变,t1时充入Y(g)
(4)0.lmol·L-1的X溶液和0.2mol·L-1的Y溶液等体积混合后显碱性,则该混合溶液中各离子浓度大小顺序是.
(5)常温下,0.1mol·L-1的Y溶液中 =l×10-8,下列叙述中错误的是()
=l×10-8,下列叙述中错误的是()
A.该溶液的pH="11"
B.该溶液中的溶质电离出的阳离子浓度为0.1mol·L-1
C.该溶液中水电离出的c(H+)与c(OH—)乘积为l×10-22
D.pH=l的X溶液V1L与0.1mol·L-1的Y溶液V2L混合,若混合溶液pH =7,则V1<V2
E.将0.1mol·L-1的Y溶液加水稀释100倍后,pH >9
芳香族化合物A只有两个对位取代基,在一定条件下有如下图所示转化关系。其中,1 mol C与Na完全反应生成1 mol H2,若1 mol C与NaHCO3完全反应,也产生1 mol气体,E可以使溴的四氯化碳溶液褪色。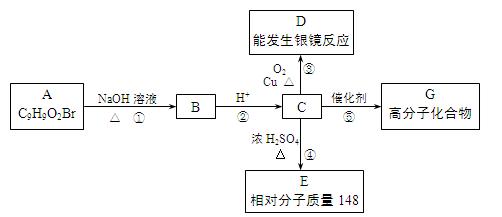
(1)D分子中的含氧官能团名称是,A的结构简式是。
(2)反应④的基本类型是反应,反应⑤的化学方程式是
。
(3)与C取代基位置相同,既能与FeCl3溶液显色、又能发生水解反应的同分异构体结构简式为: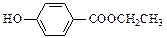 、
、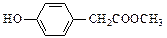 、
、
。
(4)现有C和 E的混合物nmol,在空气中完全燃烧消耗O2 L(标准状况),若生成CO2aL(标准状况)、H2Obg,则C、E混合物中含E的物质的量的计算式为:。
E的混合物nmol,在空气中完全燃烧消耗O2 L(标准状况),若生成CO2aL(标准状况)、H2Obg,则C、E混合物中含E的物质的量的计算式为:。