氧氮杂是新药研制过程中发现的一类重要活性物质,具有抗惊厥、抗肿瘤、改善脑缺血等性质。下面是某研究小组提出的一种氧氮杂化合物H的合成路线:
 在核磁共振氢谱图中,特征峰的数目反映了有机分子中氢原子化学环境的种类;不同特征峰的强度比(及特征峰的高度比)反映了不同化学环境氢原子的数目比。
在核磁共振氢谱图中,特征峰的数目反映了有机分子中氢原子化学环境的种类;不同特征峰的强度比(及特征峰的高度比)反映了不同化学环境氢原子的数目比。
完成下列填空:
(1)原料A的同分异构体中,含有苯环、且核磁共振氢谱中有4个峰的是_________(写出其结构简式)。
(2)反应②的化学方程式是_____________________________________________________。
(3)③的反应类型是_____________。原料D中含有的官能团名称是___________________。
(4)原料B俗名“马莱酐”,它是马莱酸(顺丁烯二酸: )的酸酐,它可以经下列变化分别得到苹果酸(
)的酸酐,它可以经下列变化分别得到苹果酸( )和聚合物Q:
)和聚合物Q:
反应II的化学方程式:_______________________________________________。
(5)符合下列条件的中间产物F的同分异构体数目是_________,写出其中任意一种的结构简式________________________。
①能发生银镜反应;②分子中含有三取代的苯环结构,其中两个取代基是-COOCH3和CH3CO-,且二者处于对位。
Cl2是一种重要的化工原料,下图是一些含氯产品。
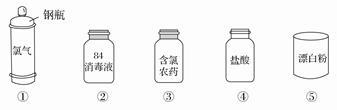
(1)①中钢瓶上应贴的标签为_____________。
A.腐蚀品 B.爆炸品 C.有毒品 D.易燃品
(2)下列有关漂白粉和漂白液的说法正确的是___________。
A.漂白粉是纯净物,漂白液是混合物
B.漂白粉的有效成分是Ca(ClO)2
C.工业上将氯气通入澄清石灰水制取漂白粉
D.漂白液的有效成分是Na2O2
(3)工业上利用Cl2制盐酸,其化学方程式为____________________________。Cl2溶于水可制得氯水,检验一瓶氯水是否已经完全变质,可选用的试剂是_____________。
A.硝酸银溶液 B.酚酞溶液 C.碳酸钠溶液 D.紫色石蕊溶液
(4)将8.7 g MnO2与足量浓盐酸混合加热,反应生成氯气的体积(标准状况)是_________L;被氧化的HCl的质量是_____________g。
(5)下图是实验室用KMnO4与浓盐酸制取适量氯气的简易装置。
装置B、C、D的作用分别是:
B____________________________;
C____________________________;
D____________________________。
工业上常用铁质容器盛装冷浓硫酸。为研究铁质材料与热浓硫酸的反应,某学习小组进行了以下探究活动:
(1)将已去除表面氧化物的铁钉(碳素钢)放入冷浓硫酸中,10分钟后移入硫酸铜溶液中,片刻后取出观察,铁钉表面无明显变化,其原因是__________。
(2)另称取铁钉6.0 g放入15.0 mL浓硫酸中,加热,充分应后得到溶液X并收集到气体Y。
①甲同学认为X中除Fe3+外还可能含有Fe2+。若要确认其中的Fe2+,需进行的实验是__________。
②乙同学取336 mL(标准状况)气体Y通入足量溴水中,发生反应:
SO2+Br2+2H2O=2HBr+H2SO4
然后加入足量BaCl2溶液,经适当操作后得干燥固体2.33 g。由此推知气体Y中SO2的体积分数为(简要表述计算过程)__________。
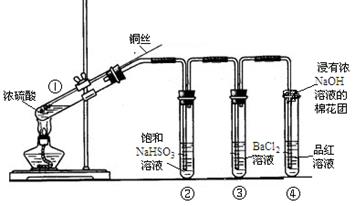
下图为铜丝与浓硫酸反应并验证其产物性质的实验装置。
|
| 加入试剂 |
现象 |
反应的离子方程式 |
|
| 第一份 |
加入NaOH溶液 |
有白色沉淀生成 |
____________ |
| 第二份 |
加入氯水 |
有白色沉淀生成 |
____________ |
完成上述反应的离子方程式。
(4)④中棉花团的作用是 。
(5)上述实验结束后,发现①中试管内有少量白色固体出现,冷却后将试管中的物质缓缓倒入水中,溶液呈蓝色。取少量蓝色溶液于试管中,滴加NaOH溶液至过量,出现的现象是 。
某混合物A,含有KAl(SO4)2、Al2O3和Fe2O3,在一定条件下可实现下图所示的物质之间的变化: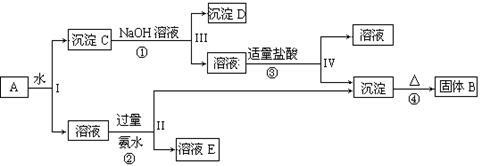
据此回答下列问题:
(1)I、II、III、IV四步中对于溶液和沉淀的分离采取的方法是 。
(2)根据上述框图反应关系,写出下列B、D所含物质的化学式
固体B ;沉淀D 。
(3)写出①、②反应的离子方程式:
① ;② ;
(4)以Fe2O3为原料,可制备FeCl2溶液,请写出有关的化学反应方程式,试剂任选。
Ⅰ.实验室配制1mol/L Na2CO3溶液250mL。
(1)需要固体Na2CO3 g;
(2)该溶液中的阳离子数目为 个;
(3)需要物质的量浓度为5mol/L 的Na2CO3溶液 mL;
(4)将该溶液与足量稀硫酸反应,产生的气体在标准状况下的体积为 L。
(5)用固体Na2CO3配制该溶液的操作顺序是(用字母表示,不重复使用) 。
| A.称量 | B.洗涤 | C.定容 | D.溶解 E.摇匀 F.转移 |
(6)没有洗涤这步操作,所配制的溶液浓度 (填偏大、偏小或无影响)
Ⅱ.(4分)在25℃、101kPa条件下,将15L O2通往10L CO和H2的混合气中,使其完全燃烧,干燥后,恢复至原来的温度和压强。
(1)若剩余气体的体积是15L,则原CO和H2的混合气体中,V(CO)= L,V(H2)= L。
(2)若剩余气体的体积为a L,则原CO和H2的混合气中,V(CO): V(H2)= 。