氧氮杂卓是新药研制过程中发现的一类重要活性物质,具有抗惊厥、抗肿瘤、改善脑缺血等性质。下面是某研究小组提出的一种氧氮杂卓类化合物H的合成路线:
(1)原料A的同分异构体中,含有苯环且核磁共振氢谱中有5个峰的结构简式为 ,
写出该物质催化氧化反应的化学方程式 。
(2)②的反应类型是 。原料D中含有的官能团名称是 、 。
(3)写出符合下列条件的中间产物F的同分异构体的结构简式 。
(i) 能发生银镜反应;
(ii) 分子中含有三取代的苯环结构,其中两个取代基是:—COOCH3和 ,且二者处于对位。
,且二者处于对位。
(4)原料B俗名“马莱酐”,它是马莱酸(HOOC-CH=CH-COOH)的酸酐,请设计用原料CH2OH-CH=CH-CH2OH合成马莱酸的合成路线。合成路线流程图示例如下:
某反应中反应物与生成物有:FeCl2、FeCl3、CuCl2、Cu。
(1)将上述反应设计成的原电池如图甲所示,请回答下列问题: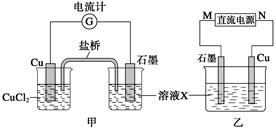

①图中X溶液是;
②石墨电极上发生的电极反应式为;
③原电池工作时,盐桥中的(填“K+”或“Cl-”)不断进入X溶液中。
(2)将上述反应设计成的电解池如图乙所示,乙烧杯中金属阳离子的物质的量与电子转移的物质的量的变化关系如图丙,请回答下列问题:
①M是极;②图丙中的②线是的变化。
③当电子转移为2 mol时,向乙烧杯中加入L 5 mol·L-1 NaOH溶液才能使Cu2+沉淀完全。
(3)铁的重要化合物高铁酸钠(Na2FeO4)是一种新型饮用水消毒剂,具有很多优点。
①高铁酸钠生产方法之一是电解法,其原理为Fe+2NaOH+2H2O Na2FeO4+3H2↑,则电解时阳极的电极反应式是。
Na2FeO4+3H2↑,则电解时阳极的电极反应式是。
②高铁酸钠生产方法之二是在强碱性介质中用NaClO氧化Fe(OH)3生成高铁酸钠、氯化钠和水,该反应的离子方程式为。
汽车尾气中含有CO、NO2等有毒气体,对汽车加装尾气净化装置,可使有毒气体相互反应转化为无毒气体。汽车尾气中CO与H2O(g)在一定条件下可以发生反应:
CO(g)+H2O(g) CO2(g)+H2(g)ΔH<0。820 ℃时在甲、乙、丙三个恒容密闭容器中,起始时按照下表进行投料,达到平衡状态,K=1.0。
CO2(g)+H2(g)ΔH<0。820 ℃时在甲、乙、丙三个恒容密闭容器中,起始时按照下表进行投料,达到平衡状态,K=1.0。
| 起始物质的量 |
甲 |
乙 |
丙 |
| n(H2O)/mol |
0.10 |
0.20 |
0.20 |
| n(CO)/mol |
0.10 |
0.10 |
0.20 |
(1)该反应的平衡常数表达式为。
(2)平衡时,甲容器中CO的转化率是。比较下列容器中CO的转化率:乙甲;丙甲(填“>”、“=”或“<”)。
(3)丙容器中,若要通过改变温度,使CO的平衡转化率增大,则温度需要降低才能达到,则降温后的平衡常数K(填“增大”、“减小”或“不变”)。
合理利用资源,降低碳的排放,实施低碳经济是今后经济生活主流方向。
⑴下列措施不利于有效减少二氧化碳排放的是。
A.植树造林,保护森林,保护植被
B.加大对煤和石油的开采,并鼓励使用石油液化气
C.推广使用节能灯和节能电器,使用空调时夏季温度不宜设置过低,冬天不宜过高
D.倡导出行时多步行和骑自行车,建设现代物流信息系统,减少运输工具空驶率
⑵科学家致力于二氧化碳的“组合转化”技术研究,如将CO2和H2以1∶4比例混合通入反应器,适当条件下反应可获得一种能源。完成以下化学方程式:CO2+4H2 +2H2O。
+2H2O。
⑶CO2合成生产燃料甲醇(CH3OH)是碳减排的新方向。进行如下实验:某温度下在1 L的密闭容器中,充2 mol CO2和6 mol H2,发生:CO2(g)+3H2(g ) CH3OH(g)+H2O(g)能判断该反应已达化学反应限度标志的是(填字母)。
CH3OH(g)+H2O(g)能判断该反应已达化学反应限度标志的是(填字母)。
A.CO2百分含量保持不变
B.容器中H2浓度与CO2浓度之比为3:1
C.容器中混合气体的质量保持不变
D.CO2生成速率与CH3OH生成速率相等
现测得CO2和CH3OH(g)的浓度随时间变化如左下图所示。从反应开始到平衡,氢气的平均反应速率v(H2)= mol/(L·min)。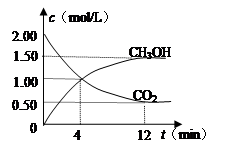
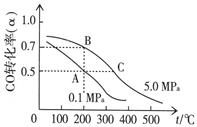
⑷CO在催化作用下也能生成甲醇:CO(g)+2H2(g)  CH3OH(g);已知密闭容器中充有10 mol CO与20 mol H2,CO的平衡转化率(α)与温度、压强的关系如右上图所示。
CH3OH(g);已知密闭容器中充有10 mol CO与20 mol H2,CO的平衡转化率(α)与温度、压强的关系如右上图所示。
①若A、C两点都表示达到的平衡状态,则自反应开始到达平衡状态所需的时间tA tC(填“大于”、“小于”或“等于”)。
②若A、B两点表示在某时刻达到的平衡状态,此时在A点时容器的体积为VAL,则A、B两点时容器中,n(A)总︰n(B)总=。
⑸以KOH为电解质的甲醇燃料电池总反应为:2CH3OH+3O2+4KOH= 2K2CO3+6H2O,通入甲醇的电极为燃料电池的负极,正极发生的电极反应式为。
(1)已知下列两个热化学方程式:
C3H8(g)+5O2(g) =3CO2(g)+4H2O(l)ΔH=-2220.0 kJ·mol-1
H2O(l)=H2O(g)ΔH="+44.0" kJ·mol-1
则0.5mol丙烷燃烧生成CO2和气态水时释放的热量为。
(2)已知:TiO2(s)+2Cl2(g)=TiCl4(l)+O2(g)ΔH=+140 kJ·mol-1
2C(s)+O2(g)="2CO(g)" ΔH=-221 kJ·mol-1
写出TiO2和焦炭、氯气反应生成TiCl4和CO气体的热化学方程式:。
(3)科学家已获得了极具理论研究意义的N4分子,其结构为正四面体(如图所示),与白磷分子相似。已知断裂1molN—N键吸收193kJ热量,断裂1molN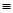 N键吸收941kJ热量,则1molN4气体转化为2molN2时要放出kJ能量。
N键吸收941kJ热量,则1molN4气体转化为2molN2时要放出kJ能量。
(4)阿波罗宇宙飞船上使用的是氢氧燃料电池,其电池总反应为:2H2+O2=2H2O,电解质溶液为稀H2SO4溶液,电池放电时是将能转化为能。其电极反应式分别为:负极,正极。
按下图所示装置进行实验,并回答下列问题:
(1)判断装置的名称:A池为,B池为。
(2)锌极为极,电极反应式为;铜极为极,电极反应式为;石墨棒C1为极,电极反应式为;石墨棒C2附近发生的实验现象为,反应结束后,B池溶液的pH值。(增大、减小、不变,忽略气体溶于水) 。
(3)当C2极析出224 mL气体(标准状况下),锌的质量(增加或减少)g。