在下列给定条件的溶液中,一定能大量共存的离子组是
| A.澄清透明溶液:H+、Na+、SO42-、C6H5O- |
| B.常温下Kw/c(H+)=0.1 mol/L的溶液:K+、Na+、SiO32-、NO3- |
| C.铁片加入产生气泡的溶液:Na+、NH4+、I-、NO2- |
| D.NaHCO3溶液:K+、Na+、SO42-、Al3+ |
“类推”的思维方式在化学学习与研究中经常采用,但是有时会产生错误结论。下列类推结论中,正确的是
| A.由甲酸可以发生银镜反应可推出其余的羧酸也均能发生银镜反应 |
B.由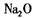 中阳离子与阴离子的个数比为2:1,可推出 中阳离子与阴离子的个数比为2:1,可推出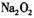 中阳离宇与阴离子的个数比为1:1 中阳离宇与阴离子的个数比为1:1 |
C.由“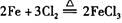 ”反应可推出“ ”反应可推出“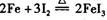 ”反应也能发生 ”反应也能发生 |
| D.Na,K具有强还原性,Na常温下与水剧烈反应,故K常温下也能与水剧烈反应 |
化学用语是学习化学的重要工具。以下化学用语表示错误的是
A.质量数之和是质子数之和两倍的水分子符号可能是: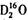 |
B.NaHCO3水溶液呈碱性的原因: |
C.基态硫离子的电子排布式: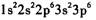 |
D.熔融状态下硫酸氢钠的电离方程式: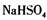 (熔融)= (熔融)=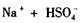 |
2010年上海世博会的主题是“城市,让生活更美好"。大会提倡低碳、节能、环保,下列措施中不符合该主题的是
| A.世博园区公共交通使用的是纯电动汽车 |
| B.日本馆的外壳使用非晶硅薄膜,以充分利用太阳能 |
| C.游客为了方便大量使用一次性塑料袋 |
D.世博停车场安装催化光解设施,可将汽车尾气中 和 和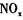 反应生成无毒气体 反应生成无毒气体 |
在下列变化中,只发生物理变化的是
| A.荔枝酿酒 | B.酸雨侵蚀建筑物 |
| C.空气液化制取氮气 | D.生石灰遇水成为熟石灰 |
向饱和 石灰水中不断通入二氧化碳,其溶液导电性的变化是
石灰水中不断通入二氧化碳,其溶液导电性的变化是
| A.由弱变强 | B.由强变弱 |
| C.由强变弱,再变强 | D.由弱变强,再变弱 |