生铁中含碳和硫等元素。化学兴趣小组对某生铁样品进行了探究。根据要求回答下列问题。
Ⅰ.生铁中碳和硫元素的定性检验
按如图装置进行实验(夹持仪器已略去,填接口字母代号)可以实现碳和硫元素的检验。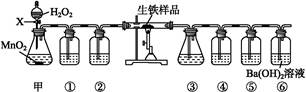
(1)仪器X的名称是 ;装置③⑤中试剂相同,装置④中盛放的试剂是 。
(2)写出甲中反应的化学方程式 。
(3)如果撤除装置③④⑤,能否确认生铁样品中碳元素的存在? ,理由是 。
Ⅱ.生铁中碳、硫质量分数的测定
(4)甲同学认为,以上装置可以粗略测定样品中碳的含量。称取样品w1 g进行实验,充分反应后,测得装置⑥中生成的沉淀为w2 g,该样品中碳的质量分数为 (用含w1、w2的式子表示)。
(5)乙同学认为,待一定量样品充分反应后,向装置④中加入过量氯化钡溶液,根据沉淀质量可以计算样品中硫的质量分数,此方案测得的结果 (填“偏大”或“偏小”);若要提高硫元素含量的测定精度,在不改变实验原理的前提下,可以采取的一种措施是 。
硫酸锰在工业上广泛用于制电解猛、合成脂肪酸催化剂等。某科研小组利用软锰矿(主要成分为MnO2,同时含少量铁、铝等的化合物)制备硫酸锰晶体,其工艺流程如下: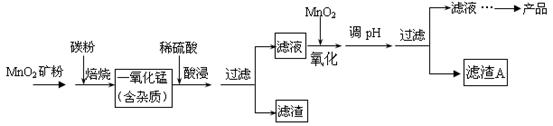
部分金属阳离子以氢氧化物形式完全沉淀时溶液的pH见下表:
| 沉淀物 |
Al(OH)3 |
Fe(OH)3 |
Fe(OH)2 |
Mn(OH)2 |
| pH |
5.2 |
3.2 |
9.7 |
10.4 |
已知溶液的pH大于9时氢氧化铝又开始溶解。
请回答下列问题:
(1)焙烧时一般需要把矿石粉碎,矿石粉碎的目的是_______________;高温焙烧时在实验室宜选择的主要仪器是______________。
(2)酸浸、过滤后再向滤液中加入MnO2的目的是将溶液中的Fe2+氧化成Fe3+,该反应的离子方程式为 。
(3)在氧化的同时需要调节溶液的pH值,应调节pH的范围为 。滤渣A的成分除MnO2外,还有_______________。
(4)滤液得到产品的实验操作步骤为蒸发浓缩、冷却结晶、过滤、洗涤、干燥。检验产品已洗涤干净的实验操作为______________________________。
(5)工业生产中为了确定需要向滤液中加入多少MnO2粉末,可准确量取10.00mL滤液用0.02mol/L酸性KMnO4溶液滴定,判断滴定终点的方法是 ;若达滴定终点共消耗10.00mL酸性KMnO4溶液,则滤液中Fe2+浓度是______________。
(6)MnO2可作超级电容器材料。用惰性电极电解MnSO4溶液可制得MnO2,其阳极的电极反应式为:
__________________________________。
已知氨气具有还原性,某校化学兴趣小组为了探究氨气能否和氢气一样还原金属氧化物,设计如下实验装置(夹持装置未画),请回答下列问题:
(1)仪器E的名称是____;F中的试剂最好是___(选填下列字母编号)。
A.饱和NH4Cl溶液B.稀NaOH溶液C.CaO
(2)有同学模仿排饱和食盐水收集氯气的方法,想用排饱和氯化铵溶液的方法收集氨气,你认为他能否达到目的?_________(填“能”或“否“),理由是_____________________。
(3)若氨气与金属氧化物MxOy反应生成M、N2、H2O,通过测量生成水的质量来测定M的相对原子质量。
①按气流方向各仪器接口的顺序为(装置可重复使用):
a→____→____→b→c→____→____→____→____。
②实验中多余的NH3需吸收处理。以下各种尾气吸收装置(a、b、d装置中盛放的均是水)中能起到吸收氨气作用的是________。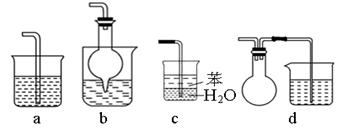
③若实验中准确称取金属氧化物的质量为ng,完全反应后,测得生成水的质量为mg,则M的相对原子质量为__________(用含x、y、m、n的式子表示)。
(4)若金属氧化物MxOy为CuO。有同学认为:NH3与CuO反应生成的红色物质中可能含有Cu2O。已知:Cu2O是一种碱性氧化物;在酸性溶液中,Cu+的稳定性比Cu2+差(2Cu+=Cu+Cu2+)。请你设计一个简单的实验检验该红色物质中是否含有Cu2O:________。
某研究性学习小组用下列装置(铁架台等支撑仪器略)探究氧化铁与乙醇的反应,并检验反应产物。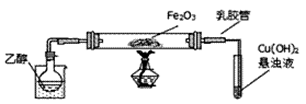
(1)装入试剂之前,需要进行什么操作: ;为快速得到乙醇气体,可采取的方法是 ;若实验时小试管中的溶液已经开始发生倒吸,你采取的措施是_________(填写编号);
a.取下小试管b.移去酒精灯
c.将导管从乳胶管中取下 d.以上都可以
(2)盛Cu(OH)2悬浊液的试管中可能出现的现象为___________________。
(3)如图实验,观察到红色的Fe2O3全部变为黑色固体(M),充分反应后停止加热。为了检验M的组成,进行下列实验。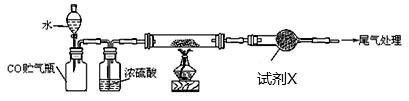
①M能被磁铁吸引;加入足量稀硫酸,振荡,固体全部溶解,未观察到有气体生成;
②经检验溶液中有Fe2+和Fe3+;
关于M 中铁元素价态的判断正确的是 (填写编号)。
a.一定有+3价和+2价铁,一定无0价铁 b.一定有+3价、+2价和0价铁
c.一定有+3价和0价铁,一定无+2价铁 d.一定有+3和+2价铁,可能有0价铁
(4)若M的成份可表达为FeXOY,用CO还原法定量测定其化学组成。称取a g M样品进行定量测定,实验装置如上图,步骤如下。
①组装仪器;②点燃酒精灯;③加入试剂;④打开分液漏斗活塞;
⑤检查气密性;⑥停止加热;⑦关闭分液漏斗活塞;⑧……。
正确的操作顺序是__________(填写编号)
a.①⑤④③②⑥⑦⑧b.①③⑤④②⑦⑥⑧
c.①⑤③④②⑥⑦⑧ d.①③⑤②④⑥⑦⑧
实验装置中盛水的仪器名称是 ;试剂X为 。
(5)若实验中每步反应都进行完全,反应后M样品质量减小b g,则FeXOY中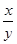 =_____。
=_____。
碳酸锂,可用于制陶瓷、药物、催化剂等,常用的锂离子电池原料。以锂辉石(主要成分为LiAlSi2O6)为原材料制备Li2CO3的工艺流程如下: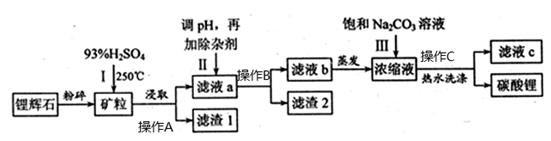
已知:①2LiAlSi2O6+H2SO4(浓) 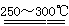 Li2SO4+Al2O3·4SiO2·H2O↓
Li2SO4+Al2O3·4SiO2·H2O↓
②Fe3+、Al3+、Fe2+和Mg2+以氢氧化物形式完全沉淀时,溶液的PH分别为3.2、4.7、9.0和11.1
③某些物质的溶解度(S)如右表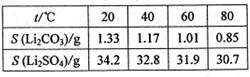
请回答下列问题:
(1)操作A、操作B、操作C是 ,锂辉石用浓硫酸浸取之前要粉碎成细颗粒的目的是 。
(2)滤液a中含有Li+、SO42-,另含有Fe3+、Al3+、Fe2+、Mg2+ 、Ca2+、Na+等杂质,步骤Ⅱ需在搅拌下加入石灰石以调节溶液的pH到6.0~6.5,此时沉淀的杂质离子有 。
(3)步骤Ⅱ在滤液a中加入的除杂剂依次为适量的H2O2溶液,石灰乳和Na2CO3溶液,发生反应的离子方程式有 。
(4)步骤Ⅲ中加入饱和Na2CO3溶液过滤后需要用热水洗涤的原因是 ,检验是否洗涤干净的方法是 。
(5)从滤液c中可回收的主要物质是 。
【实验化学】制备水杨酸对正辛基苯基酯(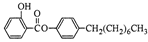 )如下:
)如下:
步骤一:将水杨酸晶体投入三颈烧瓶中,再加入氯苯,搅拌溶解后,加入无水三氯化铝。
步骤二:按下图所示装置装配好仪器,水浴加热控制温度在20~40℃之间,在搅拌下滴加SOCl2,反应制得水杨酰氯。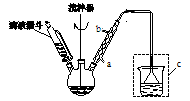
该反应为: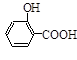 (水杨酸)+SOCl2—→
(水杨酸)+SOCl2—→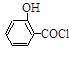 (水杨酰氯)+HCl↑+SO2↑
(水杨酰氯)+HCl↑+SO2↑
步骤三:将三颈烧瓶中的混合液升温至80℃,再加入对正辛苯酚[ ],温度控制在100℃左右,不断搅拌。
],温度控制在100℃左右,不断搅拌。
步骤四:过滤、蒸馏、减压过滤;酒精洗涤、干燥。
(1)步骤一中加入三氯化铝的作用是 。
(2)实验时,冷凝管中的水应从 进 出(选填“a”或“b”);装置c的作用是 。
(3)步骤三中发生反应的化学方程式为 。
(4)步骤四减压过滤操作中,除烧杯、玻璃棒外,还必须使用的硅酸盐材料的仪器有 。
(5)步骤四减压过滤时,有时滤纸会穿孔,避免滤纸穿孔的措施是 。