Q、W、X、Y、Z为五种原子序数递增的短周期元素。
已知:①Q原子核外电子数等于电子层数,且与W组成的化合物是沼气的主要成分;
②W与Y、X与Y组成的化合物是机动车排出的大气污染物;
③Y与Z能形成电子总数为30和38的两种离子化合物。
(1)W在周期表的位置:________;电子数为38的Y与Z形成化合物的电子式:________。
(2)工业合成XQ3,ΔH<0;下列措施既能加快反应速率,又能使原料转化率一定都提高的是________。
| A.升高温度 |
| B.加入高效催化剂 |
| C.将XQ3及时分离出去 |
| D.增大反应体系压强 |
E.增大反应物浓度
(3)标准状况下22.4 L X的气态氢化物,与0.5 L 1 mol/L的X的最高价氧化物的水化物反应,所得碱性溶液中离子浓度由大到小顺序是_______(用化学式表示)。
现有下列四种物质:① SiO2、② NH3、③ Na2CO3、④ Al2(SO4)3。其中,俗称为“苏打”的是____(填序号,下同),极易溶于水的气体是____,向其溶 液中,逐滴加入氢氧化钠溶液,先产生白色沉淀,后沉淀溶解的是____,为石英主要成份的是____
液中,逐滴加入氢氧化钠溶液,先产生白色沉淀,后沉淀溶解的是____,为石英主要成份的是____
2009年9月8日,中国卫生部部长陈竺表示,中国甲型H1N1流感疫苗接种方案的原则已经确立:要首先保护最为易感和脆弱的人群,特别是中学生、有基础性疾病(如糖尿病)的人、一线的公共服务人员。请根据这一主题和题意回答下列问题。(用下列选项的字母代号填空)
| A.蛋白质 | B.强氧化性 | C.葡萄糖 | D.变性 |
E.强酸性 F.淀粉 G.盐析 H.强还原性
(1)糖尿病是因为病人的尿液中含而得名的。
(2)甲型H1N1流感病毒和疫苗都含有。
(3)为预防甲型H1Nl流感.可用具有性的NaClO溶液进行环境消毒。
(4)烹制猪肉时温度达到71℃,就可杀死细菌和病毒。这是因为细菌和病毒发生了。
(14分)随着人类对温室效应和资源短缺等问题的重视,如何降低大气中CO2的含量及有效地开发利用CO2,引起了各国的普遍关注
⑴目前工业上有一种方法是用CO2来生产燃料甲醇。为探究反应原理,现进行如下实验:在体积为1 L的密闭容器中,充入1mol CO2和3mol H2,一定条件下发生反应:
CO2(g)+3H2(g)  CH3OH(g)+H2O(g)△H=-49.0kJ/mol
CH3OH(g)+H2O(g)△H=-49.0kJ/mol
测得CO2和CH3OH(g)的浓度随时间变化如图所示。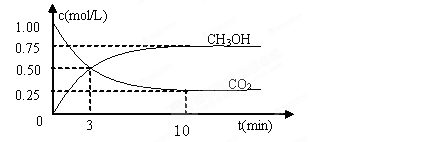
①反应开始到平衡,H2的平均反应速率v(H2)=_____mol/(L·min)。H2的转化率为。
②下列措施中能使n(CH3OH)/n(CO2)增大的是___________。
| A.升高温度 | B.充入He(g),使体系压强增大 |
| C.将H2O(g)从体系中分离 | D.再充入1mol CO2和3mol H2 H2 |
E、使用催化剂 F、缩小容器体积
⑵①反应进行到3分钟时, 同种物质的v正与v逆的关系: v正v逆 (填>,=,<)
同种物质的v正与v逆的关系: v正v逆 (填>,=,<)
②上述反应平衡常数的表达式为,经计算该温度下此反应平衡常数的数值为。
10℃时加热NaHCO3饱和溶液,测得该溶液的pH发生如下变化:
| 温度(℃) |
10 |
20 |
30 |
加热煮沸后冷却到50℃ |
| pH |
8.3 |
8.4 |
8.5 |
8.8 |
甲同学认为,该溶液的pH值升高的原因是HCO3—的水解程度增大,故碱性增强,该反应的离子方程式为 。
。
乙同学认为,溶液pH升高的原因是NaHCO3受热分解,生成了Na2CO3,并推断Na2CO3的水解程度(填“大于”或“小于”)NaHCO3。
丙同学认为甲、乙的判断都不充分。丙认为:
(1)只要在加热煮沸的溶液中加入足量的试剂X,若产生沉淀, 则乙判断正确。试剂X是。A、Ba(OH)2溶液 B、NaOH溶液 C、BaCl2溶液 D、澄清石灰水
则乙判断正确。试剂X是。A、Ba(OH)2溶液 B、NaOH溶液 C、BaCl2溶液 D、澄清石灰水
(2)将加热后的溶液冷却到10℃,若溶液的pH(填“高于”、“低于”或“等于”)8.3,则甲判断正确。
炼金废水中含有络离子[Au(CN)2]-,它能电离出有毒的CN-,当CN-与H+结合时 生成剧毒的HCN。完成下列问题:
生成剧毒的HCN。完成下列问题:
(1)HCN的水溶液酸性很弱,则HCN电离方程式为_________________,NaCN的水溶液呈碱性是因为_________________(用离子方程式表示)。
(2)室温下,如果将0.2mol NaCN和0.1mol HCl全部溶于水,形成混合溶液(假设无损失),①___和___两种粒子的物质的量之和等于 0.2mol。②___和___两种粒子的物质的量
0.2mol。②___和___两种粒子的物质的量 之和比H+多0.1mol。
之和比H+多0.1mol。
(3)已知某溶液中只存在OH-、H+、Na+、CN-四种离子,某同学推测该溶液中各离子浓度大小顺序可能有如下四种关系:
| A.c(CN-)>c(Na+)>c(H+)>c(OH-) | B.c(Na+)>c(CN-)>c(OH-)>c(H+) |
| C.c(CN-)>c(H+)>c(Na+)>c(OH-) | D.c(CN-)>c(Na+)>c(OH-)>c(H+) |
①若溶液中只溶解了一种溶质,上述离子浓度大小顺序关系中正确的是(填序号)。
②若上述关系中C是正确的,则溶液中溶质的化学式是__和_。
③若该溶液中由体积相等的稀HCN溶液和NaOH溶液混合而成,且恰好呈中性,则混合前
c(HCN)c(NaOH)(填“>”、“<”、或“=”下同),
混合后溶液中c(Na+)与c(CN-)的关系c(Na+)c(CN-)。