钛是20世纪50年代发展起来的一种重要的结构金属,钛合金因具有强度高、耐蚀性好、耐热性高等特点而被广泛用于各个领域。
(1)与钛同周期的所有元素的基态原子中,未成对电子数与钛相同的元素有 (填元素符号)。
(2)[Ti(OH)2(H2O)4]2+中的化学键有 。
| A.σ键 | B.π键 | C.离子键 | D.配位键 |
(3)纳米TiO2是一种应用广泛的催化剂,纳米TiO2催化的一个实例如下图所示。
化合物甲的分子中采取sp2杂化方式的碳原子个数为 ,化合物乙中采取sp3杂化的原子的第一电离能由小到大的顺序为 。
(4)有一种氮化钛晶体的晶胞如图所示,该晶体的化学式为 ,该晶体中Ti原子周围与它距离最近且相等的N原子的个数______。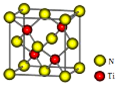
13分)机物A为烃类化合物,质谱图表明其相对分子质量为70,其相关反应如下图所示,其中B、D、E的结构中均含有2个—CH3,它们的核磁共振氢谱中均出现4个峰。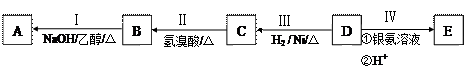
请回答:
(1)D的分子式为;
(2)Ⅲ的反应类型为(填字母序号);
a.还原反应 b.加成反应 c.氧化反应 d.消去反应
(3)写出下列反应的化学方程式:
Ⅰ:;
Ⅱ:;
C和E可在一定条件下反应生成F,F为有香味的有机化合物,该反应的化学方程式
为;
(4)A的同分异构体中有一对互为顺反异构,且结构中有2个—CH3,它们的结构简式为
和;
(5)E的另一种同分异构体能发生银镜反应,能与足量金属钠生成氢气,不能发生消去反应,其结构简式为。
(9分)有机物A的结构简式为: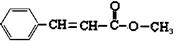
(1)A中含氧官能团为_______________________(写名称);
(2)1mol该化合物与氢气发生加成反应,最多需要_______mol氢气;
(3)A在稀硫酸水溶液中加热水解,得到有机物B和D,D是芳香族化合物,反应的方程式为________________________________________;
(4)A水解生成的芳香族化合物D有多种同分异构体,请写出其中含有苯环、且能发生水解反应和银镜反应的所有同分异构体的结构简式(不包括立体异构)_____。
按要求回答下列问题:
(1)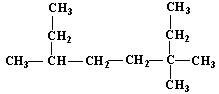 的名称为___________________________;
的名称为___________________________;
(2)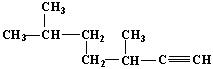 的名称为____________________________;
的名称为____________________________;
(3)2,4-二氯甲苯的结构简式为_________________________ ___;
___;
(4)某物质结构如图所示,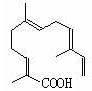
碳原子数为;
该物质可以与下列(填序号)发生反应。
| A.KMnO4酸性溶液 | B.氢气 | C.溴水 | D.NaOH溶液 |
生物质能是一种洁净、可再生的能源。生物质气(主要成分为CO、CO2、H2等)与H2混合,催化合成甲醇是生物质能利用的方法之一。
(1)上述反应的催化剂含有Cu、Zn、Al等元素。写出基态Al原子的价电子排布图。
(2)根据等电子原理,写出CO分子结构式。
(3)甲醇催化氧化可得到甲醛,甲醛与新制Cu(OH)2的碱性溶液反应生成Cu2O沉淀。
①甲醇的沸点比甲醛的高,其主要原因是;甲醛分子中碳原子轨道的杂化类型为。
②甲醛分子的空间构型是;1mol甲醛分子中σ键的数目为。
③在1个Cu2O晶胞中(结构如图所示),所包含的Cu原子数目为。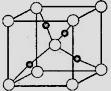
四种元素X、Y、Z、W位于元素周期表的前四周期,已知它们的核电荷数依次增加,且核电荷数之和为51;Y原子的L层p轨道中有2个电子;Z与Y原子的价层电子数相同;W原子的L层电子数与最外层电子数之比为4︰1,其d轨道中的电子数与最外层电子数之比为5︰1。
(1)Y、Z可分别与X形成只含一个中心原子的共价化合物a、b,它们的分子式分别是、;杂化轨道分别是、;a分子的立体结构是。
(2)Y的最高价氧化物和Z的最高价氧化物的晶体类型分别是晶体、晶体。
(3)X的氧化物与Y的氧化物中,分子极性较小的是(填分子式)。
(4)Y与Z比较,电负性较大的,其中W+2价离子的核外电子排布式是。