下列关于除去物质中杂质的方案设计,所选除杂试剂合理的是( )
| |
主要物质 |
杂质 |
除杂试剂 |
| A |
SiO2 |
Al2O3 |
盐酸 |
| B |
Si |
C |
氧气 |
| C |
CO2 |
SO2 |
Na2CO3溶液 |
| D |
Cl2 |
HCl |
NaOH溶液 |
等体积的硫酸钠、硫酸镁、硫酸铝溶液分别于足量氯化钡溶液反应,若生成硫酸钡的质量相等,则三种硫酸盐的物质的量浓度之比为
| A.3:3:1 | B.6:3:2 | C.3:2:1 | D.1:1:1 |
下列溶液中的Cl-的物质的量与50 mL 1 mol ·L-1 MgCl2溶液中相等的是
| A.150 mL 1 mol·L-1的NaCl溶液 | B.75 mL 0.5mol·L-1的CaCl2溶液 |
| C.50 mL 2 mol·L-1的KCl溶液 | D.75 mL 1 mol ·L-1的FeCl3溶液 |
下列括号中的物质是除去杂质所需的药品,其中不正确的是
| A.FeCl2中有CuCl2(铁粉) | B.KCl中有杂质K2SO4(氯化钡) |
| C.N2中混有O2(灼热的铜粉) | D.CO2中混有HCl(氢氧化钠溶液) |
现有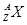 和
和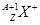 两种粒子,下列叙述正确的是
两种粒子,下列叙述正确的是
| A.质子数相等 |
| B.X元素的质量数为A |
C.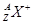 一定具有稀有气体元素原子的核外电子排布 一定具有稀有气体元素原子的核外电子排布 |
| D.它们的化学性质几乎完全相同 |
下列关于物质的量浓度表述正确的是
| A.0.2 mol·L-1 Na2SO4溶液中含有Na+和SO42—总物质的量为0.6 mol |
| B.50mL 2 mol·L-1的NaCl溶液和100mL 0.5mol·L-1MgCl2溶液中,Cl-的物质的量浓度相等 |
| C.用1 L水吸收22.4 L氯化氢(标况下)所得盐酸的浓度是1 mol·L-1 |
| D.10 g 98%的硫酸(密度为1.84g · cm—3)与10mL 18.4mol·L—1的硫酸的浓度是相同的 |