工业上以黄铜矿(主要成分是CuFeS2,杂质不溶于水和酸)为原料,制备蓝色晶体G,其化学式为[Cu(NH3)4]SO4·H2O,涉及流程如下:
已知25 ℃时,几种金属氢氧化物的溶度积常数和完全沉淀的pH范围如下表:
| |
Fe(OH)2 |
Cu(OH)2 |
Fe(OH)3 |
| Ksp |
8.0×10-16 |
2.2×10-20 |
4.0×10-38 |
| 完全沉淀pH |
≥9.6 |
≥6.4 |
≥3.2 |
(1)加快黄铜矿焙烧速率,可采用的措施有 (写两种)。
(2)加入双氧水可能发生反应的离子方程式为 ;
试剂X的化学式为 。
(3)常温下,0.1 mol/L试剂Y的pH=11,则该温度下,试剂Y的电离常数为 ,用pH试纸测该溶液pH的方法是 。
(4)已知Cu(OH)2+4NH3·H2O [Cu(NH3)4]2++2OH-+4H2O,写出该反应的平衡常数表达式: 。
[Cu(NH3)4]2++2OH-+4H2O,写出该反应的平衡常数表达式: 。
(5)在溶液N中加入乙醇的目的是 。
糖类、油脂和蛋白质在人类的生命活动过程中起重要作用,请根据糖类、油脂、蛋白质的有关性质回答下列问题:
(1)糖尿病是由于人体内胰岛素紊乱所导致的代谢紊乱综合症,以高血糖为主要标志。血糖是指血液中的葡萄糖(C6H12O6)。下列说法正确的是______________。
A、葡萄糖属于碳水化合物,分子式可表示为C6(H2O)6,则每个葡萄糖分子中含6个H2O
B、糖尿病人尿糖较高,可用新制的氢氧化铜悬浊液来检测病人尿液中的葡萄糖
C、葡萄糖可用于制镜工业
D、淀粉水解的过程中可以产生麦芽糖和蔗糖
(2)糖尿病人宜多吃蔬菜和豆类食品。蔬菜中富含纤维素,豆类食品中富含油脂和蛋白质。下列说法中错误的是_______________。
A、油脂和蛋白质都属于天然有机高分子化合物,蛋白质都不溶于水
B、用灼烧闻气味的方法可以区别合成纤维和羊毛
C、人体内不含纤维素水解酶,人不能消化纤维素,因此蔬菜中的纤维素对人没有用处
D、紫外线、医用酒精能杀菌消毒,是因为可以使细菌的蛋白质变性
(3)某种蛋白质的结构片段如右图:
上述蛋白质结构片段完全水解所生成的氨基酸中属于芳香族化合物的是:__ ___。
(4)已知上述蛋白质结构片段的相对分子质量是307,则水解生成的各种氨基酸的相对分子质量之和为。
对比同体积、同浓度的盐酸和醋酸,c(H+)前者后者,与碱完全中和时,消耗NaOH的物质的量是前者后者,与足量的Zn反应产生H2的速率是前者后者,产生H2的量是前者后者。(填“>”、“<”或“=”)
(12分)恒温下,将a mol O2与bmol SO2的混合气体通入一个固定容积的密闭容器中,发生如下反应:
O2 (g) + 2SO2(g) 2SO3(g)
2SO3(g)
(一)①若反应达平衡时,n(O2) = 4mol,n(SO3) = 4mol,计算a的值为。
②平衡时总体积在标准状况为313.6L,原混合气体与平衡混合气体的总物质的量之比(写出最简整数比,下同),n(始)∶n(平) =。
③达到平衡时,O2和SO2的转化率之比,α(O2)∶α (SO2)=。
(二)若起始将6mol O2、b mol SO2和1 molSO3通入上反应容器中,起始反应向正方向进行,使反应达到平衡时容器中气体的物质的量为12mol。则b的取值范围是。
在2L密闭容器内,800℃时反应:2NO(g)+O2(g)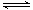 2NO2(g)体系中,n(NO)随时间的变化如表:
2NO2(g)体系中,n(NO)随时间的变化如表:
| 时间(s) |
0 |
1 |
2 |
3 |
4 |
| n(NO)(mol) |
0.020 |
0.01 |
0.008 |
0.007 |
0.007 |
(1)写出该反应的平衡常数表达式:K= 。
已知: >
>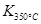 ,则该反应是 热反应。
,则该反应是 热反应。
(2)图中表示NO2的变化的曲线是 ;用O2表示从0~2 s内该反应的平均速率v= ;
(3)能说明该反应已达到平衡状态的是 。
a.v(NO2)=2v(O2) b.容器内压强保持不变
c.v逆(NO)=2v正(O2) d.容器内密度保持不变
(4)为使该反应的反应速率增大,且平衡向正反应方向移动的是 。
a.及时分离除NO2气体 b.适当升高温度
c.增大O2的浓度 d.选择高效催化剂
(1)常温下物质的量浓度相同的aHF、bNH3·H2O、c H2S溶液,电离常数分别为7.2ⅹ10-4、1.8ⅹ10-5和K1=9.1ⅹ10-8,K2=1.1ⅹ10-12。
①电解质的强弱顺序为__(填a、b、c)
②溶质分子浓度最小的是__(填a、b、c)
③氢离子浓度最小的是___(填a、b、c)
(2)1L1mol/LH2SO4溶液与2L1mol/LNaOH溶液完全反应,放出114.6kJ的热量,由此推知H2SO4与NaOH发生中和反应的中和热为_________,
表示该中和热的热化学方程式为___________。
(3)向1L1mol/L的NaOH溶液中加入下列物质:①浓H2SO4;②稀硝酸;③稀醋酸,恰好完全反应的热效应△H1、△H2、△H3的大小关系为。
(4)已知下列反应的反应热:
①CH3COOH(l) + 2O2 (g)= 2CO2 (g)+ 2H2O(l)△H=-870.3kJ∕mol
②C(S) + O2 (g)= CO2 (g)△H=-393.5kJ∕mol
③2C(S) + 2H2 (g) + O2 (g)= CH3COOH(l)△H=-488.3kJ∕mol
请写出H2燃烧热的热化学方程式。