海洋资源的开发与利用具有广阔的前景。海水的pH一般在7.5~8.6之间。某地海水中主要离子的含量如下表:
| 成分 |
Na+ |
K+ |
Ca2+ |
Mg2+ |
Cl- |
SO42- |
HCO3- |
| 含量/mg·L-1 |
9 360 |
83 |
200 |
1 100 |
16 000 |
1 200 |
118 |
(1)电渗析法是近年发展起来的一种较好的海水淡化技术,其原理如下图所示。其中阴(阳)离子交换膜只允许阴(阳)离子通过。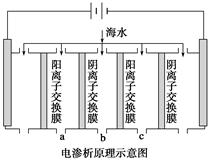
①阴极的电极反应式为__________________。
②电解一段时间,阴极区会产生水垢,其成分为CaCO3和Mg(OH)2,写出生成CaCO3的离子方程式______________________________________。
③淡水的出口为a、b、c中的________出口。
(2)海水中锂元素储量非常丰富,从海水中提取锂的研究极具潜力。锂是制造化学电源的重要原料,如LiFePO4电池某电极的工作原理如下图所示: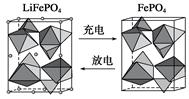
该电池电解质为传导Li+的固体材料。放电时该电极是电池的________极(填“正”或“负”),电极反应式为______________________。
某化学小组采用以下装置(如图一),以环己醇制备环己烯。已知:


图一[
(1)制备粗品
将12.5mL环己醇加入试管A中,再加入1mL浓硫酸,摇匀后放入碎瓷片,缓慢加热至反应完全,在试管C内得到环己烯粗品。
①A中碎瓷片的作用是 ,导管B除了导气外还具有的作用是
,导管B除了导气外还具有的作用是
②试管C置于冰水浴中的目的是 。
。
(2)制备精品
图二
①环己烯粗品中含有环己醇和少量酸性杂质等。加入饱和食盐水,振荡、静置、分层,环己烯在________层(填“上”或“下”),分液后用________(填入编号)洗涤。
A.KMnO4溶液B.稀H2SO4C.Na2CO3溶液
②再将环己烯按(图二)装置蒸馏,冷却水从 口进入(填字母)。蒸馏时要加入生石灰,目的是 。
|
③收集产品时,控制的温度应在 左右,实验制得的环己烯精品质量低于理论产量,可能的原因是()
A.蒸馏时从70℃开始收集产品 B.环己醇实际用量多了 C.测定沸点
C.测定沸点
近年来,由于石油价格不断上涨,以煤为原料制备一些化工产品的前景又被看好。下图是以煤为原料生产聚氯乙烯(PVC)和人造羊毛的合成路线。
请回答下列问题:
(1)写出反应类型:反应①反应②。
(2)写出结构简式:A、B、PVC 。
。
(3)写出C+D→人造羊毛的反应方程式
(4)有机物M是乙醇的催化氧化产物。M与A以任意比例混合Xmol,完全燃烧后消耗氧气的物质的量为mol
取0.1 mol某烃M在足量的氧气中完全燃烧,生成的CO2气体在标准状况下体积为13.44L,生成的H2O与CO2的物质的量之比为1:1,则:
(1)烃M的化学式为;
(2)若烃M能使溴水或高锰酸钾溶液褪色,在一定条件下与H2加成生成2,2-二甲基丁烷,则烃M的结构简式为;M与HCl加成的产物有种;
(3)若烃M不能使溴水或高锰酸钾溶液褪色,但在一定条件下,可以和溴蒸汽发生取代反应,其一溴取代物只有一种,则烃M的结构简式为,名称是
正确书写下列化学用语:
(1)电子式:氯仿(2)结构简式:TNT;
(3)结构式:甘油。
(4)化学方程式:
①2-溴丙烷与Na0H溶液共热:;
②乙二醇催化氧化的反应: 。
。
在离子晶体中,阴阳离子按一定规律在空间排列,如图(1)所示即是NaCl的晶体结构,这两种离子在空间三个互相垂直的方向上都是等距离排列的。
①在晶体中,每个Na+离子周围与它最接近的、且距离相等的Cl-共有 个。
每个Na+离子周围与它最接近的、且距离相等的Na+共有 个。而Na+离子数目与Cl-离子数目之比为 。
②在离子晶体中,阴阳离子具有球对称的电子云。它们可以被看成是不等径的刚性圆球,并彼此相切(如图⑵所示)。离子键的键长是相邻阴阳离子的半径之和(如图⑶所示),已知a为常数。

|