煤是重要的能源,也是生产化工产品的重要原料。试用所学知识,解答下列问题:
(1)煤的转化技术包括煤的气化技术和液化技术。煤的液化技术又分为________和________。
(2)在煤燃烧前需对煤进行脱硫处理。煤的某种脱硫技术的原理为FeS2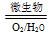 Fe2++SO42—
Fe2++SO42—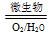 Fe3+这种脱硫技术称为微生物脱硫技术。该技术的第一步反应的离子方程式为_____________________________,
Fe3+这种脱硫技术称为微生物脱硫技术。该技术的第一步反应的离子方程式为_____________________________,
第二步反应的离子方程式为____________________。
(3)工业煤干馏得到的产品有焦炭、________。
(4)工业上主要采用氨氧化法生产硝酸,如图是氨氧化率与氨-空气混合气中氧氨比的关系。其中直线表示反应的理论值;曲线表示生产实际情况。当氨氧化率达到100%,理论上r[n(O2)/n(NH3)]=________,实际生产要将r值维持在1.7~2.2之间,原因是__________________________________________。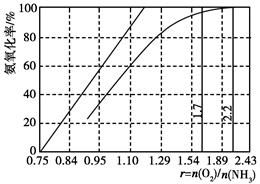
常温下由三种短周期元素形成的气体单质X、Y、Z,并有下列转化关系(反应条件已略去):
已知:X分子中含共价键最多;甲分子中含10个电子,乙分子含有18个电子。
(1)写出单质X的结构式是___________________________________;
(2)化合物甲的电子式是___________________________________;
已知工业上合成氨的反应为:N2(g)+3H2(g) 2NH3(g) △H<0。在一体积为2L的密闭容积中,加入0.20mol的N2和0.60mol的H2,反应中NH3的物质的量浓度的变化情况如图所示,
2NH3(g) △H<0。在一体积为2L的密闭容积中,加入0.20mol的N2和0.60mol的H2,反应中NH3的物质的量浓度的变化情况如图所示,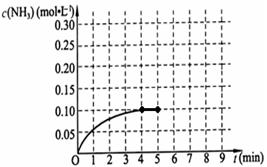
请回答下列问题:
(1) 写出该反应平衡常数的表达式K="_____"
(2)反应进行到4分钟到达平衡。请计算从反应开始到刚刚平衡,平均反应速率v(NH3)为;
(3)5分钟时,保持其它条件不变,把容器的体积缩小一半,平衡移动(填“向逆反应方向”、“向正反应方向”或“不”)。化学平衡常数将(填“增大”、“减少”或“不变”)。
(4)N2和H2的反应还有其它应用。如:有人设想寻求合适的催化剂和电极材料,分别以N2、H2为电极反应物,以HCl—NH4Cl溶液为电解质溶液制造新型燃料电池,试写出该电池的正极电极反应式。
某二元酸(化学式用H2A表示)在水中的电离方程式是:H2A===H++HA-HA- H++A2-回答下列问题:
H++A2-回答下列问题:
(1)Na2A溶液显____(填“酸性”、“中性”或“碱性”),理由是:______(用离子方程式或必要的文字说明)。
(2)常温下,已知0.1 mol·L-1 NaHA溶液pH=2,则0.1 mol·L-1 H2A溶液中氢离子的物质的量浓度可能_______0.11 mol·L-1(填“大于”、“等于”或“小于”),理由是______。
(3)0.1 mol·L-1 NaHA溶液中各种离子浓度由大到小的顺序是_______ ___。
依据题目要求回答下列问题。
(1)常温下,浓度均为 0.l mol·L-1的下列六种溶液的pH如下表:
| 溶质 |
CH3COONa |
NaHCO3 |
Na2CO3 |
NaClO |
NaCN |
C6H5ONa |
| pH |
8.8 |
9.7 |
11.6 |
10.3 |
11.1 |
11.3 |
①上述盐溶液中的阴离子,结合H+能力最强的是。
②浓度均为0.0l mol·L-1的下列五种物质的溶液中,酸性最强的是(填编号);将各溶液分别稀释100倍,pH变化最小的是(填编号)
A. HCN B. HClO C. C6H5OH D. CH3COOH E. H2CO3
③据上表数据,请你判断下列反应不能成立的是(填编号)
A. CH3COOH + Na2CO3 = NaHCO3 + CH3COONa
B. CH3COOH + NaCN = CH3COONa + HCN
C. CO2 + H2O + NaClO = NaHCO3 + HClO
D. CO2 + H2O + 2C6H5ONa = Na2CO3 + 2C6H5OH
④要增大氯水中HC1O的浓度,可向氯水中加入少量的碳酸氢钠溶液,反应的离子方程式为。
(2)已知常温下Cu(OH)2的Ksp=2×10—20。又知常温下某CuSO4溶液里 c(Cu2+)=0.02mol·L-1,如果要生成Cu(OH)2沉淀,则应调整溶液pH大于_。
A与B反应生成C,假定反应由A、B开始,它们的起始浓度均为1 mol.L-1。反应进行2min后,A的浓度为0.8 mol.L-1 ,B的浓度为0.6 mol.L-1 C的浓度为0.6 mol.L-1
(1)2min内反应的平均反应速率为: ν(A)=
(2)ν(A)、ν(B)、ν(C) 三者之间的关系是:
(3)该反应的化学反应方程式: