CuCl2溶液中的铜主要以Cu (H2O)42+、CuCl42-形式存在,它们间有如下转化关系:Cu(H2O)42+(蓝色)+4Cl- CuCl42-(黄色)+4H2O;电解不同浓度的CuCl2溶液,均可看做Cu2+、Cl-直接放电。下图为电解浓度较大CuCl2溶液的装置,实验开始后,观察到丙中的KI-淀粉溶液慢慢变蓝。回答下列问题:
CuCl42-(黄色)+4H2O;电解不同浓度的CuCl2溶液,均可看做Cu2+、Cl-直接放电。下图为电解浓度较大CuCl2溶液的装置,实验开始后,观察到丙中的KI-淀粉溶液慢慢变蓝。回答下列问题:
(1)甲电极的电极反应式为_________________。
(2)丙中溶液变蓝是乙电极产物与KI反应导致的,该反应的化学方程式为_________________。
(3)随电解的不断进行,U型管中溶液的颜色变化为__________;
A.由黄色变为浅蓝色 B.由蓝色变为浅黄色
溶液颜色变化的原因是_________________。
(4)当电解到一定程度,甲电极附近出现蓝色Cu(OH) 2絮状物。经测,甲电极附近溶液的pH=a,此时甲电极附近溶液中c(Cu2+)=______ mol·L-1。(已知:Cu(OH) 2的Ksp=2.2×10-20)。
(5)电解较长时间后,丙中溶液的蓝色又会褪去,这是因为乙电极产物进一步将I2氧化为IO3-。该反应的离子方程式为______________。
(16分)对于甲、乙、丙、丁、戊五种溶液有如下信息:
①分别NH4+、Na+、Al3+、Ba2+、Ag+和NO3-、Cl-、SO42-、Br-、CO32-离子中的各一种组成(不重复)。
②其中甲、丙、戊三种溶液呈酸性,乙溶液呈碱性。
③甲、乙反应生成白色沉淀和气体,丁可分别与甲、乙、丙反应生成白色沉淀。
请回答下列问题:
⑴用化学式表示出各物质:乙、丁。
⑵请用离子方程式表示戊溶液呈酸性的原因:。
⑶请用离子方程式表示甲与乙的反应:。
⑷检验甲溶液中甲的阴离子的方法是先加试剂,再加试剂,观察到
现象,证明该阴离子存在。
⑸若丙、丁形成的白色沉淀的溶度积常数Ksp=1.8×10-20,则将1 L 1mol/L的丙溶液与1 L 1 mol/L的丁溶液混合充分反应后,不考虑溶液混合时的微小体积变化,形成沉淀的阳离子的浓度约为mol/L。
以下是依据一定的分类标准,对某些物质与水反应情况进行分类的分类图。请根据你所学的知识.按要求填空: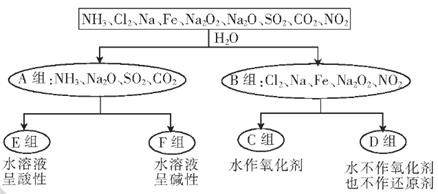
(1)上述第一级分类标准(分成A、B组的依据)是________________________________
(2)D组物质包括________________________(填化学式)。
(3)C组物质中某一物质在常温时能与冷水反应,其化学方程式为___________
(4)F组物质中某一物质的水溶液呈弱碱性,用电离方程式表示呈弱碱性的原因: _________
(5)D组中某一物质与E组中某一物质在水中反应生成两种强酸,写出该反应的离子方程式: _______________________________________________________
(1)一个体重50 kg的健康人身体中含铁2 g。铁在人体中不是以游离态的形式存在,而是以Fe2+和Fe3+形式存在。Fe2+易被吸收,给贫血者补充铁时,应给予含Fe2+的盐,如硫酸亚铁(FeSO4)。服用维生素C,可使食物中的Fe3+转化为Fe2+,利于铁的吸收,该过程中维生素C做剂,Fe3+作剂,维生素C的还原性______于 Fe2+(填“强”“弱”)
(2)在热的稀硫酸溶液中溶解了11.4 g FeSO4。当加入50 mL 0.5 mol/L KNO3溶液后,使其中的Fe2+全部转化成Fe3+,KNO3也反应完全,并有NxOy氮氧化物气体逸出。
____FeSO4 + KNO3 + H2SO4 =K2SO4 + Fe2(SO4)3 + NxOy + H2O
①配平该化学方程式,用单线桥标出电子转移的方向和数目。
②反应中氧化剂为,氮氧化物的化学式为__________
(3)羟胺(NH2OH)是一种还原剂,用25.00 mL 0.049 mol/L羟胺的酸性溶液跟足量的硫酸铁溶液在煮沸条件下反应,生成的Fe2+离子恰好与24.5 mL 0.020 mol/L的KMnO4酸性溶液反应。则在上述反应中, Fe2+离子与酸性高锰酸钾反应的离子方程式为:________________________。羟胺的氧化产物是。
(4分)氮元素的氢化物和氧化物在工业生产和国防建设中都有广泛应用,回答下列问题:
(1)NH3与NaClO反应可得到肼(N2H4),该反应的化学方程式为;
(2)肼可作为火箭发动机的燃料,与氧化剂N2O4反应生成N2和水蒸气。
已知:①N2(g)+2O2(g)= N2O4 (1)△H1= -195kJ·mol-1
②N2H4 (1) + O2(g)= N2(g) + 2 H2O△H2= -534.2kJ·mol-1
写出肼和N2O4反应的热化学方程式;
X、Y、Z、M、G五种元素分属三个短周期,且原子序数依次增大。X、Z同主族,可形成离子化合物ZX;Y、M同主族,可形成MY2、MY3两种分子。回答下列问题:
⑴ Y在元素周期表中的位置为________________。
⑵上述元素的最高价氧化物对应的水化物酸性最强的是_______________(写化学式),非金属气态氢化物还原性最强的是__________________(写化学式)。
⑶ Y、G的单质或两元素之间形成的化合物可作水消毒剂的有___________(写出其中两种物质的化学式)。
⑷ X2M的燃烧热ΔH=-a kJ·mol-1,写出X2M燃烧反应的热化学方程式:___。
⑸ ZX的电子式为___________;ZX与水反应放出气体的化学方程式__________________。