某芳香族化合物A的分子中含有C、H、 O、N四种元素,相同状况下,其蒸气的密度氢气密度的68.5倍。现以苯为原料合成A,并最终制得F(一种染料中间体),转化关系如下:
请回答下列问题:
(1)写出A的分子式_______________;A的结构简式_____________________。
(2)N-A的反应类型是__________________。
(3)①上述转化中试剂I和试剂II分别是:试剂I_________,试剂II__________(选填字母)。
a.KMnO4(H+) b.Fe/盐酸 c.NaOH溶液
②若上述转化中物质A依次与试剂Ⅱ、试剂I、化合物E(浓硫酸/△)作用,能否得到F,为什么?______________________________________________________________。
(4)用核磁共振氢谱可以证明化合物E中含有________种处于不同化学环境的氢。
(5)写出同时符合下列要求的两种D的同分异构体的结构简式_________________。
①嘱于芳香族化合物,分子中有两个互为对位的取代基,其中—个取代基是硝基;
②分子中含有 结构。
结构。
(6)有一种D的同分异构体W,在酸性条件下水解后,可得到一种能与溶液发生显色反应的产物,写出W在酸性条件下水解的化学方程式_________________________。
(7)F的水解反应如下: 
化合物H在一定条件下经缩聚反应可制得高分子纤维,广泛用于通讯、导弹、宇航等领域。请写出该缩聚反应的化学方程式____________________________________________。
按要求完成下列各题
(1)、精炼铜时,阴极材料是 ,阴极的电极反应式是 ,
(2)、氯碱工业电解饱和食盐水的总反应方程式为 。
(3)、MnO2可作超级电容器材料。用惰性电极电解MnSO4溶液可制得MnO2,其阳极的电极反应式是
(4)、为提高甲醇燃料的利用率,科学家发明了一种燃料电池,电池的一个电极通入空气,另一个电极通入甲醇气体,电解质是掺入了Y2O3的ZrO2晶体,在高温下它能传导O2-离子。电池工作时正极反应式为________________。
若以该电池为电源,用石墨做电极电解100 mL含有如下离子的溶液。
| 离子 |
Cu2+ |
H+ |
Cl- |
SO |
| c/(mol·L-1) |
1 |
4 |
4 |
1 |
电解一段时间后,当两极收集到相同体积(相同条件)的气体时(忽略溶液体积的变化及电极产物可能存在的溶解现象),阳极上收集到氧气的物质的量为________mol。
高炉炼铁过程中发生的主要反应为:1/3Fe2O3(s)+CO(g) 2/3Fe(s)+CO2(g)
2/3Fe(s)+CO2(g)
已知该反应在不同温度下的平衡常数如下:
| 温度/℃ |
1000 |
1150 |
1300 |
| 平衡常数 |
4.0 |
3.7 |
3.5 |
(1)该反应的平衡常数表达式K=________ ,ΔH________0(填“>”、“<”或“=”);
(2)在一个容积为5L的密闭容器中,1000℃时加入Fe、Fe2O3、CO、CO2各1.0mol,此时比较v(正) v(逆) (填“>” “="”" “<”),反应经过2min后达到平衡。求该时间范围内反应的平均反应速率v(CO2)=________ ,CO的平衡转化率=________ ;
(3)欲提高(2)中CO的平衡转化率,可采取的措施是________。
A、减少Fe的量 B、增加Fe2O3的量 C、移出部分CO2
D、提高反应温度 E、减小容器的容积 F、加入合适的催化剂
在一定条件下,A气体与B气体反应生成C气体。反应过程中,反应物与生成物的浓度随时间变化的曲线如图,则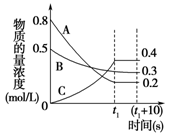
(1)、该反应的化学方程式为: ;
(2)、t1 s时反应物A的转化率为: ;
(3)、0~t1 s内A的反应速率为v(A)= ;
按要求回答下列问题
(1)、4g CO在氧气中燃烧生成CO2,放出 9. 6kJ热量,写出CO燃烧的热化学方程式。_____________________________
(2)、已知拆开1 mol H—H键、1 mol N—H键、1 mol N≡N键分别需要的能量是436 kJ、391 kJ、946 kJ,则N2与H2反应生成NH3的热化学方程式为________________________
(3)、已知碳的燃烧热ΔH1=" a" kJ·mol-1S(s)+2K(s)==K2S(s)ΔH2=" b" kJ·mol-1
2K(s)+N2(g)+3O2(g)==2KNO3(s)ΔH3=" c" kJ·mol-1
则S(s)+2KNO3(s)+3C(s)==K2S(s)+N2(g)+3CO2(g) ΔH=
(4)、已知:C(s)+O2(g)=CO2(g)ΔH="-437.3" kJ·mol一1
H2(g)+1/2O2(g)=H2O(g)ΔH="-285.8" kJ·mol一1
CO(g)+1/2O2(g)=CO2(g)ΔH="-283.0" kJ·mol一1
写出煤气化(碳和水蒸气反应生成一氧化碳和氢气)的热化学方程式
计算10m3(标况)水煤气完全燃烧放出的热量为 kJ(结果保留到小数点后一位)。
已知25 ℃、101 kPa条件下:4Al(s)+3O2(g) 2Al2O3(s);ΔH="-2" 834.9 kJ·mol-1
2Al2O3(s);ΔH="-2" 834.9 kJ·mol-1
4Al(s)+2O3(g) 2Al2O3(s);ΔH="-3" 119.1 kJ·mol-1
2Al2O3(s);ΔH="-3" 119.1 kJ·mol-1
(1)、写出O3转化成O2的热化学方程式
(2)、2molO3的能量 3molO2的能量(填“>” “="”" “<”)
(3)、2molO3的键能 3molO2的键能(填“>” “="”" “<”)
(4)、稳定性O3 O2(填“>” “<”)