亚氯酸钠(NaClO2)是一种高效氧化剂、漂白剂。已知:NaClO2饱和溶液在温度低于38oC时析出的晶体是NaClO2·3H2O,高于38oC时析出晶体是NaClO2,高于60oC时NaClO2分解成NaClO3和NaCl。利用下图所示装置制备亚氯酸钠。装置②反应容器为三颈烧瓶。
完成下列填空:
(1)组装好仪器后,检查整套装置气密性的操作是: 。
(2)装置②中产生ClO2的化学方程式为 。
装置④中发生反应的离子方程式为 。
(3)从装置④反应后的溶液获得NaClO2晶体的操作步骤为:
①减压,55oC蒸发结晶;② ;③ ;④低于60oC干燥,得到成品。
(4)目前已开发出用电解法制取ClO2的新工艺。
①上图是用石墨作电极,一定条件下电解饱和食盐水制取ClO2的示意图。则阳极产生C1O2的电极反应为 。
②电解一段时间,当阴极产生的气体体积为112 mL(标准状况)时,停止电解。通过阳离子交换膜的阳离子的物质的量为 mol。
(5)准确称取所得亚氯酸钠样品l0 g于烧杯中,加入适量蒸馏水和过量的碘化钾晶体,再滴入适量的稀硫酸,充分反应(ClO2-+4I-+4H+=2H2O+2I2+C1-)。将所得混合液配成250 mL待测溶液。配制待测液需用到的定量玻璃仪器是 ;取25.00 mL待测液,用2.0mol·L-1Na2S2O3标准液滴定(I2+2S2O32-=2I-+S4O62-),以淀粉溶液做指示剂,达到滴定终点时的现象为 。重复滴定2次,测得Na2S2O3溶液平均值为20.00 mL。该样品中NaClO2的质量分数为 。
氯化硼的熔点为-107℃,沸点为12.5℃,在其分子中键与键之间的夹角为120°,它能水解,有关叙述正确的是( )
| A.氯化硼液态时能导电而固态时不导电 | B.硼原子以sp杂化 |
| C.氯化硼遇水蒸气会产生白雾 | D.氯化硼分子属极性分子 |
某有机物X(C12H14O7)的分子中含有多种官能团,其结构简式为:
(其中R1、R2为未知部分的结构),已知X可以发生如图所示的转化: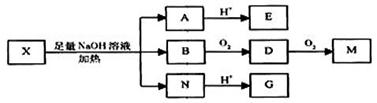
已知1)向X、E的水溶液中滴入FeCl3溶液均发生显色反应; 2)E的核磁共振谱图中只有两个峰,面积比为1:2; 3)G、M(C2H2O4)都能与NaHCO3溶液反应。
(1)写出X的结构简式为。
(2)1molX与NaOH溶液反应时,消耗mol NaOH。
(3)E的结构简式是;B的命名为_____________________
①写出B转化成D的化学方程式:___________ __________
②写出A溶液与CO2反应的离子方程式:________________ _________。
H与G互为同分异构体,H的分子中只含有醛基、羧基、羟基三种官能团,且同一个碳原子上不 能同时连有两个羟基,则H的分子结构有______种.
有机合成中增长碳链是一个重要环节。如下列反应: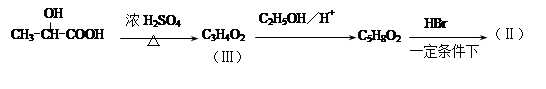
用 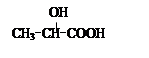 通过以下路线可合成(Ⅱ):
通过以下路线可合成(Ⅱ):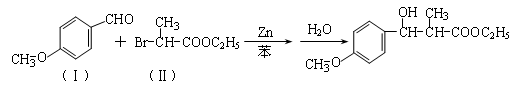
(1)(Ⅰ)的分子式为;(Ⅲ)的结构简式为。
(2)(Ⅱ)与足量的热NaOH溶液反应的化学方程式为。
(3)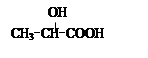 在生成(Ⅲ)时,还能得到另一种副产物C6H8O4,该反应的化学方程式为,反应类型是。
在生成(Ⅲ)时,还能得到另一种副产物C6H8O4,该反应的化学方程式为,反应类型是。
(4)(Ⅰ)的一种同分异构体(Ⅳ)能发生银镜反应,还能水解生成不含甲基的芳香化合物。(Ⅳ)的结构简式为。
有机物B,其相对分子质量为46,其中碳的质量分数为52.2%,氢的质量分数为13.0%。其余为氧。A的产量可以衡量一个国家石油化工发展水平。 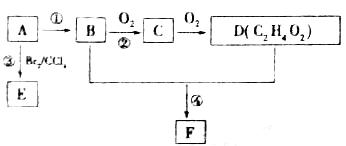
(1)B的分子式是。A的结构简式。
(2)B能与金属钠反应放出氢气,则B结构中含有的官能团的电子式为。
(3)反应②在Cu作催化剂的条件下进行,其现象是。该反应的化学方程式为。
(4)反应①的反应类型是。反应③的化学方程式为。
(5)B与高锰酸钾酸性溶液反应可生成D。在加热和浓硫酸作用下,B与D反应可生成一种有香味的物质F,若184 g B和120 g D反应能生成132g F,该反应的化学方程式为,其中B的转化率为。
肉桂酸甲酯是常用于调制具有草莓、葡萄、樱桃、香子兰等香味的食用香精。它的分子式为C10H10O2,且分子中只含有1个苯环,苯环上只有一个取代基。已知某一种肉桂酸甲酯的分子结构模型如下图所示(图中球与球之间连线表示单键或双键)。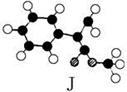
试回答下列问题。
肉桂酸甲酯的结构简式为。(2)分子中的官能团的名称为。
(3)在苯环上的一氯代物有种。
(4)写出该肉桂酸甲酯在氢氧化钠溶液中水解的化学方程式:_________________________。