2008年,三鹿等多家乳制品企业为使蛋白质含量检测合格而加入三聚氰胺,使多名儿童患肾结石,实验室可用下列实验装置测定三聚氰胺的分子式。
已知三聚氰胺的相对分子质量为126。取1.26 g三聚氰胺样品,放在纯氧中充分燃烧,生成CO2、H2O、N2,实验测得装置B增重0.54 g,C增重1.32g,排入F中水的体积为672 mL(可按标准状况计算)。
(1)E装置的作用是_____________。
(2)需要加热的装置是____________(填字母代号)。
(3)装置D的作用是_________________________________。
(4)F处读数时应该注意:____________、____________。
(5)三聚氰胺的分子式为_________________。
Ⅰ.实验室用燃烧法测定某种氨基酸(CxHyOzNp)的分子组成。取w g该种氨基酸放在纯氧中充分燃烧,生成CO2、H2O和N2。现用图示装置进行实验(铁架台、铁夹、酒精灯等未画出)请回答下列有关问题: 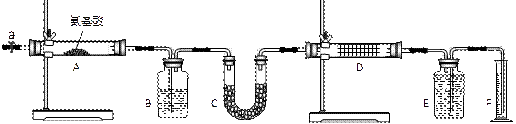
(1)写出装置B、C、D中分别盛放的试剂。
B C D
(2)检查装置气密性,进行如下操作后A中氨基酸开始反应,请用序号表示正确的操作顺序。
实验操作:①使用酒精灯加热A处;②使用酒精灯加热D处;③打开活塞a,通入氧气; ④关闭活塞a,记录F装置的液面读数。
(3)样品氨基酸充分燃烧后,待E装置气体冷却至室温后记录F装置的液面读数,请指出读数时应注意的问题。
。
(4)通过该实验所能测定的数据,能否确定该氨基酸的分子式?请说明理由。
,。
Ⅱ.某校兴趣小组的同学进行铁与水蒸气的实验。甲同学直接采用铁钉与水蒸气利用下述左图装置进行实验,最后试图收集气体于试管C中。乙同学先用右图装置进行CO还原Fe2O3,至硬质管中固体由红色转变成黑色,用磁铁进行试验,发现能被吸引,D中出现浑浊;乙同学随即熄灭酒精灯,继续通过CO冷却至室温,然后用所得固体进行甲的实验。
某学生用标准的0.2mol/L的盐酸滴定待测的NaOH溶液,其实验操作如下:
| A.用碱式滴定管取待测液NaOH溶液放入锥形瓶,滴加2—3滴酚酞指示剂。 |
| B.用待测的NaOH溶液润洗碱式滴定管。 |
| C.把滴定管用蒸镏水洗净。 |
| D.取下酸式滴定管,用标准的盐酸溶液润洗后,再将标准的盐酸注入酸式滴定管至刻 |
度“0”以上2cm—3cm处,把酸式滴定管固定好,调节液面。
E.检查滴定管是否漏水,并分别固定在滴定管架两边。
F.另取锥形瓶,再重复滴定操作一次。
G.把锥形瓶放在酸式滴定管的下面,瓶下垫一张白纸,然后边滴定边摇动锥形瓶,直
至终点,记下滴定管的液面所在刻度。
据上述滴定操作,完成下列填空:
⑴滴定操作的正确操作顺序是(用上述各编号字母填写)
→E→→B→→→;
⑵ G步操作中判断滴定终点的依据是;
⑶ D步骤的操作中液面应调节到,尖嘴部分应;
⑷酸式滴定管未用标准的盐酸润洗,待测溶液NaOH的测定值会;
碱式滴定管未用待测的NaOH溶液润洗,待测NaOH溶液的测定值会。
(填“偏高”、“偏低”或“无影响”。)
图Ⅰ是化学实验室中常用制备、干燥气体的部分仪器装置。某学校同学利用中学常用试剂及仪器设计下列实验。
(1)甲同学利用图Ⅰ装置制备并收集干燥的NO2气体,
请完成下列问题:
①图Ⅰ中仪器B的名称:_______________________;
②收集NO2的方法;
③B中发生反应的离子方程式为_____________________________。
④将收集满NO2的集气瓶浸入冰水中,烧瓶内气体颜色(填“变深”、“不
变”或“变浅”),使用化学用语和必要的文字说明颜色变化的原因_________。
(2)乙同学利用图Ⅰ装置制取氨气和氧气的混合气体,并且利用图Ⅱ装置验证氨的某些性质。A中加入浓氨水,B中加入过氧化钠固体,C中加入碱石灰,E内放置催化剂(铂石棉),按气流方向连接各仪器 a → b→ c→ h。请完成下列问题: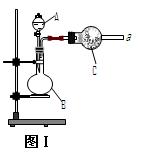
 ①实验中观察
①实验中观察 到E内有红棕色气体出现,证明氨气具有_________性;
到E内有红棕色气体出现,证明氨气具有_________性;
②E中发生反应的化学方程式为_______________________________。
(10分)某课外小组设计的实验室制取乙酸乙酯的装置如图所示,A中放有浓硫酸,B中放有乙醇、无水醋酸钠,D中放有饱和碳酸钠溶液。
已知
①无水氯化钙可与乙醇形成难溶于水的CaCl2·6 C2H50H
②有关有机物的沸点:
| 试剂 |
乙醚 |
乙醇 |
乙酸 |
乙酸乙酯 |
| 沸点/℃ |
34.7 |
78.5 |
118 |
77.1 |
请回答:
(1)浓硫酸的作用是;若用同位素180示踪法确定反应产物水分子中氧原子的提供者,写出能表示180位置的化学方程式:
(2)球形干燥管C的作用是。若反应前向D中加入几滴酚酞,溶液呈红色,产生此现象的原因是(用离子方程式表示);反应结束后D中的现象是。
(8分)某化学课外小组用海带为原料制取了少量碘水。现用CCl4从碘水中萃取碘并用分液漏斗分离两种溶液。其实验操作可分解为如下几步:
| A.把盛有溶液的分液漏斗放在铁架台的铁圈中; |
| B.把50 mL碘水和15 mL CCl4加入分液漏斗中,并盖好玻璃塞; |
| C.检验分液漏斗活塞和上口的玻璃塞是否漏液; |
| D.倒转漏斗用力振荡,并不时旋开活塞放气,最后关闭活塞,把分液漏斗放正; |
(E)旋开活塞,用烧杯接收溶液:
(F)从分液漏斗上口倒出上层水溶液;
(G)将漏斗上口的玻璃塞打开或使塞上的凹槽或小孔对准漏斗口上的小孔;
(H)静置,分层。
就此实验,完成下列填空。
(1) 正确操作步骤的顺序是:(用上述各操作的编号字母填写)
_____® _____® _____® A ® G ® _____ ® E ® F
(2) 上述(E)步骤接收溶液时应注意
(3) 能选用CCl4从碘水中萃取碘的原因是