含有农药、染料、酚、氰化物,以及引起色度、臭味的废水,常用化学氧化法进行处理,所用的氧化剂有氯类(如液氯、次氯酸钙、次氯酸钠等)和氧类(如空气、臭氧、过氧化氢、高锰酸钾等)。一个典型实例是用氯氧化法处理含有剧毒的氰化物(含CN-)的废水。在碱性条件下(pH=8.5~11),氯气可将氰化物中CN-氧化为只有它毒性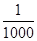 的氰酸盐(含CNO-)。
的氰酸盐(含CNO-)。
(1)写出含CN-废水用氯气氧化生成氰酸盐的离子方程式:________________________________________________________________。
(2)若向含CNO-的废水中再通入氯气,可使CNO-转化为无毒的气体,写出这个反应的离子方程式:______________________________________________。
(3)在用液氯不便的地区,可用漂白粉处理含CN-的废水,若将其氧化为CNO-,其离子方程式为__________________________________________。
钴酸锂(LiCoO2)锂离子电池是一种应用广泛的新型电源,实验室尝试利用废旧钴酸锂锂离子电池回收铝、铁、铜、钴、锂元素,实验过程如下: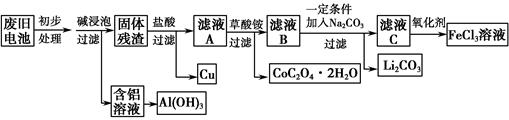
(1)碱浸泡过程中,铝被溶解的离子方程式为__________________________
(2)滤液A中加入草酸铵溶液,使Co元素以CoC2O4·2H2O沉淀形式析出。草酸钴是制备氧化钴及钴粉的重要原料。在空气中CoC2O4·2H2O的热分解失重数据见下表,请补充完整表中的热分解方程式。
| 序号 |
温度范围/℃ |
热分解方程式 |
固体失重率 |
| ① |
120~220 |
19.67% |
|
| ② |
280~310 |
56.10% |
(3)过滤Li2CO3时发现滤液中有少量浑浊,从实验操作的角度给出两种可能的原因:_____________________________________________________________
(4)最终所得的FeCl3溶液可作净水剂,试结合离子方程式解释其净水原理________________________________________________________
(1)已知:H2(g)+1/2O2(g)=H2O(l) ΔH=-285.8 kJ·mol-1
H2(g)=H2(l) ΔH=-0.92 kJ·mol-1
O2(g)=O2(l) ΔH=-6.84 kJ·mol-1
H2O(l)=H2O(g) ΔH=+44.0 kJ·mol-1
请写出液氢和液氧反应生成气态水的热化学方程式:__________________________
电解质溶液为KOH溶液的氢氧燃料电池,其负极的电极反应式为____________________________________。
(2)如图表示373 K时,反应A(g)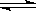 2B(g)在前110 s内的反应进程。
2B(g)在前110 s内的反应进程。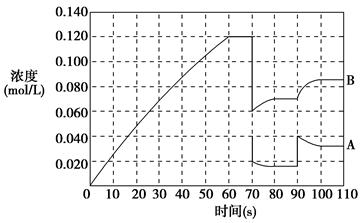
①此反应的平衡常数表达式K=________。
②373 K时反应进行到70 s时,改变的条件可能是________,反应进行到90 s时,改变的条件可能是________。
| A.加入催化剂 | B.扩大容器体积 | C.升高温度 | D.增大A的浓度 |
③请在图中画出反应物A在0~70 s时的浓度变化曲线。
2013年春季,全国各地持续出现严重的雾霾天气,给人们的生产、生活造成了严重的影响。汽车尾气中含有CO、氮氧化物、烟尘等污染物,是导致雾霾天气的原因之一。请回答下列有关问题。
(1)下列说法正确的是________。
A.NO、CO、CO2均为酸性氧化物
B.CO2的大量排放会导致温室效应,所以应尽量选用公共交通,提倡低碳出
行
C.汽车尾气中的氮氧化物主要是空气中的氮气与氧气在高温条件下生成的
(2)为减轻污染,北京为汽车加装了“三效催化净化器”,可将尾气中的CO、NO转化为参与大气循环的无毒混合气体,反应如下:2NO+2CO N2+2CO2,则该反应的化学平衡常数表达式K=________。
N2+2CO2,则该反应的化学平衡常数表达式K=________。
(3)已知下列热化学方程式:
N2(g)+O2(g)=2NO(g) ΔH=+180.5 kJ·mol-1①
2C(s)+O2(g)=2CO(g) ΔH=-221.0 kJ·mol-1②
C(s)+O2(g)=CO2(g) ΔH=-393.5 kJ·mol-1③
则汽车尾气转化反应2NO(g)+2CO(g) N2(g)+2CO2(g)的ΔH=________。
N2(g)+2CO2(g)的ΔH=________。
(4)当固体催化剂质量一定时,增大其表面积可加快化学反应速率。如图表示在其他条件不变时,反应2NO(g)+2CO(g) N2(g)+2CO2(g)中NO的浓度[c(NO)]随温度(T)、催化剂表面积(S)和时间(t)的变化曲线。
N2(g)+2CO2(g)中NO的浓度[c(NO)]随温度(T)、催化剂表面积(S)和时间(t)的变化曲线。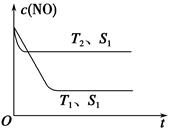
①图中T1________T2(填“>”或“<”)。
②若催化剂的表面积S1>S2,在图中画出c(NO)在T1、S2条件下达到平衡过程中的变化曲线。
(5)低温脱硝技术可用于处理各种废气中的氮氧化物,发生的化学反应为2NH3(g)+NO(g)+NO2(g) 2N2(g)+3H2O(g) ΔH<0。在恒容的密闭容器中,下列有关说法正确的是________。
2N2(g)+3H2O(g) ΔH<0。在恒容的密闭容器中,下列有关说法正确的是________。
A.反应中每转移3 mol电子,生成标准状况下N2的体积为22.4 L
B.平衡时,若其他条件不变,增大NH3的浓度,废气中氮氧化物的转化率
减小
C.因为反应物比生成物的物质的量少,所以反应物比生成物的能量低
D.其他条件不变时,使用高效催化剂,废气中氮氧化物的转化率增大
二甲醚(CH3OCH3)被称为21世纪的新型燃料,在未来可能替代汽车燃油、石油液化气、城市煤气等,市场前景极为广阔。它清洁、高效,具有优良的环保性能。
工业上制二甲醚是在一定温度(230~280 ℃)、压强(2.0~10.0 MPa)和催化剂作用下进行的,反应器中发生了下列反应。
CO(g)+2H2(g)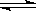 CH3OH(g) ΔH1=-90.7 kJ·mol-1 ①
CH3OH(g) ΔH1=-90.7 kJ·mol-1 ①
2CH3OH(g)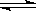 CH3OCH3(g)+H2O(g) ΔH2=-23.5 kJ·mol-1 ②
CH3OCH3(g)+H2O(g) ΔH2=-23.5 kJ·mol-1 ②
CO(g)+H2O(g)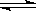 CO2(g)+H2(g)ΔH3=-41.2 kJ·mol-1 ③
CO2(g)+H2(g)ΔH3=-41.2 kJ·mol-1 ③
(1)反应器中的总反应可表示为3CO(g)+3H2(g)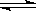 CH3OCH3(g)+CO2(g),则该反应的ΔH=__________,平衡常数表达式为____________________,在恒温、可变容积的密闭容器中进行上述反应,增大压强,二甲醚的产率会________(填升高、降低或不变)。
CH3OCH3(g)+CO2(g),则该反应的ΔH=__________,平衡常数表达式为____________________,在恒温、可变容积的密闭容器中进行上述反应,增大压强,二甲醚的产率会________(填升高、降低或不变)。
(2)二氧化碳是一种重要的温室气体,减少二氧化碳的排放是解决温室效应的有效途径。目前,由二氧化碳合成二甲醚的研究工作已取得了重大进展,其化学反应方程式为2CO2(g)+6H2(g)CH3OCH3(g)+3H2O(g) ΔH>0。
该反应在恒温、体积恒定的密闭容器中进行,下列不能作为该反应已达到化学平衡状态的判断依据的是________。
A.容器内混合气体的密度不变
B.容器内混合气体的压强保持不变
C.容器内混合气体的平均摩尔质量保持不变
D.单位时间内消耗2 mol CO2的同时消耗1 mol二甲醚
(3)二甲醚气体的燃烧热为1 455 kJ·mol-1,工业上用合成气(CO、H2)直接或间接合成二甲醚。下列有关叙述正确的是________。
A.二甲醚分子中含共价键
B.二甲醚作为汽车燃料不会产生污染物
C.二甲醚与乙醇互为同系物
D.表示二甲醚燃烧热的热化学方程式为CH3OCH3(g)+3O2(g)=2CO2(g)+3H2O(g) ΔH=-1 455 kJ·mol-1
(4)绿色电源“直接二甲醚燃料电池”的工作原理示意图如图所示:正极为________(填“A电极”或“B电极”),写出A电极的电极反应式:________________________________________。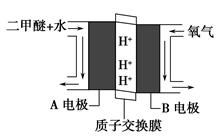
多晶硅是太阳能光伏产业的重要原材料。
(1)由石英砂可制取粗硅,其相关反应的热化学方程式如下:
SiO2(s)+C(s)=SiO(g)+CO(g) ΔH=a kJ·mol-1
2SiO(g)=Si(s)+SiO2(s) ΔH=b kJ·mol-1
①反应SiO2(s)+2C(s)=Si(s)+2CO(g)的ΔH=________ kJ·mol-1(用含a、b的代数式表示)。
②SiO是反应过程中的中间产物。隔绝空气时,SiO与NaOH溶液反应(产物之一是硅酸钠)的化学方程式为________________________________。
(2)粗硅提纯常见方法之一是先将粗硅与HCl制得SiHCl3,经提纯后再用H2还原:
SiHCl3(g)+H2(g)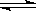 Si(s)+3HCl(g)。
Si(s)+3HCl(g)。
不同温度及不同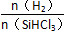 时,反应物X的平衡转化率关系如图所示。
时,反应物X的平衡转化率关系如图所示。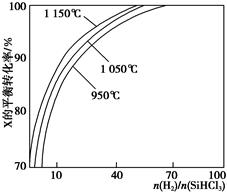
①X是________(填“H2”或“SiHCl3”)。
②上述反应的平衡常数K(1 150 ℃)________K(950 ℃)(填“>”、“<”或“=”)。
(3)SiH4(硅烷)法生产高纯多晶硅是非常优异的方法。
①用粗硅作原料,熔融盐电解法制取硅烷原理如图所示,电解时阳极的电极反应式为_________________________________________。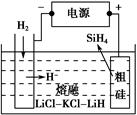
②硅基太阳电池需用N、Si两种元素组成的化合物Y作钝化材料,它可由SiH4与NH3混合气体进行气相沉积得到,已知Y中Si的质量分数为60%,Y的化学式为________。