小刚、小军、小红对一久置的NaOH白色粉末的成分进行探究并测定其成分的含量。
【成分的确定】
三位同学都作出以下的猜想:
① 可能是NaOH;② 可能是Na2CO3;③ 可能是NaOH与Na2CO3的混合物。
做出②③猜想的依据是 (用化学方程式表示)。
为了验证①②③猜想,他们分别做了下面的实验。
(1)小刚取少量白色粉末于试管中,再滴加稀HCl,有气泡产生,由此可推出白色粉末中一定含有 ,肯定猜想 (填序号)是错误的。
(2)小军又取少量白色粉末溶于水,向所得溶液中滴加酚酞试液,溶液变为红色。由此小军结合小刚的实验,认为猜想③是正确的。小红却认为小军的所得结论不确切,因为 。
(3)为探究白色粉末是否含有NaOH,小红设计了如下实验方案: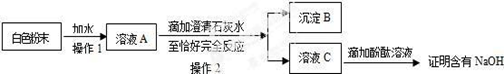
①沉淀B的化学式为 。
②在操作1中要用到玻璃棒,其作用是 。
③小刚认为小红的这个方案也有问题,理由是_ ,但只要稍加改进,就可以证明粉末中还含有NaOH,则小刚改进的方法是 。
小刚对小红的实验作了正确的改进后进行了实验,实验现象和小红的一致,由此确定猜想③是正确的。
【各成分含量的测定】 三位同学利用电子天平共同作了以下测定实验,并记录如下实验数据。
三位同学利用电子天平共同作了以下测定实验,并记录如下实验数据。
| 称量项目 |
称量时间 |
质量(g) |
| 试样 |
———— |
10.00 |
| 装置+稀硫酸质量 |
———— |
241.20 |
| 装置+稀硫酸质量+试样 |
反应开始后15秒 |
249.20 |
| 装置+稀硫酸质量+试样 |
反应开始后35秒 |
249.00 |
| 装置+稀硫酸质量+试样 |
反应开始后55秒 |
249.00 |
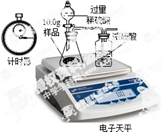

(1)写出锥形瓶中发生反应化学方程式:
① ;
② 。
(2)试通过分析表中数据计算试样中碳酸钠的质量分数。
【实验反思】
有同学提出按上述实验所测得试样中Na2CO3质量分数会偏小,该同学的理由是(实验操作均正确): (答一条即可)。
牙膏中常用碳酸钙、二氧化硅等物质作为摩擦剂.某同学对牙膏中摩擦剂碳酸钙的含量进行探究.
【实验原理】测定
装置中生成的
沉淀的质量,通过计算确定牙膏中
的质量分数.
【查阅资料】
,牙膏中其他成分遇到盐酸时无气体产生.
【实验装置】
根据探究过程回答下列问题:
(1)装置
中发生反应的化学方程式;
(2)实验过程中需持续缓缓通入空气,其作用有:①搅拌 、 中的反应物,使其充分反应;②.
(3)从 中过滤出 沉淀所需的玻璃仪器有烧杯、和玻璃棒;
(4)实验中准确称取三份牙膏样品,每份 ,进行三次测定,测得生成 的平均质量为 .则样品中 的质量分数为.
(5)若没有 装置,直接通入空气,则测得 的质量分数(填"偏大"、"偏小"或"不变").
碳酸氢钠(
)俗称"小苏打",在生活中用途广泛.某化学实验小组的同学对碳酸氢钠的性质进行探究.
【探究实验1】碳酸氢钠溶液的酸碱性
用试管取适量碳酸氢钠溶液,滴加酚酞试液,振荡,溶液变浅红色.结论:.
【探究实验2】能与酸反应
取适量碳酸氢钠加入试管中,滴加稀盐酸,再把燃着的木条迅速伸入试管,木条熄灭,碳酸氢钠和盐酸的化学反应方程式:.
【探究实验3】能与碱反应
查阅资料:
;氢氧化钙微溶于水.用试管取适量碳酸氢钠溶液,滴加氢氧化钠溶液,无明显现象.(提示:可以选择
溶液做试剂,通过证明有
生成,从而证明二者发生了反应)如图,两位同学分别进行了甲、乙两个实验.回答下列问题: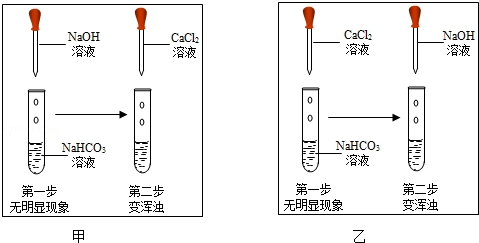
比较甲、乙两个实验的目的性区别是;
有同学提出两个实验都不足以证明有
生成,其理由;要证明有
生成,还需要进行的操作是.
一男孩在排污井盖上燃放鞭炮,点燃了排污井内的气体,井盖被炸飞,男孩被井盖击伤.
【提出问题】排污井内气体的主要成分是什么?
【查阅资料】排污井内的有机物在一定的条件下发酵产生了气体,其成分可能含有
、
、
等.
【提出猜想】某兴趣小组同学对排污井内气体含有上述气体中最少2种成分的猜想如下:
猜想Ⅰ:有
、
猜想Ⅱ:有
、
猜想Ⅲ:有
、
猜想Ⅳ:有
、
、
【实验方案】小组同学共同设计了下图所示的装置并经行探究.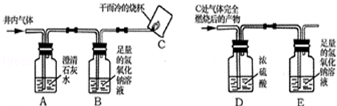
【问题讨论】
(1)装置A出现浑浊,证明猜想不正确.
(2)小明通过装置C处的现象,证明猜想Ⅲ不成立.小芳对此提出了疑义,小芳认为要在位置,再增加一个上图中(填序号)装置,才能证明猜想Ⅲ不成立.
(3)为了进一步确认气体中是否含有一氧化碳,小明将装置C处气体完全燃烧后的产物依次通过装置D、E,经实验测定装置D增重1.8g,装置E增重2.2g,由此证明猜想成立.
(4)小明认为要证明排污井内气体是否含有
,可以不用装置B,小芳则认为需要使用装置B,你认为装置B的作用是.
过氧化钠(
)为淡黄色固体,可作为潜水艇或呼吸面具的供氧剂,人呼出气体主要成分有氨气、二氧化碳、水蒸气和氧气,
能分别与
、
反应,化学方程式为:
↑;
↑.某化学兴趣小组的同学开展了以下探究活动.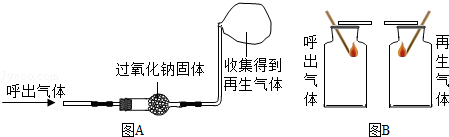
【实验探究一】将呼出气体通过下图
中的装置,收集得到一瓶再生气体.在收集一瓶呼出的气体.将两支燃着的同种木条分别同时伸入呼出气体和再生气体中,如下图
,比较分析呼出气体和再生气体中氧气含量的多少.
【分析讨论】图
的实验是通过比较来比较两种气体中氧气含量的多少.请说明呼吸面具或潜水艇用过氧化钠作为供氧剂的最大优点是.
实验探究一结束后,同学们将图
装置中的残留固体溶于水,得到了一杯无色溶液,他们对溶液的溶质成分进行探究:
【提出猜想】猜想Ⅰ:溶液是
;猜想Ⅱ:溶质是;猜想Ⅲ:溶质是
和
【实验探究二】取上述溶液少许于试管中,滴加澄清石灰水,产生的现象,证明猜想Ⅰ不成立.
同学们经过实验探究证明猜想Ⅲ成立,请你写出证明猜想Ⅲ成立的实验步骤和现象.
| 实验步骤和现象 |
结论 |
| 猜想Ⅲ成立 |
某无土栽培营养液的配方中可能含有氯化钾、硫酸铵、碳酸氢氨中的一种或几种物质,为确定配方的成分,化学兴趣小组的同学开展了以下探究活动:
(1)【实验探究一】取少量固体样品在研体中与熟石灰混合研磨,有刺激性气味的气体产生,该气体能使湿润的红色石蕊试纸变色,写出可能发生该反应的一个化学方程式.
(2)【实验探究二】另取少量固体样品溶于水得到溶液A,按下图所示进行实验,现象如图所述(设发生的反应都恰好完全进行).请你回答下列问题: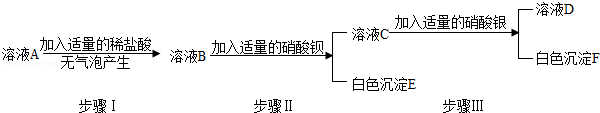
①白色沉淀E是.
②小明认为由实验探究二可以确定该化肥中一定含有氯化钾和硫酸铵,一定没有碳酸氢铵.小强认为这个结论不正确,他的理由.为了使小明的结论正确,小强对上述实验进行了改动,他的做法是.