(12分)工业上以碳酸锰矿为主要原料生产MnO2的工艺流程如下:
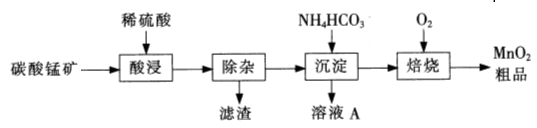
有关氢氧化物开始沉淀和沉淀完全的pH如下表:
| 氢氧化物 |
Al(OH)3 |
Fe(OH)3 |
Fe(OH)2 |
Pb(OH)2 |
Mn(OH)2 |
| 开始沉淀的pH |
3.3 |
1.5 |
6.5 |
8.0 |
8.3 |
| 沉淀完全的pH |
5.2 |
3.7 |
9.7 |
8.8 |
9.8 |
请问答下列问题:
(1)为了提高锰矿中锰元素的浸取率,可采取的措施为 。
(2)写出焙烧过程反应的化学方程式 。
(3)MnO2粗品中含有少量Mn3O4,可以用稀硫酸处理,将其转化为MnSO4和MnO2,然后再用氧化剂将Mn2+转化为MnO2,制得优质MnO2。写出Mn3O4与稀硫酸反应离子方程式:
。
(4)某兴趣小组在实验室中除去酸浸后的溶液有少量Fe2+、Fe3+.A13+、Pb2+等,得到只含的Mn2+、 SO42-的溶液,其除杂过程设计如下:
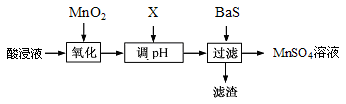
①加入MnO2氧化时发生的离子方程式为 。
②试剂X最好选用 (填字母)。
a.NaOH 溶液 b。KMnO4溶液 c。稀硝酸 d.MnCO3
③滤渣的成分是 。
碳及其化合物在人类生产、生活中的应用非常广泛。“低碳生活”不再只是一种理想,更是一种值得期待的生活方式。
(1)已知:①2CH4(g)+3O2(g)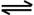 2CO(g)+4H2O(l)△H1=-1214.6kJ/mol
2CO(g)+4H2O(l)△H1=-1214.6kJ/mol
②2CO(g)+ O2(g)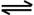 2CO2(g) △H2=-566kJ/mol,
2CO2(g) △H2=-566kJ/mol,
则甲烷与氧气反应生成二氧化碳和液态水的热化学方程式为。
(2)已知在恒温恒压下密闭容器的可逆反应CH4(g)+ H2O(g)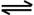 CO(g)+3H2(g)
CO(g)+3H2(g)
①该可逆反应一定达到平衡的标志是。
| A.v(CH4)正=3v(H2)逆 |
| B.水蒸气的浓度与一氧化碳的浓度相等 |
| C.平均相对分子质量不随时间的变化而变化 |
| D.密度不随时间的变化而变化 |
②该可逆反应在不同条件下,测得CH4转化率随时间变化如图所示,与实验a相比,b的实验条件是。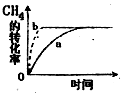
(3)将不同物质的量的CO(g)和H2O(g)分别通入到体积为2L的恒容密闭容器中,进行反应:
CO(g)+H2O(g) 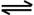 CO2(g)+H2(g);△H得到如下三组数据:
CO2(g)+H2(g);△H得到如下三组数据:
| 实验组 |
温度/℃ |
起始量/mol |
平衡量/mol |
达到平衡所需时间/min |
||
| H2O |
CO |
CO2 |
CO |
|||
| 1 |
650 |
2 |
4 |
1.6 |
2.4 |
5 |
| 2 |
900 |
1 |
2 |
0.4 |
1.6 |
3 |
| 3 |
900 |
a |
b |
c |
D |
t |
①实验1中以v(H2)表示的反应速率为。
②实验2中的平衡常数是(计算结果保留两位小数)。
③该反应的△H0(填“>”或“<”)。
④若实验3要达到与实验2相同的平衡状态(即各物质的质量分数分别相等),则a、b应满足的关系
是(用含a、b的式子表示)。
有A、B、C、D、E、F、G七种前四周期元素,原子序数依次增大,其相关信息如下表:
| 元素 |
元素的相关信息 |
| A |
存在多种核素,其中一种核素没有中子 |
| B |
核外电子排布式三个能级上的电子数相同 |
| C |
其第一电离能比同周期相邻元素的第一电离能都大 |
| D |
最外层电子数是内层电子数三倍的元素 |
| E |
单质或其化合物在火焰灼烧时,火焰呈黄色 |
| F |
位于第三周期ⅦA族 |
| G |
未成对电子数最多的副族元素 |
(1)G元素的价层电子排布式为。
(2)D、E、F三种元素的简单离子的离子半径由大到小的顺序是(用微粒符号表示)。
(3)B、C、F三种元素的最高价氧化物的水化物的酸性最强的是(写名称)。
(4)由上述两种元素组成的与O3互为等电子体的负一价阴离子的化学式为。
(5)由B、C、E三种元素的三原子组成的含σ键和π键的离子化合物的电子式。
(6)由A、B、D三种元素组成的有两种官能团的能形成分子内氢键的芳香族化合物的结构简式为(任写一种)。
(7)如图所示装置,两玻璃管中盛满滴有酚酞溶液的EF饱和溶液,C(Ⅰ)、C(Ⅱ)为多孔石墨电极。接通S1后,C(Ⅰ)附近溶液变红,两玻璃管中有气体生成。一段时间后(两玻璃管中液面未脱离电极),断开S1,接通S2,电流表的指针发生偏转。此时:C(Ⅱ)的电极反应式是。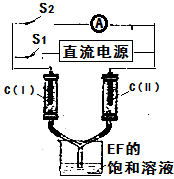
(本题共14分)碘海醇为非离子型造影剂,尤适用于有造影剂反应的高危因素的病人。
下面是以化合物A为原料合成碘海醇的路线:
其中R-为-CH2CH(OH)CH2OH
请回答以下问题:
48.碘海醇的分子式为________。
49.A是苯的同系物,其蒸气相对氢气的密度是53,则A的结构简式是。
50.写出A的侧链与氯气发生一氯取代的条件_____________。
51.反应①→⑤中,属于取代反应的是_____________(填序号)。
52.写出能同时满足下列条件的D的两种同分异构体的结构简式:________。
Ⅰ.苯环上有3个取代基,苯环上的一卤代物有2种;
Ⅱ.能发生银镜反应,水解产物之一能与FeCl3溶液发生显色反应;
Ⅲ.含有1个α-氨基酸的结构(例如: 属于α-氨基酸);
属于α-氨基酸);
53.已知:①
②
③ 呈弱碱性,易被氧化
呈弱碱性,易被氧化
请写出以  和(CH3CO)2O为原料制备染料中间体
和(CH3CO)2O为原料制备染料中间体 的合成路线流程图(无机试剂任用)。
的合成路线流程图(无机试剂任用)。
(合成路线常用的表示方式为: )
)
__________________________________________________________________________
(本题共8分)炔烃与羰基化合物在强碱性条件下于乙醚中发生反应,可得到炔醇,反应原理为:
以下合成路线是某化工厂生产流程的一部分:
已知: 
请回答下列问题:
43.写出C中含氧官能团的名称。
44.有关C的说法正确的是
a.不能使酸性高锰酸钾褪色 b.能和氢氧化钠溶液反应
c.能使溴的四氯化碳溶液褪色 d.能与乙酸发生酯化反应
45.经测定,E的分子结构与天然橡胶结构相同,写出D的名称(系统命名)。
46.⑤的反应类型是;B的结构简式是。
47.写出反应⑦的化学方程式。
(本题共12分)氯酸镁[ Mg(ClO3)2 ]常用作催熟剂、除草剂等,实验室制备少量Mg(ClO3)2·6H2O的流程如下:
已知:①卤块主要成分为MgCl2·6H2O,含有MgSO4、FeCl2等杂质。②四种化合物的溶解度(S)随温度(T)变化曲线如图所示。
38.加速卤块在KMnO4溶液中溶解的措施有:(写出一点即可)。
39.加入MgO的作用是;过滤后所得滤渣的主要成分为。
40.加入NaClO3饱和溶液后发生反应的化学方程式为,再进一步制Mg(ClO3)2·6H2O晶体的实验步骤依次为:①加热蒸发;②;③;④过滤洗涤。
产品中Mg(ClO3)2·6H2O含量的测定:
步骤1:准确称量3.50 g产品配成100 mL溶液。
步骤2:取10.00 mL试液于锥形瓶中,加入10.00 mL稀硫酸和20 .00mL 1.000 mol/L的FeSO4溶液,微热。
步骤3:冷却至室温,用0.100 mol/L K2Cr2O7溶液滴定剩余的Fe2+至终点。此过程中反应的离子方程式为:Cr2O72-+6Fe2++14H+→2Cr3++6Fe3++7H2O。
步骤4:将步骤2、3重复两次
41.①写出步骤2中发生反应的离子方程式:;
②步骤3中若滴定前不用标准液润洗滴定管,将会导致最终结果(填“偏大”、“偏小”或“不变”);
42.若平均消耗K2Cr2O7溶液15.00 mL,则产品中Mg(ClO3)2·6H2O的质量分数为。