从含镁、钾盐湖水中蒸发最后得到的产物中含光卤石(xKCl·yMgCl2·zH2O),它在空气中极易潮解、易溶于水,是制造钾肥和提取金属镁的重要原料,其组成可通过下列实验测定:
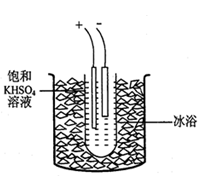
①准确称取11.100g样品溶于水,配成l00.00mL溶液。
②取25.00mL溶液,加入NaOH溶液至沉淀完全,过滤、洗涤、干燥至恒重,得到白色固体0. 580g。
③另取25.00mL溶液,加入足量的硝酸酸化的AgNO3溶液至沉淀完全,过滤、洗涤、干燥至恒重,得到白色固体4.305g。
(1)步骤②中检验沉淀完全的方法是 。
(2)若步骤③中为了加快干燥速度,置于阳光直射下干燥沉淀,结果出现沉淀变黑。测得光卤石结晶水含量将 (填“偏高”、或“偏低”或“不变”)。
(3)通过计算确定样品的组成(写出计算过程)。
A、B、C、D、E、F六种物质在一定条件下有如下图所示的相互转化关系,所有反应物和生成物均已给出。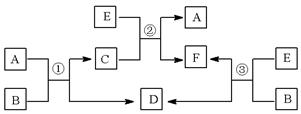
(1)若反应①、②、③均为溶液中的置换反应,A、D、E为第ⅦA族元素单质。则A、D、E的氧化性由强到弱的顺序为(用化学式表示)________________________。
(2)若B是某元素R的氢化物,B的沸点大于与其同主族的其他元素氢化物的沸点,且B在常温下为液态;C是一种有磁性的化合物;E是一种无色、无味的有毒气体。则反应①的化学方程式___________________,③的化学方程式______________。
(3)若B由短周期元素X、Y组成,且X、Y原子个数比为1∶1,B晶体中既含离子键,又含非极性共价键;绿色植物的光合作用和呼吸作用可实现自然界中 D、E的循环。则B的电子式为_________________,反应①的离子方程式_____________________________。
D、E的循环。则B的电子式为_________________,反应①的离子方程式_____________________________。
甲、乙、丙为常见单质,乙、丙两元素在周期表中位于 同一主族。X、A、B、C、D、E、F、G均为常见的化合物,其中A和X的摩尔质量相同,A、G的焰色反应为黄色。在一定条件下,各物质相互转化关系如右图。请回答:
同一主族。X、A、B、C、D、E、F、G均为常见的化合物,其中A和X的摩尔质量相同,A、G的焰色反应为黄色。在一定条件下,各物质相互转化关系如右图。请回答: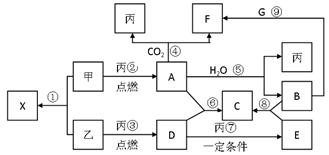
(1)写化学式:丙_____E________
(2)X的电子式为_____________。
(3)写出反应⑥的化学反应方程式:。
(4)写出B与G溶液反应生成F的离子方程式:。
(5)在上图的反 应中,不属于氧化还原反应的是(填序号)____________________。
应中,不属于氧化还原反应的是(填序号)____________________。
(6)将8 g乙在足量丙中燃烧,所得气体D通入100mL 3.5mol·L-1的B溶液中,完全吸收 后,溶液中的溶质及其物质的量分别为;若同体积的气体D通入100mL 2.5mo
后,溶液中的溶质及其物质的量分别为;若同体积的气体D通入100mL 2.5mo l·L-1的B溶液中,完全吸收后,溶液中所含离子的物质的量浓度由大到小的顺序为。
l·L-1的B溶液中,完全吸收后,溶液中所含离子的物质的量浓度由大到小的顺序为。
某一反应体系中的物质有:HCl、SnCl2、H2SnCl6、As、H3AsO3、H2O,
已知:As是产物之一。
(1)写出并配平该反应的化学方程式;
(2)在该反应中,得电子的物质是,被氧化的元素是;
(3)在反应中,每转移1 mol电子,消耗(或生成)HClmol;
(4)下列叙述正确的是(填写序号)。
a.在相同条件下,第VIIA族元素的阴离子的还原性从上到下逐渐增强
b.Sn和Pb位于同一主族,其+4价的化合物均很稳定
c.在相同条件下,还原性顺序:S2->I->Fe2+>Br->Cl-
 甲醇被称为2l世纪的新型燃料,工业上通过下列反应①和②,用CH4和H2O为原料来制备甲醇。
甲醇被称为2l世纪的新型燃料,工业上通过下列反应①和②,用CH4和H2O为原料来制备甲醇。
① CH4(g)+H2O(g) 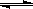 CO(g)+3H2(g)△H1
CO(g)+3H2(g)△H1
② CO(g)+2H2(g) 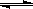 CH3OH(g)△H2
CH3OH(g)△H2
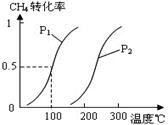
将0.20mol CH4和0.30 mol H2O(g)通入容积为10L的密闭容器中,在一定条件下发生反应①,达到平衡时,CH4的转化率与温度、压强的关系如右图。
(1)温度不变,缩小体积,增大压强,①的反应速率(填“增大”、“减小”或“不变”),平衡向方向移动。
(2)反应①的△H10(填“<”、“=”或“>”),其平衡常数表达式为K=,100℃时的平衡常数值是。
(3)在压强为0.1 MPa条件下, 将a mol CO与 3amol H2的混合气体在催化剂作用下进行反应②生成甲醇。为了寻找合成甲醇的温度和压强的适宜条件,某同学设计了三组实验,部分实验条件已经填在下面实验设计表中。请在下表空格中填入剩余的实验条件数据。
| 实验编号 |
T(℃) |
n (CO)/n(H2) |
P(MPa) |
| I |
150 |
1/3 |
0.1 |
| II |
5 |
||
| III |
350 |
5 |
A、B、C、D四种芳香族化合物都是某些植物挥发油中的主要成分,有的是药物,有的是香料。它们的结构简式如下所示: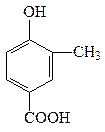
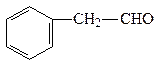
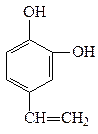

A BC D
(1)A中的含氧官能团名称是。
(2)B与足量氢气充分反应的产物的结构简式为。
(3)D发生聚合反应的产物的结构简式为。
(4)A能与乙醇发生反应生成一种有特殊香味的物质,请写出该反应的方程式:
。
(5)关于上述四种物质的说法中正确的是。
A.都能与Na反应放出H2
B.C、D均能使溴的四氯化碳溶液褪色
C.A和C均能与NaHCO3溶液反应放出CO2
D.1molC最多能与4molBr2发生反应